Дата создания: 23 мая 2017
Обновлено: 27 июня 2021
Как продлить нашу жизнь с помощью генной терапии
Все подходы к генной терапии старения делятся на те, где в организм доставляется ген долголетия, и на те, где «выключается» ген или путь старения. В сравнении с другими подходами к продлению жизни генную терапию достаточно провести только один раз за всю жизнь. Внедрение гена теломеразы (TERT), нарушение работы гена Agtr1a, нокаут GHRKO, нарушение в генах, кодирующих рецепторы к ИФР-1, сверхэкспрессия FGF21, нокаут AC5, удаление RIP3, редактирование гена PCSK9, сверхэкспрессия Klotho, нокаут RAGE, сверхэкспрессия BubR1, сверхэкспрессия MTH1 - всё это примеры самых эффективных способов генной инженерии, позволяющих продлевать жизнь до 30%. Чтобы добиться более существенных результатов в генной терапии старения, необходимо комбинировать разные подходы. Сегодня частично повторить эффекты генотерапии можно с помощью лекарств и добавок.
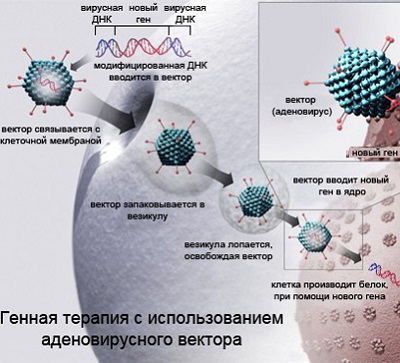
Все подходы к генной терапии старения делятся на те, где в организм доставляется ген долголетия, и на те, где «выключается» ген или путь старения.
Концепция генной терапии существует на протяжении последних двадцати-тридцати лет. Она заключается в том, что наиболее радикальный способ борьбы с заболеваниями – это уничтожение самой генетической причины болезни, а не его следствий. Генная терапия – это вмешательство в работу клеточного «завода» по производству белков. Она позволяет, как активировать работу нужных генов, так и «выключать» вредные. В первом случае в клетку доставляют ген, с которого начинает считываться белок, необходимый для терапии заболевания. А во втором – в клетку вводятся регуляторные РНК, которые блокируют экспрессию «вредного» гена.
По данным журнала Gene Medicine, в 2015 году было проведено 2210 клинических испытаний по генной терапии различных болезней. Это, преимущественно рак (64%), моногенные заболевания, вызванные мутацией в одном гене (9,5%), сердечно-сосудистые (7,9%) и инфекционные (7,9%). Для ряда заболеваний генная терапия оказалась вполне успешной. К настоящему времени уже 4 генотерапевтических лекарства допущены к продаже. В Китае в 2003 году выпущен «Гендицин» (Gendicine) – препарат для лечения плоскоклеточного рака головы и шеи на основе гена p53, а в 2006 - «Онкорин» (Oncorine) – онколитический вирус для лечения назофарингеальной карциномы. В Европе в 2012 году запущено производство препарата «Глибера» (Glybera), предназначенного для терапии наследственного дефицита липопротеинлипазы (ЛПЛ) путем доставки одноименного гена. А в России допущен к продаже препарат «Неоваскулген» для лечения заболеваний периферических артерий. Он представляет собой ген VEGF (фактора роста эндотелия сосудов).
 Использование технологии редактирования генома CRISPR/Cas9 открывает новые возможности в генной терапии. CRISPR/Cas9 позволяет очень точно и безопасно изменять ДНК клеток. И если совместить технологию CRISPR/Cas9 с доставкой при помощи аденоассоциированных вирусов, то это, по-видимому, позволит системно воздействовать на организм и совершенно безопасно изменять геном очень большого числа клеток. Использование CRISPR/Cas превзошло все ожидания. Она позволила с минимальным числом ошибок как «выключать» нужные гены, так и встраивать новые гены в строго определенные участки генома. А совсем недавно, в декабре 2015 года научная группа Фенга Джанга видоизменила данную систему так, что она стала и вовсе безошибочной, что было опубликовано в ведущем научном журнале Science. Ученые заменили 3 аминокислоты («кирпичика», из которых состоит белок) в эндонуклеазе Cas9, после чего число ошибок такой системы свелось практически к нулю.
Использование технологии редактирования генома CRISPR/Cas9 открывает новые возможности в генной терапии. CRISPR/Cas9 позволяет очень точно и безопасно изменять ДНК клеток. И если совместить технологию CRISPR/Cas9 с доставкой при помощи аденоассоциированных вирусов, то это, по-видимому, позволит системно воздействовать на организм и совершенно безопасно изменять геном очень большого числа клеток. Использование CRISPR/Cas превзошло все ожидания. Она позволила с минимальным числом ошибок как «выключать» нужные гены, так и встраивать новые гены в строго определенные участки генома. А совсем недавно, в декабре 2015 года научная группа Фенга Джанга видоизменила данную систему так, что она стала и вовсе безошибочной, что было опубликовано в ведущем научном журнале Science. Ученые заменили 3 аминокислоты («кирпичика», из которых состоит белок) в эндонуклеазе Cas9, после чего число ошибок такой системы свелось практически к нулю.
Использование CRISP/Cas9 особенно актуально для генной терапии старения, где требуется воздействовать на пути долголетия, общие для большинства клеток организма. По генной терапии старения до 2015 года не проведено ни одного клинического испытания на людях, что неудивительно, поскольку старение до сих пор не признано болезнью. Кроме того, генная терапия старения пока еще очень молодая и развивающаяся область. Сейчас все исследования по генной терапии старения проводятся на модельных мышах, крысах, обезьянах и клеточных культурах человека - клетках в пробирке. Все подходы к генной терапии старения делятся на те, где в организм доставляется ген долголетия, и на те, где вводятся малые РНК, «выключающие» ген или путь старения. То есть в первом случае вводится нечто полезное для долголетия, а во втором – отключается вредное.
Ссылка на источник:
- https://ru.wikipedia.org/wiki/CRISPR
В строгом смысле исследований по генной терапии старения на млекопитающих до 2015 года было проведено только два. Гораздо больше работ моделируют генную терапию на трансгенных мышах. В таких исследованиях терапевтический ген не доставляют в организм взрослой мыши, а при помощи генной инженерии создают мышей, геном которых изменен с рождения. Как и генная терапия, это позволяет исследовать, как увеличение или снижение активности разных генов влияет на продолжительность жизни и старение организма.
А теперь давайте рассмотрим, что можно теоретически сделать с помощью генной терапии и генной инженерии для борьбы со старением.
Преимущество генной терапии перед другими способами продления жизни.
Зачем нам генная терапия, если можно использовать таблетки от старения (геропротекторы)? В сравнении с другими подходами к продлению жизни (например, геропротекторами или ограничением питания, продлевающими жизнь до 30-50%) генную терапию достаточно провести только один раз за всю жизнь, а таблетки нужно пить всё время и не забывать - иначе и результат будет не полным. Например, в работе Андржея Бартке 2001 года ограничение питания продлило жизнь мышам на 30%. Однако мыши употребляли низкокалорийную диету до 670 дней подряд – то есть каждый день, в течение половины своей жизни! Для большинства людей - это малореально. А в эксперименте по генной терапии Марии Бласко (будет рассмотрено дальше в этой статье) 2012 года генная терапия теломеразой привела к немного меньшему эффекту – мыши стали жить дольше на 20%. Однако в этой работе мыши получили только 1 инъекцию лекарства в кровь за всю жизнь в довольно преклонном возрасте! Поэтому, если мы говорим о трансляции исследований по продлению жизни на человека, то генная терапия имеет абсолютное преимущество, поскольку не снижает качество жизни из-за необходимости постоянного лечения – соблюдать ежедневно определенную диету или же постоянно употреблять геропротекторы или другие лекарства.
Кроме того, лекарственные средства имеют ограничения по биодоступности в различные ткани и органы, а также обладают побочными действиями - большими, чем генотерапия. Эффективность и практичность генотерапии потенциально значительно выше.
Внедрение гена теломеразы (TERT) у двухлетних мышей дикого типа (40-50 лет по человеческим меркам) с помощью одной инъекции увеличивает длину теломер и продлевает им жизнь на 20%.
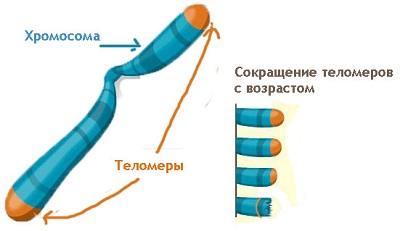 История исследований теломеразы уходит корнями еще в 1961 год. Американский исследователь Леонард Хейфлик культивировал фибробласты эмбриона человека в пробирке и заметил, что они способны поделиться не более 50 раз, после чего стареют. А если брать клетки более старых доноров, то делятся они и того меньше. Ученый предположил, что в клетках существует некий счетчик деления, ограничивающий их общее число. Спустя 10 лет российским ученым Алексеем Оловниковых был предложен гипотетический механизм работы этого счетчика. Оловников предположил, что при делении клеток концы хромосом, называемые теломерами, немного сокращаются. А когда теломеры достигают критической длины, клетка перестает делиться и стареет. В нестареющих клетках (например, половых и эмбриональных стволовых), напротив, должен существовать фермент, который удлиняет теломеры, позволяя клеткам делиться практически до бесконечности. Кроме того, было показано, что повреждение гена теломеразы сильно сокращает жизнь модельных животных и приводит к возникновению синдрома преждевременного старения - прогерии.
История исследований теломеразы уходит корнями еще в 1961 год. Американский исследователь Леонард Хейфлик культивировал фибробласты эмбриона человека в пробирке и заметил, что они способны поделиться не более 50 раз, после чего стареют. А если брать клетки более старых доноров, то делятся они и того меньше. Ученый предположил, что в клетках существует некий счетчик деления, ограничивающий их общее число. Спустя 10 лет российским ученым Алексеем Оловниковых был предложен гипотетический механизм работы этого счетчика. Оловников предположил, что при делении клеток концы хромосом, называемые теломерами, немного сокращаются. А когда теломеры достигают критической длины, клетка перестает делиться и стареет. В нестареющих клетках (например, половых и эмбриональных стволовых), напротив, должен существовать фермент, который удлиняет теломеры, позволяя клеткам делиться практически до бесконечности. Кроме того, было показано, что повреждение гена теломеразы сильно сокращает жизнь модельных животных и приводит к возникновению синдрома преждевременного старения - прогерии.
После открытия теломеразы десятки ученых загорелись тем, чтобы сделать на ее основе лекарство от старости. Казалось бы, «включение» теломеразы во всех клетках может сделать организм бессмертным. Однако вскоре возникли опасения в связи с тем, что активный синтез теломеразы наблюдается и в 90% раковых опухолей. Встал вопрос: не приведет ли активация теломеразы к риску злокачественной трансформации? Кроме того, оказалось, что старение клеток далеко не всегда сопровождается сокращением теломер. Например, в случае эпителиальных клеток слизистой полости рта или роговицы глаза человека. Это говорило о том, что одной активации теломеразы может быть недостаточно для омоложения всего организма. Перед тем как перейти к генной терапии, эффекты теломеразы исследовались на трансгенных мышах. Оказалось, что если «включить» ген TERT во всех клетках мыши, то продолжительность жизни увеличивается на 40%! Однако постоянная активность теломеразы увеличивала и риск рака. Поэтому стал вопрос о том, как активировать работу теломеразы на более короткий срок.
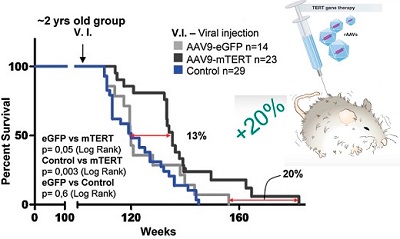 Именно это было сделано в работе Марии Бласко 2012 года (см. график). Ген теломеразы доставлялся в организм мыши при помощи аденоассоциированного вируса (AAV9), способного обеспечивать системную доставку. Аденоассоциированные вирусы характеризуются высокой безопасностью: они не встраивают доставляемый ген в геном хозяина, и поэтому не приводят к мутагенезу (нет риска рака). Кроме того, они почти не вызывают иммунный ответ. Кроме того, терапия геном TERT оказалась совершенно безопасной: риск рака у мышей не увеличивался. Двухлетним мышам делалась одна инъекция, с аденовирусом, к которому вставлен ген теломеразы. Это продлевало жизнь мышам на 20 % (как показано на графике слева). А это теоретически может позволить сделать людям в возрасте 40-50 лет одну инъекцию такого лекарства и продлить жизнь ещё на 8-12 лет.
Именно это было сделано в работе Марии Бласко 2012 года (см. график). Ген теломеразы доставлялся в организм мыши при помощи аденоассоциированного вируса (AAV9), способного обеспечивать системную доставку. Аденоассоциированные вирусы характеризуются высокой безопасностью: они не встраивают доставляемый ген в геном хозяина, и поэтому не приводят к мутагенезу (нет риска рака). Кроме того, они почти не вызывают иммунный ответ. Кроме того, терапия геном TERT оказалась совершенно безопасной: риск рака у мышей не увеличивался. Двухлетним мышам делалась одна инъекция, с аденовирусом, к которому вставлен ген теломеразы. Это продлевало жизнь мышам на 20 % (как показано на графике слева). А это теоретически может позволить сделать людям в возрасте 40-50 лет одну инъекцию такого лекарства и продлить жизнь ещё на 8-12 лет.
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/22585399
- www.ncbi.nlm.nih.gov/pmc/articles/PMC3494070/figure/fig03
- www.ncbi.nlm.nih.gov/pubmed/27462436
Сегодня простимулировать теломеразу можно и лекарствами. Так 1 месячный курс валсартана 20 мг + флувастатина 10-20 мг. существенно повышает активность теломеразы в 3.28 раза, которая достоверно коррелирует с улучшением эндотелиальной функции (омоложением сосудов) и снижением воспаления в кровеносных сосудах. И этот повышенный уровень теломеразы сохраняется, постепенно снижаясь, ещё полгода. Но на сколько эффективно такое повышение теломеразы влияет на теломеры нужно ещё определить.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/26214555
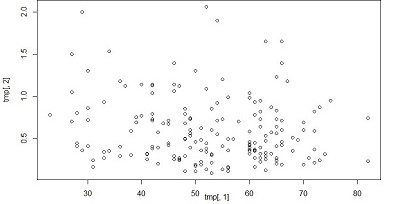 Важно знать, что теломеры не обязательно могут продлить нам жизнь, если подобную терапию делать не в нужный момент и слишком долго. К тому же одна лишь стимуляция теломеразы может не удлинить теломеры. Активность теломеразы с возрастом почти не меняется — вот посмотрите график слева. А теломеры всё равно сокращаются. Также сегодня есть на рынке препарат, который повышает активность теломеразы - ТА-65. Он очень дорогой, а жизнь мышей никак не продлевал в исследованиях. И так со многими пустышками-лекарствами.
Важно знать, что теломеры не обязательно могут продлить нам жизнь, если подобную терапию делать не в нужный момент и слишком долго. К тому же одна лишь стимуляция теломеразы может не удлинить теломеры. Активность теломеразы с возрастом почти не меняется — вот посмотрите график слева. А теломеры всё равно сокращаются. Также сегодня есть на рынке препарат, который повышает активность теломеразы - ТА-65. Он очень дорогой, а жизнь мышей никак не продлевал в исследованиях. И так со многими пустышками-лекарствами.
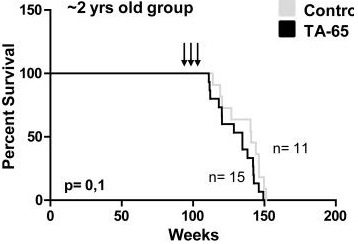 Вот смотрите график слева. Двухлетним мышам, начали давать ТА-65 для повышения теломеразы, как и в предыдущем исследовании. Только в предыдущем исследовании мышам делали инъекцию для генной терапии. Но препарат ТА-65 никак не продлил жизнь мышам в отличии от генной терапии (см. график слева).
Вот смотрите график слева. Двухлетним мышам, начали давать ТА-65 для повышения теломеразы, как и в предыдущем исследовании. Только в предыдущем исследовании мышам делали инъекцию для генной терапии. Но препарат ТА-65 никак не продлил жизнь мышам в отличии от генной терапии (см. график слева).
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/21426483
Кроме того, по теломерам сейчас не всё ясно. Исследования показывают (при сравнении около 60 видов млекопитающих), что чем длиннее теломеры у вида, тем быстрее накапливаются у него мутации ДНК, больше раковых опухолей и короче продолжительность жизни. Длина теломер обратно коррелирует с продолжительностью жизни. Это даёт основания предполагать, что результат по продлению жизни теломеразой, который был получен на мышах с помощью одной инъекции, может не продлить жизнь людям. Вопрос по теломерам для людей остаётся открытым.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/21518243
Вывод: в будущем мы возможно сможем с помощью внедрения гена теломеразы (TERT) в возрасте 40-50 лет с помощью одной инъекции увеличивать длину теломер и продлевать жизнь в среднем на 8-12 лет. А сегодня мы можем добиваться возможного эффекта с помощью одномесячной терапии 1 раз в полгода комбинацией препаратов валсартана 20 мг + флувастатина 10-20 мг, либо телмисартан + аторвастатин 10 мг. По крайне мере эти препараты в комбинации способны стимулировать саму теломеразу.
Нарушение работы гена Agtr1a, кодирующего рецепторы ангиотензина AT1a продлевает жизнь трансгенным мышам на 26% в сравнении с мышами дикого типа.
Антагонисты рецепторов ангиотензина II, или блокаторы АТ1-рецепторов — одна из новых групп антигипертензивных средств (лекарства для лечения артериального давления). К таким лекарствам можно отнести все лекарства группы сартанов (например, телмисартан). Как было показано в исследованиях, эти лекарства сильно продлевают жизнь животным и даже людям. Например, один из сартанов лозартан, когда его давали крысам линии вистар, то он продлевал их максимальную продолжительность жизни на 18%.
Ссылка на исследование:
- http://m.ajpheart.physiology.org/content/293/3/H1351.full
Но можно повлиять на АТ1-рецепторы и генетически, чтобы всю жизнь не пить такие лекарства. Этого можно достигнуть, повлияв на ген Agtr1a. Кроме того, генетическое воздействие на АТ1-рецепторы более эффективно, так как лекарство возможно не проникает во все ткани и органы.
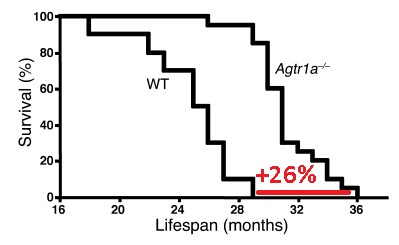 Как мы можем видеть на графике слева, нарушение работы гена Agtr1a, кодирующего рецепторы ангиотензина AT1a продлевает жизнь трансгенным мышам по сравнению с мышами дикого типа на 26%. Чтобы получить такой эффект нужно либо пить лекарства группы сартанов с самого детства, либо с самого детства произвести такие генетические вмешательства. Судя по исследованиям органы и ткани мышей старели функционально на 26% медленнее.
Как мы можем видеть на графике слева, нарушение работы гена Agtr1a, кодирующего рецепторы ангиотензина AT1a продлевает жизнь трансгенным мышам по сравнению с мышами дикого типа на 26%. Чтобы получить такой эффект нужно либо пить лекарства группы сартанов с самого детства, либо с самого детства произвести такие генетические вмешательства. Судя по исследованиям органы и ткани мышей старели функционально на 26% медленнее.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pmc/articles/PMC2648681

Такая генотерапия может быть использована и у уже возрастных людей для продления жизни. Особенно у людей с повышенным артериальным давлением, подобная терапия (влияющая на АТ1-рецепторы) может помочь им не использовать лекарства для снижения артериального давления, а также медленнее стареть.
Вывод: В будущем с помощью генной инженерии или генотерапии мы можем нарушать работу гена, кодирующего рецепторы ангиотензина AT1 и продлевать себе жизнь на 5-15 лет в зависимости от возраста таких вмешательств. А сегодня частичного эффекта (ввиду не полной биодоступности во все ткани организма) можно добиваться терапией курсовых приёмов в малых дозах лекарства телмисартан в дозе 10 мг в сутки, если нет высокого артериального давление - иначе дозы выше.
Нокаут гена, кодирующего рецепторы гормона роста GHRKO (выборочное удаление рецепторов гормона роста) продлевает жизнь трансгенным мышам примерно на 30% в сравнении с мышами дикого типа.
 В организме человека гормон роста регулирует уровень ИФР-1 (инсулин подобный фактор роста 1 типа). Чем выше гормон роста, тем выше и ИФР-1. Сегодня один из самых доказанных почти на всех видах животных метод продления жизни - это оптимизация ИФР-1 (инсулин подобный фактор роста 1 типа) с помощью голоданий, либо с помощью диеты FMD. Но для этого нужно всю жизнь соблюдать диету, что по силам далеко не каждому.
В организме человека гормон роста регулирует уровень ИФР-1 (инсулин подобный фактор роста 1 типа). Чем выше гормон роста, тем выше и ИФР-1. Сегодня один из самых доказанных почти на всех видах животных метод продления жизни - это оптимизация ИФР-1 (инсулин подобный фактор роста 1 типа) с помощью голоданий, либо с помощью диеты FMD. Но для этого нужно всю жизнь соблюдать диету, что по силам далеко не каждому.
Ссылки на исследования:
- www.karger.com/Article/Abstract/212538
- www.ncbi.nlm.nih.gov/pubmed/19590001
- www.ncbi.nlm.nih.gov/pubmed/26094889
ИФР-1 - гормон, который связывается с рецепторами ИФР-1. И вот, если генетически нарушить работу рецепторов ИФР-1, то можно частично имитировать недостаток ИФР-1.
 Нарушение в генах, кодирующих рецепторы к ИФР-1 у евреев долгожителей Ашкеназии возможно объясняет их феномен долгожительства. Похоже, что у супердолгожителей, которые живут более 100 лет, в детстве и во взрослом возрасте был оптимальный (не такой высокий, как у остальных людей) уровень ИФР-1, либо был высокий ИФР-1, но при этом генетически обусловленный дефект рецепторов к ИФР-1.
Нарушение в генах, кодирующих рецепторы к ИФР-1 у евреев долгожителей Ашкеназии возможно объясняет их феномен долгожительства. Похоже, что у супердолгожителей, которые живут более 100 лет, в детстве и во взрослом возрасте был оптимальный (не такой высокий, как у остальных людей) уровень ИФР-1, либо был высокий ИФР-1, но при этом генетически обусловленный дефект рецепторов к ИФР-1.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/18316725
А вдруг оптимизация ИФР-1 просто совпадение. Ведь долгожителей не так много. Нужно провести исследования на больших группах людей и выяснить, как влияет высокий ИФР-1 на их смертность. И такие исследования есть.
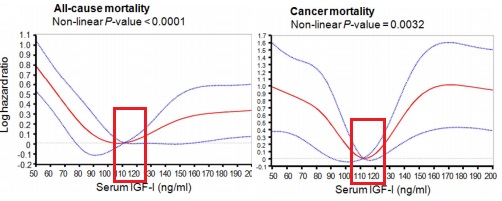 Данные исследований предлагают предположить, что есть уровень ИФР-1, выше и ниже которого риск смерти от рака и от других причин у людей повышается. Этот диапазон примерно от 105 нг/мл до 120 нг/мл. (см. график слева). Так у людей в возрасте от 50 до 65 лет ИФР-1 на уровне от 105 до 120 нг/мл был связан с наименьшей общей смертностью в следующие 18 лет.
Данные исследований предлагают предположить, что есть уровень ИФР-1, выше и ниже которого риск смерти от рака и от других причин у людей повышается. Этот диапазон примерно от 105 нг/мл до 120 нг/мл. (см. график слева). Так у людей в возрасте от 50 до 65 лет ИФР-1 на уровне от 105 до 120 нг/мл был связан с наименьшей общей смертностью в следующие 18 лет.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/23015658
Но мы можем сделать такие же изменения в ИФР-1 с помощью генной инженерии или генной терапии. Так как ИФР-1 тем больше, чем выше гормон роста, то можно снизить ИФР-1 просто, снизив чувствительность рецепторов гормона роста. И вот как это выглядит на животных.
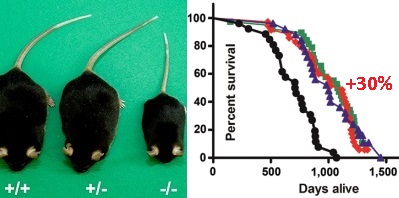 Нокаут у мышей гена, кодирующего рецепторы гормона роста GHRKO (выборочное удаление рецепторов гормона роста) продлевает жизнь трансгенным мышам примерно на 30% в сравнении с мышами дикого типа. На графике слева: чёрный цвет линии - это мыши дикого типа. График синего цвета - это мыши дикого типа, которых недокармливали, чтобы снижать у них ИФР-1 (они прожили на 30% дольше мышей дикого типа). Красная линия - это мыши у которых генетически низкий ИФР-1, так как у них нокаутировали ген, кодирующий рецепторы гормона роста GHRKO (они прожили на 30% дольше мышей дикого типа). Зелёная линия - это те же мышки с нокаутом гена, кодирующего рецепторы гормона роста GHRKO, но которых недокармливали - им недокармливание уже не давало преимуществ, так как ИФР-1 у них был и так уже снижен генетически.
Нокаут у мышей гена, кодирующего рецепторы гормона роста GHRKO (выборочное удаление рецепторов гормона роста) продлевает жизнь трансгенным мышам примерно на 30% в сравнении с мышами дикого типа. На графике слева: чёрный цвет линии - это мыши дикого типа. График синего цвета - это мыши дикого типа, которых недокармливали, чтобы снижать у них ИФР-1 (они прожили на 30% дольше мышей дикого типа). Красная линия - это мыши у которых генетически низкий ИФР-1, так как у них нокаутировали ген, кодирующий рецепторы гормона роста GHRKO (они прожили на 30% дольше мышей дикого типа). Зелёная линия - это те же мышки с нокаутом гена, кодирующего рецепторы гормона роста GHRKO, но которых недокармливали - им недокармливание уже не давало преимуществ, так как ИФР-1 у них был и так уже снижен генетически.
Что это нам даёт? А то, что если людям генетически снизить ИФР-1 до оптимального, то им не нужно голодать периодически, чтобы продлить сильно жизнь.
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/27688483
- www.ncbi.nlm.nih.gov/pubmed/27732088
 Интересно, что именно с подобной (но немного другой) генной инженерией была создана мышь, которая установила рекорд по продолжительности жизни. Это мышь с необычным именем GHR-KO 11C, созданная Анджеем Бартке (Andrzej Bartke) — эндокринологом из Медицинской Школы Университета Южного Иллинойса, расположенной в Спрингфилде (США). Его мышь не дожила всего 6 дней до своего пятилетия, прожив 1819 дней. Этот рекорд удалось достичь, отключив у грызуна ген-рецептор гормона роста, что позволило у неё сильно снизить ИФР-1. 25 сентября 2003 года Анджей Бартке получил Longevity Prize - приз за долголетие созданной им мыши
Интересно, что именно с подобной (но немного другой) генной инженерией была создана мышь, которая установила рекорд по продолжительности жизни. Это мышь с необычным именем GHR-KO 11C, созданная Анджеем Бартке (Andrzej Bartke) — эндокринологом из Медицинской Школы Университета Южного Иллинойса, расположенной в Спрингфилде (США). Его мышь не дожила всего 6 дней до своего пятилетия, прожив 1819 дней. Этот рекорд удалось достичь, отключив у грызуна ген-рецептор гормона роста, что позволило у неё сильно снизить ИФР-1. 25 сентября 2003 года Анджей Бартке получил Longevity Prize - приз за долголетие созданной им мыши
Полезно знать, что немного имитировать эффект оптимизации ИФР-1 может лекарство от сахарного диабета метформин в дозировке 500 мг в сутки.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/27654259
Вывод: в будущем нокаут гена, кодирующего рецепторы гормона роста GHRKO (выборочное удаление рецепторов гормона роста), либо нарушение в работе генах, кодирующих рецепторы ИФР-1 с помощью генной терапии сможет продлить нашу жизнь лет на 5-17, в зависимости от возраста вмешательства. А сегодня мы можем получить подобный эффект с помощью голоданий, либо с помощью диеты FMD. Но для этого нужно всю жизнь соблюдать диету, что по силам далеко не каждому. Кроме того, немного имитировать данный эффект оптимизации ИФР-1 может препарат для лечения сахарного диабета 2-го типа метформин в дозировке 500 мг в сутки.
Генетическая сверхэкспрессия FGF21 (фактора роста фибробластов 21) заметно увеличивает продолжительность жизни у трансгенных мышей в сравнении с мышами дикого типа, не снижая потребления пищи
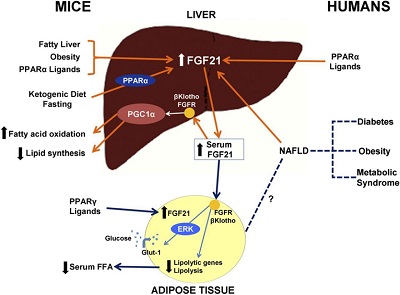 Фактор роста фибробластов-21 (FGF21) – это гормон, секретируемый печенью в периоды голодания для того, чтобы помочь организму адаптироваться к недостатку питательных веществ. FGF21 также синтезируется печенью в ответ на сахарный диабет и многие другие проблемы со здоровьем и даже при употреблении алкоголя. FGF21 блокирует рецепторы гормона роста из-за чего снижается синтез ИФР-1 печенью. А более низкий, чем обычно ИФР-1 во многих исследованиях сильно продлевал жизнь животным и снижал смертность у людей. И было бы интересно проверить, можно ли просто генетически заставить организм секретировать больше FGF21. И продлит ли это значительно жизнь. Как оказалось - можно. Кстати, немного имитировать эффект повышения FGF21 может лекарство от сахарного диабета метформин в дозировке 500 мг в сутки.
Фактор роста фибробластов-21 (FGF21) – это гормон, секретируемый печенью в периоды голодания для того, чтобы помочь организму адаптироваться к недостатку питательных веществ. FGF21 также синтезируется печенью в ответ на сахарный диабет и многие другие проблемы со здоровьем и даже при употреблении алкоголя. FGF21 блокирует рецепторы гормона роста из-за чего снижается синтез ИФР-1 печенью. А более низкий, чем обычно ИФР-1 во многих исследованиях сильно продлевал жизнь животным и снижал смертность у людей. И было бы интересно проверить, можно ли просто генетически заставить организм секретировать больше FGF21. И продлит ли это значительно жизнь. Как оказалось - можно. Кстати, немного имитировать эффект повышения FGF21 может лекарство от сахарного диабета метформин в дозировке 500 мг в сутки.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/24041694
Генетическая сверхэкспрессия FGF21 (фактора роста фибробластов 21) заметно увеличивает продолжительность жизни трансгенных мышей (на графике красная линия) в сравнении с мышами дикого типа (на графике синяя линия), не снижая потребление пищи
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/23066506
Вывод: В будущем генетическая сверхэкспрессия FGF21 (фактора роста фибробластов 21) может заметно увеличить нашу продолжительность жизни без снижения потребления пищи. Немного имитировать эффект повышения FGF21 может лекарство от сахарного диабета метформин в дозировке 500 мг в сутки.
Генетический нокаут Аденилат циклазы 5-го типа продлевает жизнь трансгенным мышам на 30% в сравнении с мышами дикого типа
 ОК. До этого мы видели, как можно с помощью генетической терапии имитировать эпизодические голодания и сильно продлевать жизнь. Но оказывается есть и другой способ добиться тех же эффектов, но уже не имитируя снижение ИФР-1 до оптимального с помощью коротких циков голода, а снижая воздействие гормонов стресса на наш организм. Хороший способ повысить стрессоустойчивость организма – это блокировать передачу сигнала от гормона стресса - адреналина в клетку. Сегодня это можно делать с помощью лекарства пропранолол. Также ингибирует AC5 литий. Оба этих лекарства являются потенциальными геропротекторами (веществами, продлевающими жизнь).
ОК. До этого мы видели, как можно с помощью генетической терапии имитировать эпизодические голодания и сильно продлевать жизнь. Но оказывается есть и другой способ добиться тех же эффектов, но уже не имитируя снижение ИФР-1 до оптимального с помощью коротких циков голода, а снижая воздействие гормонов стресса на наш организм. Хороший способ повысить стрессоустойчивость организма – это блокировать передачу сигнала от гормона стресса - адреналина в клетку. Сегодня это можно делать с помощью лекарства пропранолол. Также ингибирует AC5 литий. Оба этих лекарства являются потенциальными геропротекторами (веществами, продлевающими жизнь).
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/18205980
- www.ncbi.nlm.nih.gov/pubmed/19922557
Кстати. Совмещать генетическую блокаду рецепторов гормона роста и Аденилатциклазу 5-го типа (АС5) нельзя. Мыши в таком эксперименте умерли уже через месяц, будто голодали. Этим мышам заблокировали АС5 и сократили рацион питания по калорийности. Поэтому либо голодать, либо полностью заблокировать АС5. Либо голодать и снизить излишнюю активность АС5, но не блокировать её полностью.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pmc/articles/PMC3727099/
 Адреналин – гормон, который вызывает реакцию бей-беги («flight or fight»); он начинает активно выделяться при ощущении опасности, страхе, травмах, ожогах, шоке и в пограничных ситуациях, мобилизуя организм для устранения угрозы. При этом адреналин очень мощный стресс гормон, при длительном воздействии он повреждает клетки и целые ткани, приводя к истощению организма, разрушает сердце. Американский исследователь Stephen F. Vatner с коллегами создал трансгенных мышей с «выключенным» геном аденилатциклазы 5 типа (AC5) – молекулы, необходимой для передачи адреналинового сигнала в клетки через один из типов его рецепторов – β-адренорецепторы. Важно отметить, что такие рецепторы присутствуют почти на всех клетках организма.
Адреналин – гормон, который вызывает реакцию бей-беги («flight or fight»); он начинает активно выделяться при ощущении опасности, страхе, травмах, ожогах, шоке и в пограничных ситуациях, мобилизуя организм для устранения угрозы. При этом адреналин очень мощный стресс гормон, при длительном воздействии он повреждает клетки и целые ткани, приводя к истощению организма, разрушает сердце. Американский исследователь Stephen F. Vatner с коллегами создал трансгенных мышей с «выключенным» геном аденилатциклазы 5 типа (AC5) – молекулы, необходимой для передачи адреналинового сигнала в клетки через один из типов его рецепторов – β-адренорецепторы. Важно отметить, что такие рецепторы присутствуют почти на всех клетках организма.
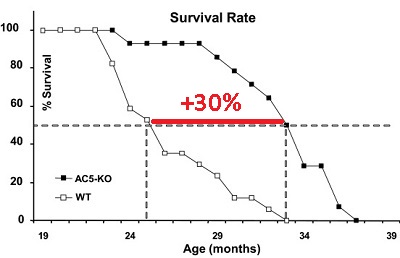 Посмотрите на графике. Нокаут АС5 сильно продлевал медианную продолжительность жизни трансгенным мышам - на 30% по сравнению с мышами дикого типа, защищал сердце от старения, защищал от диабета 2-го типа и ожирения. На молекулярном уровне эти эффекты были связаны с тем, что инактивация AC5 запускала путь стрессоустойчивости - Raf/MEK/ERK. В результате клетка вырабатывала целый набор защитных молекул, запускала механизмы выживания клеток. Кроме того, из более ранних работ известно, что действие адреналина на клетку через β2 -адренорецепторы непосредственно вызывает повреждения ДНК. Таким образом, можно предположить, что «выключение» гена AC5 мышей способствовала еще и повышенной стабильности генома.
Посмотрите на графике. Нокаут АС5 сильно продлевал медианную продолжительность жизни трансгенным мышам - на 30% по сравнению с мышами дикого типа, защищал сердце от старения, защищал от диабета 2-го типа и ожирения. На молекулярном уровне эти эффекты были связаны с тем, что инактивация AC5 запускала путь стрессоустойчивости - Raf/MEK/ERK. В результате клетка вырабатывала целый набор защитных молекул, запускала механизмы выживания клеток. Кроме того, из более ранних работ известно, что действие адреналина на клетку через β2 -адренорецепторы непосредственно вызывает повреждения ДНК. Таким образом, можно предположить, что «выключение» гена AC5 мышей способствовала еще и повышенной стабильности генома.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pmc/articles/PMC3727099
Интересно, что подавление или блокада AC5 у мышей защищает от многих видов рака, в том числе от меланомы. Сегодня даже FDA в США одобрила противовирусный препарат аденин-9-β-д-арабинофуранозид (Vidarabine или AraAde), который специфически блокирует АС5 и может быть полезным для лечения меланомы и рака лёгких. Таким образом, ингибирование АС5 - это новый механизм для профилактики раковых заболеваний, связанных со старением.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/23957304
Есть также свидетельства, которые показывают, что блокада АС5 лекарством пропранолол заблокировала развитие атеросклероза у обезьян и продлевала жизнь людям.
 То, что эмоциональный стресс повышает давление и вызывает болезни сердца — наглядно показано в работе Дж. Каплана. Каплан на примере приматов показал, что если собрать группу самцов приматов, то в течение скольких-то дней у обезьян появится социальная иерархия. Самое худшее место в такой иерархии — это внизу. Самцы приматов, находящиеся в подчиненном положении, демонстрируют ряд показателей хронического стресса. Часто у таких приматов появляется атеросклероз. Но если учёные давали самцам приматов, находящимся внизу социальной иерархии (группа риска), бета-блокатор пропранолол, подавляющий активность симпатической нервной системы, то у них не развивался атеросклероз сосудов. Это показало, как симпатическая нервная система из-за стресса негативно влияет на развитие атеросклероза и участвует в проблемах с сердцем и сосудами. Правда в том, что эмоциональный стресс реализует себя через симпатическую (адренергическую) автономную нервную систему, которая связывает управляющие центры нашего мозга и внутренние органы. В том числе — с иммунными, костным мозгом и др. А атеросклероз — главный фактор, который приводит к наибольшему число смертей в развитых странах от инфаркта сердца и инсульта мозга.
То, что эмоциональный стресс повышает давление и вызывает болезни сердца — наглядно показано в работе Дж. Каплана. Каплан на примере приматов показал, что если собрать группу самцов приматов, то в течение скольких-то дней у обезьян появится социальная иерархия. Самое худшее место в такой иерархии — это внизу. Самцы приматов, находящиеся в подчиненном положении, демонстрируют ряд показателей хронического стресса. Часто у таких приматов появляется атеросклероз. Но если учёные давали самцам приматов, находящимся внизу социальной иерархии (группа риска), бета-блокатор пропранолол, подавляющий активность симпатической нервной системы, то у них не развивался атеросклероз сосудов. Это показало, как симпатическая нервная система из-за стресса негативно влияет на развитие атеросклероза и участвует в проблемах с сердцем и сосудами. Правда в том, что эмоциональный стресс реализует себя через симпатическую (адренергическую) автономную нервную систему, которая связывает управляющие центры нашего мозга и внутренние органы. В том числе — с иммунными, костным мозгом и др. А атеросклероз — главный фактор, который приводит к наибольшему число смертей в развитых странах от инфаркта сердца и инсульта мозга.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/2899392
Клинические испытания на людях показали, что пропранолол снижает смертность от сердечно-сосудистых заболеваний (причина смертности №1 в мире),
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/6342840
3-х летнее наблюдение пациентов 60-69 лет, которые перенесли инфаркт миокарда, показало, что пропранолол снижал у таких пациентов общую смертность на 35-37%. Кроме того, пропранолол вызывал уменьшение признаков болезни и старения сердца (значительно большее увеличение фракции выброса левого желудочка и значительно большее снижение массы миокарда левого желудочка).
Ссылки на исследование:
- www.ncbi.nlm.nih.gov/pubmed/9230162
- www.ncbi.nlm.nih.gov/pubmed/6342843
Вывод: в будущем мы можем делать генетический нокаут, либо снижение эффективности работы Аденилат циклазы 5-го типа с помощью генной терапии и сильно продлевать себе жизнь. Но и сегодня мы можем добиваться этого же эффекта медикаментозно, если действовать очень аккуратно под наблюдением врача с помощью лекарства пропранолол, который блокирует именно все бета адренергические рецепторы, а не некоторые, как это делают селективные бета-адреноблокаторы. Немного блокировать АС5 (до 50%) может и литий.
Удаление RIP3 (рецептор взаимодействия серин/треонин-протеинкиназы 3) продлевает жизнь атеросклеротических мышей на 30% - до уровня здоровых мышей дикого типа.
Систематическое воспаление способствует развитию многих заболеваний, включая сердечно-сосудистые заболевания, которые являются ведущей причиной смертности во всем мире. Интересно, что если в сосудах подавить воспаление, то даже у мышей с высоким холестерином (с плохой генетикой в отношении атеросклероза) атеросклероз не развивается, и мыши живут также долго, как и мыши дикого типа. Речь идёт о мышах с "Арое−/−" - экстремальной моделью атеросклероза. Арое - аполипопротеин Е. У таких мышей очень быстро повышается холестерин в крови (особенно ЛПНП) и развивается атеросклероз. Казалось бы, что если не снизить холестерин, то их не спасти. Но как оказалось, если подавить воспаление, то эти мыши могут не болеть атеросклерозом даже при высоком холестерине в крови.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pmc/articles/PMC4066890
- https://en.wikipedia.org/wiki/Apolipoprotein_E
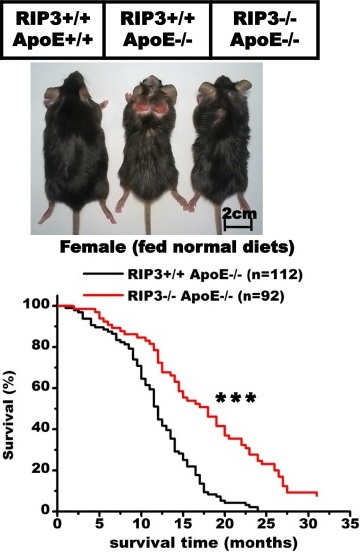 У людей также бывает плохая генетика по Apoe и высокий уровень холестерина. И данные настоящего исследования могут очень помочь нам отменить ускоренное старение при такой генетике, иметь здоровое сердца и сосуды. Видите, на картинке, когда у мышек ApoE +/+ - нет дефицита ApoE, то всё ок. Они выглядят здоровыми. Когда у мышек ApoE -/-, то они выглядят больными. Но когда при ApoE -/- генетически удалить RIP3 (RIP3-/-), то воспаление в сосудах снижается, и мышки опять выглядят здоровыми и живут также долго, как и мышки с ApoE +/+ даже с по прежнему высоким уровнем холестерина в крови.
У людей также бывает плохая генетика по Apoe и высокий уровень холестерина. И данные настоящего исследования могут очень помочь нам отменить ускоренное старение при такой генетике, иметь здоровое сердца и сосуды. Видите, на картинке, когда у мышек ApoE +/+ - нет дефицита ApoE, то всё ок. Они выглядят здоровыми. Когда у мышек ApoE -/-, то они выглядят больными. Но когда при ApoE -/- генетически удалить RIP3 (RIP3-/-), то воспаление в сосудах снижается, и мышки опять выглядят здоровыми и живут также долго, как и мышки с ApoE +/+ даже с по прежнему высоким уровнем холестерина в крови.
На графике также видно, что мышки с дефицитов ApoE -/- имели сильное воспаление в сосудах из-за RIP3 +/+ и жили не более 25 месяцев. Но стоили удалить им RIP3 (RIP3 -/-), то такие мышки уже жили 32 месяца - до уровня продолжительности жизни мышей дикого типа.
Механизм такой. RIP3 при высоком холестерине в крови стимулируют некроз в сосудах с выделением цитокинов, которые мобилизуют моноциты из костного мозга в участки поражения с последующим их превращением в макрофаги и т. д. - образуются холестериновые бляшки, а в анализах крови повышается фактор некроза опухоли ФНО. Но удаление RIP3 подавляет некроз и снимает воспаление в атеросклеротических бляшках сосудов, не снижая при этом уровень холестерина и триглицеридов в крови, а в анализах падает фактор некроза опухоли ФНО. Когда 50% мышек с ApoE -/- и RIP3 +/+ уже погибли от атеросклероза, то мышки с ApoE -/- и RIP3 -/- были ещё живы на 88% подобно мышкам дикого типа. RIP3 повышает воспаление через NF-κb, повышает апоптоз (самоуничтожение тканей организма). Важно: у RIP3 +/+ есть и полезная функция. RIP3 вызывает апоптоз (самоуничтожение) для защиты против вирусной инфекции.
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pmc/articles/PMC4568286/figure/fig04
- www.ncbi.nlm.nih.gov/pubmed/20210786
- http://sci-hub.cc/10.1042/CS20090488
- http://genesdev.cshlp.org/content/27/15/1640.full
Из предыдущих данных читатель может сделать вывод, что после нокаута RIP3 хоть и не будет развиваться атеросклероз, но будет опасность цитомегаловируса. Ведь RIP3 вызывает апоптоз (самоуничтожение) для защиты против вирусной инфекции. Цитомегаловирус человека (ЦМВ) — это основной вирус, вызывающий врожденные дефекты и серьезные проблемы у лиц с ослабленным иммунитетом. ЦМВ также связан с атеросклерозом (поражение сосудов). Предыдущие исследования показали, что индукция mTOR независимой аутофагии может заблокировать репликацию различных ДНК и РНК вирусов. Активация mTOR независимой аутофагии с помощью трегалозы может быть ещё одним методом лечения ЦМВ. Трегалоза - это сахар, который может войти в наш постоянный рацион вместо сахара, так как является потенциальным геропротектором (средством, продлевающим жизнь).
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/26559848
- www.ncbi.nlm.nih.gov/pubmed/18340111
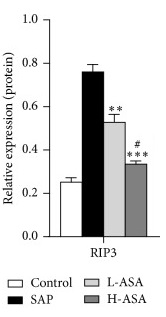 По традиции давайте посмотрим, а можно ли задавить RIP3 доступными нам сегодня средствами. Оказывается, можно. Так низкие дозы аспирина (L-ASA) хоть и не снижают через RIP3 некроз до уровня здоровых мышей (control), но снижают некроз хотя бы частично по сравнению с SAP. Смотрите на графике. У здоровых мышей уровень некроза был чуть больше 0,2. У мышей больных атеросклерозом - почти 0,8. А при малых дозах аспирина - 0,3 (немного больше, чем у здоровых).
По традиции давайте посмотрим, а можно ли задавить RIP3 доступными нам сегодня средствами. Оказывается, можно. Так низкие дозы аспирина (L-ASA) хоть и не снижают через RIP3 некроз до уровня здоровых мышей (control), но снижают некроз хотя бы частично по сравнению с SAP. Смотрите на графике. У здоровых мышей уровень некроза был чуть больше 0,2. У мышей больных атеросклерозом - почти 0,8. А при малых дозах аспирина - 0,3 (немного больше, чем у здоровых).
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pmc/articles/PMC5227127/figure/fig6
- www.ncbi.nlm.nih.gov/pubmed/28119929
Значит ли это, что аспирин способен замедлять развитие атеросклероза, подавляя воспаление в сосудах? И вот в исследованиях на людях было показано, что низкие дозы аспирина замедляют прогресс атеросклеротического поражения сосудов, подавляя воспаление сосудов и повышая стабильность атеросклеротической бляшки.
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/16326168
- www.ncbi.nlm.nih.gov/pubmed/12208806
- www.ncbi.nlm.nih.gov/pubmed/26843277
- www.ncbi.nlm.nih.gov/pubmed/25824964
В отличии от аспирина полностью ингибирует RIP3 Некросулфонамид (necrosulfonamide)
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/22265413
Вывод: в будущем мы можем делать генетический нокаут RIP3 и продлевать жизнь людей с высоким холестерином в крови, дополнительно стимулируя противовирусную защиту, употребляя в пищу вместо сахара трегалозу. А сегодня, если повышен холестерин, и в анализах крови выявляется повышенный фактор некроза опухоли ФНО, то можно для профилактики некроза и воспаления в сосудах подавлять RIP3 с помощью лекарств: аспирина 250 мг 1 раз в два дня и других.
Редактирование гена PCSK9 у взрослых мышей, склонных к высокому уровню холестерина в крови и атеросклерозу с помощью всего одной интервенции снизило уровень плохого холестерина ЛПНП на всю жизнь, лишив необходимости снижать холестерин с помощью статинов.
Сердечно-сосудистые заболевания является убийцей номер один во всем мире. В предыдущей главе мы видели, как сильно сокращает жизнь повышенный холестерин в крови, если не подавить воспаление в сосудах. В июне 2014 года учёные смогли отредактировать гены в >50% клеток печени взрослой мыши – с помощью аденовируса с Cas9/CRISPR. Удалось внести изменения в ген PCSK9 с помощью одной интервенции. Люди с такими изменениями в этом гене имеют меньший уровень плохого холестерина и меньше болеют сердечно-сосудистыми заболеваниями. Таким образом было показано, что всего лишь одной инъекцией можно снизить уровень плохого холестерина и в будущем обходиться без лекарств для снижения уровня холестерина - статинов.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/24916110
Генетическая сверхэкспрессия Klotho увеличивает продолжительность жизни у трансгенных мышей на 19-30% в сравнении с мышами дикого типа.
20 лет назад, в 1997 году японские и американские ученые во главе с Yo-ichi Nabeshima обнаружили новый ген долголетия и дали ему название в честь греческой богини судьбы, плетущей нить жизни - Klotho. Его «выключение» у трансгенных мышей вызывало синдром ускоренного старения. А еще через 7 лет те же исследователи выяснили, что и активация klotho значительно продлевает мышам жизнь – самцам на 20-30%, а самкам – до 19%.
Вырабатывается klotho в почках и сосудах мозга и разносится кровью по организму, как гормон. Он системно воздействует на большинство клеток в организме – связывается с рецепторами на их поверхности и подавляет сигналинг инсулина и ИФР-1 (один из главных путей старения). Уже через 3 года после открытия гена klotho – в 2000 году – была проведена первая работа по генной терапии, правда, не от старения, а от хронического заболевания сосудов – атеросклероза. Ryozo Nagai с коллегами системно ввел этот ген крысам и добился улучшения состояния сосудов и снижения артериального давления.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/11027545
А в 2014 году было показано, что определенные варианты в гене klotho (SNP Rs9536314) ассоциированы с долголетием и высокими умственными способностями у людей.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/24813892
 Чтобы понимать, как на нас влияет Klotho, рассмотрим исследования, которые показали, что мутагенные мыши, у которых ген Klotho был с дефектом, выглядели нормальными примерно в течение 3-4 недель жизни, а затем начинали стремительно стареть. За месяц у них обнаруживались такие яркие признаки старения: атрофия кожи, остеопороз, атеросклероз и эмфизема. Приблизительно через два месяца мыши умирали.
Чтобы понимать, как на нас влияет Klotho, рассмотрим исследования, которые показали, что мутагенные мыши, у которых ген Klotho был с дефектом, выглядели нормальными примерно в течение 3-4 недель жизни, а затем начинали стремительно стареть. За месяц у них обнаруживались такие яркие признаки старения: атрофия кожи, остеопороз, атеросклероз и эмфизема. Приблизительно через два месяца мыши умирали.
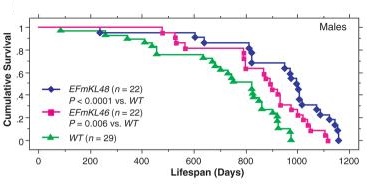 В других исследованиях ученые вывели второй тип мутагенных мышей, у которых ген Klotho вырабатывает существенно больше белка, чем у обычных мышей. Эти мышки жили на 19% — 30% дольше своих обычных сородичей (см. график слева). Учёные отмечают, что Klotho представляет собой тот редчайший случай в биологии млекопитающих, когда один-единственный ген столь существенным образом влияет на продолжительность жизни. Сверхэкспрессия белка klotho вызывает сопротивление инсулина к ИФР-1, имитируя снижение ИФР-1 до оптимального с помощью коротких циков голода
В других исследованиях ученые вывели второй тип мутагенных мышей, у которых ген Klotho вырабатывает существенно больше белка, чем у обычных мышей. Эти мышки жили на 19% — 30% дольше своих обычных сородичей (см. график слева). Учёные отмечают, что Klotho представляет собой тот редчайший случай в биологии млекопитающих, когда один-единственный ген столь существенным образом влияет на продолжительность жизни. Сверхэкспрессия белка klotho вызывает сопротивление инсулина к ИФР-1, имитируя снижение ИФР-1 до оптимального с помощью коротких циков голода
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/16123266
Уровень белка klotho естественным образом снижается по мере старения организма, что ведет к ухудшению познавательных способностей. Повышение экспрессии белка klotho, ассоциировано с лучшими познавательными функциями у нормальных здоровых людей.
Ссылка на исследование:
- http://onlinelibrary.wiley.com/doi/10.1002/acn3.161/abstract
- www.ucsf.edu/news/2015/01/122761/brain-region-vulnerable-aging-larger-those-longevity-gene-variant
Пока у нас нет возможности с помощью генной инженерии повысить уровень klotho в организме, мы можем это сделать с помощью лекарств. Рандомизированные контролируемые испытания на людях в возрасте около 60 лет показали, что лечение валсартаном или лозартаном (лекарства от высокого артериального давления) увеличивает экспрессию белка долголетия klotho.
Ссылки на основной источник:
- www.ncbi.nlm.nih.gov/pubmed/23929932
Также активированный уголь увеличивает экспрессию белка долголетия klotho у крыс.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/19955715
Вывод: в будущем мы сможем с помощью генной инженерии повышать экспрессию Klotho и продлевать жизнь от 5 до 17 лет - в зависимости от возраста вмешательства и пола. А сегодня некоторые лекарства от артериального давления (валсартан и лозартан) доказано у людей повышают klotho, а также повышает klotho, по крайней мере у грызунов, использование активированного угля.
Генетический нокаут рецепторов конечных продуктов гликирования RAGE может потенциально продлить жизнь примерно также, как и снижение ИФР-1 до оптимального с помощью коротких циков голода и сокращение калорий. А сокращение калорий с потреблением высокого количества конечных продуктов гликирования не позволяет продлевать жизнь мышей.
Накопление конечных продуктов гликирования — одна из причин старения человека, а также многих возраст зависимых заболеваний: атеросклероз, инфаркт миокарда, застойная сердечная недостаточность, диабетическая ретинопатия, диабетическая нейропатия, диабетическая нефропатия, болезнь Альцгеймера, псориаз. RAGE — это рецепторы, которые связывают конечные продукты гликирования.
Ссылка на источник:
- https://en.wikipedia.org/wiki/RAGE_(receptor)
 У птиц нет RAGEs, и возможно поэтому они имеют большую продолжительность жизни при более высокой температуре тела и уровня глюкозы в крови. Птицы не болеют сахарным диабетом в нормальных условиях. Кроме того, в плазме птиц содержится более низкая концентрация метилглиоксаля.
У птиц нет RAGEs, и возможно поэтому они имеют большую продолжительность жизни при более высокой температуре тела и уровня глюкозы в крови. Птицы не болеют сахарным диабетом в нормальных условиях. Кроме того, в плазме птиц содержится более низкая концентрация метилглиоксаля.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/24684667
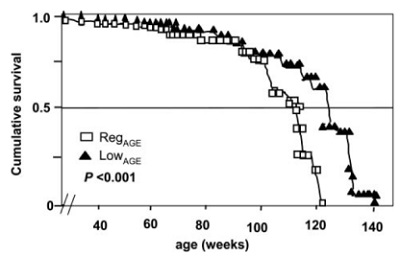 В исследованиях на мышах было показано, что диета с сокращением у мышей одного из самых распространённых конечных продуктов гликирования (карбокси-метил-лизин) с возраста около 30 недель (с юношества по меркам людей) была достаточна, чтобы значительно увеличить среднюю и максимальную продолжительность жизни животных (на 15% и 6% соответственно). На следующем графике показано, что мыши с сокращением в рационе питания конечных продуктов гликирования жили значительно дольше. Кроме того, у мышей с низким уровнем конечных продуктов гликирования в рационе питания удалось значительно снизить вес тела. Это показывает, что лишний вес — это не только следствие калорий в пище, но и следствие высокого потребления конечных продуктов гликирования.
В исследованиях на мышах было показано, что диета с сокращением у мышей одного из самых распространённых конечных продуктов гликирования (карбокси-метил-лизин) с возраста около 30 недель (с юношества по меркам людей) была достаточна, чтобы значительно увеличить среднюю и максимальную продолжительность жизни животных (на 15% и 6% соответственно). На следующем графике показано, что мыши с сокращением в рационе питания конечных продуктов гликирования жили значительно дольше. Кроме того, у мышей с низким уровнем конечных продуктов гликирования в рационе питания удалось значительно снизить вес тела. Это показывает, что лишний вес — это не только следствие калорий в пище, но и следствие высокого потребления конечных продуктов гликирования.
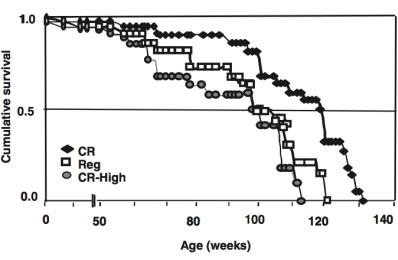
Однако, как показано на следующем графике, если в оптимально-калорийном питании у мышей обеспечить столько же конечных продуктов гликирования, сколько при обычном питании, то продления жизни не наблюдается (см. график слева)
Ссылка на исследование:
- _https://michaellustgarten.wordpress.com/2014/07/25/advanced-glycation-end-products-theres-more-to-health-than-counting-calories-protein-fat-and-carbs
Но ведь можно и не сокращать конечные продукты гликирования, а просто нокаутировать с помощью генной инженерии рецепторы RAGE. Генетическая блокада рецепторов RAGE у мышей уже не раз проводилась исследователями и приводила к положительным последствиям для здоровья мышей. Но вот, как это будет влиять на продление жизни мышей видимо не проверялось. Но потенциал у этого большой.
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/27236646
- www.ncbi.nlm.nih.gov/pubmed/27109771
 В переводе на наш рацион - это будет выглядеть так. Если сократить калории, но при этом кушать жареную, запечённую пищу и много сладостей и мучного, никакого преимущества для здоровья не будет. В то же время, если даже не сокращать калории в питании, но полностью исключить из рациона жареное, печёное, мясо кушать только в варёном виде, а овощи только в сыром, не есть сладости и продукты с высоким Гликемическим Индексом, добавить средства ингибиторы конечных продуктов гликирования (метформин 500 мг в сутки, витамин Б6 5-20 мг в сутки, сырую капусту брокколи 60-100 грамм в сутки), то возможно увеличить продолжительность жизни. А такое лекарство, как Телмисартан снижает способность RAGE к связыванию конечных продуктов гликирования у гипертоников.
В переводе на наш рацион - это будет выглядеть так. Если сократить калории, но при этом кушать жареную, запечённую пищу и много сладостей и мучного, никакого преимущества для здоровья не будет. В то же время, если даже не сокращать калории в питании, но полностью исключить из рациона жареное, печёное, мясо кушать только в варёном виде, а овощи только в сыром, не есть сладости и продукты с высоким Гликемическим Индексом, добавить средства ингибиторы конечных продуктов гликирования (метформин 500 мг в сутки, витамин Б6 5-20 мг в сутки, сырую капусту брокколи 60-100 грамм в сутки), то возможно увеличить продолжительность жизни. А такое лекарство, как Телмисартан снижает способность RAGE к связыванию конечных продуктов гликирования у гипертоников.
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/18473846
- www.ncbi.nlm.nih.gov/pubmed/14502106
- www.ncbi.nlm.nih.gov/pubmed/25933243
- www.ncbi.nlm.nih.gov/pubmed/15905958
Но лучший путь, если его эффективность подтвердится окончательно в исследованиях - это нокаутировать RAGE с помощью генной инженерии или генной терапии и кушать себе вкусную жареную пищу и не только.
Генетическая сверхэкспрессия BubR1 защищает ДНК, увеличивает максимальную продолжительность жизни трансгенных мышей на 15% и значительно снижает частоту раковых опухолей даже при наличии мутаций ДНК
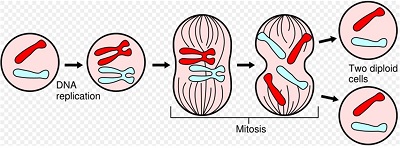 Исследователи обнаружили, что протеин под названием BubR1 снижает риск онкологических заболеваний и на 15% продлевает максимальную продолжительность жизнь подопытных мышей. Протеин BubR1 помогает клеткам формировать хромосомы в процессе деления. Когда экспрессия BubR1 снижается, хромосомы не могут правильно разделиться во время митоза, и формируются клетки с дефектными хромосомами. Пока протеин BubR1 изучен лишь поверхностно, но ученые знают, что большинство раковых клеток образуются именно из-за дефектных хромосом, вернее их разного количества. Это явление называют анеуплоидия, и оно является общим для всех раковых клеток, хотя доподлинно неизвестно, является ли анеуплоидия главной причиной онкозаболеваний.
Исследователи обнаружили, что протеин под названием BubR1 снижает риск онкологических заболеваний и на 15% продлевает максимальную продолжительность жизнь подопытных мышей. Протеин BubR1 помогает клеткам формировать хромосомы в процессе деления. Когда экспрессия BubR1 снижается, хромосомы не могут правильно разделиться во время митоза, и формируются клетки с дефектными хромосомами. Пока протеин BubR1 изучен лишь поверхностно, но ученые знают, что большинство раковых клеток образуются именно из-за дефектных хромосом, вернее их разного количества. Это явление называют анеуплоидия, и оно является общим для всех раковых клеток, хотя доподлинно неизвестно, является ли анеуплоидия главной причиной онкозаболеваний.
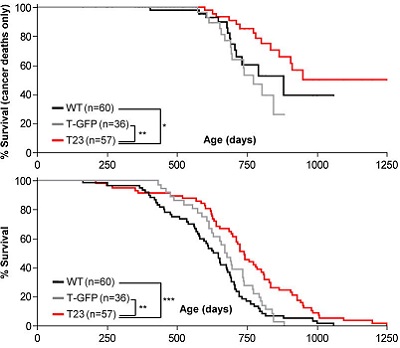
Как бы то ни было, анеуплоидные клетки имеют слишком мало или слишком много хромосом, и протеин BubR1 играет в этом явлении ключевую роль. В ходе экспериментов, американские ученые из клиники Майо в Рочестере, штат Миннесота, вывели с помощью генной инженерии трансгенных мышей (Т23) с повышенной экспрессией BubR1. Затем подвергали подопытных мышей воздействию веществ, необратимо вызывающих опухоли легких и кожи. В результате выяснилось, что онкологические заболевания «заработали» лишь 33% трансгенных мышей (Т23) с гиперэкспрессией BubR1. При этом заболевание у мышей с гипер-BubR1 наступало позже, чем у мышей дикого типа – примерно через 2 года, а смертность от рака была в разы ниже – 15% против 40% (см. первый график слева). Более того, продолжительность жизни грызунов выросла на 15% (см. второй график слева), а их физическая форма впечатлила даже ученых. Так, мыши пробегали по беговой дорожке 200 м, а не 100, как обычные мыши.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/23242215
Возможно, ван Дерсен и его коллеги сделали первый шаг к созданию новых методов лечения рака и способов задержать старение.
Интересно, что антибиотик доксициклин, который замечен, как мощный препарат для лечения некоторых видов рака, способен повышать экспрессию BubR1.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/16227576
Вывод: в будущем мы сможем с помощью генной инженерии повышать экспрессию BubR1 и продлевать жизнь лет на 10, а также задерживать развитие многих видов рака. А сегодня в клинических испытаниях проверяется для лечения некоторых видов рака антибиотик доксициклин, который является мощным ингибитором пролиферации раковых клеток у животных. И доксициклин, как раз является активатором BubR1
Генетическая сверхэкспрессия MTH1 увеличивает продолжительность жизни у трансгенных мышей на 22% в сравнении с мышами дикого типа.
Характерной чертой и, по-видимому, одной из основных причин старения является накопление мутаций ДНК. Кроме того, многочисленные болезни преждевременного старения – прогерии – тоже возникают в результате чрезмерного накопления геномных повреждений. В течение жизни ДНК постоянно повреждается разными воздействиями. Из внешней среды на нее действует температура, УФ-излучение, химические мутагены и вирусы. Но и внутренние процессы самой клетки увеличивают геномную нестабильность: ДНК повреждается активными формами кислорода из митохондрий, а системы репликации (удвоения ДНК) и ремонт ДНК часто работают неточно и сами вносят ошибки. В результате с возрастом в ДНК накапливается целый спектр нарушений: разрывы, точечные мутации, перемещение кусков ДНК с одного места на другое, слипание хромосом, встраивание в геном вирусов и транспозонов. Если повреждений слишком много, клетка вынуждена пойти по одному из 3х путей: запустить процессы клеточного самоубийства (апоптоза), стать сенесцентной или превратиться в раковую. Все эти процессы (в случае если им подвержено много клеток) чрезвычайно вредны для организма.
Наиболее изученный путь увеличения стабильности генома – это активация систем ремонта ДНК. Именно этот подход используют в большинстве работ по генной терапии.
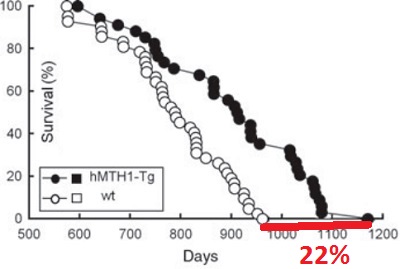 В 2013 году итальянские ученые под руководством Gemma Calamandre исследовали трансгенных мышей со сверх экспрессией гена MTH1. Белок MTH1 участвует в ремонте повреждений ДНК и РНК, вызываемых активными формами кислорода. Он исправляет дефектные нуклеотиды - окисленные по восьмому атому углерода гуанидины (из четырех букв, на которых написана ДНК эта обозначается «Г»). Оказалось, что повышенная экспрессия MTH1 продлевает жизнь трансгенных мышей до 22% (см. график слева). Кроме того, у таких мышей геномные повреждения с возрастом накапливались гораздо меньше. Изменялось и их поведение: мыши становились менее тревожными и более любопытными.
В 2013 году итальянские ученые под руководством Gemma Calamandre исследовали трансгенных мышей со сверх экспрессией гена MTH1. Белок MTH1 участвует в ремонте повреждений ДНК и РНК, вызываемых активными формами кислорода. Он исправляет дефектные нуклеотиды - окисленные по восьмому атому углерода гуанидины (из четырех букв, на которых написана ДНК эта обозначается «Г»). Оказалось, что повышенная экспрессия MTH1 продлевает жизнь трансгенных мышей до 22% (см. график слева). Кроме того, у таких мышей геномные повреждения с возрастом накапливались гораздо меньше. Изменялось и их поведение: мыши становились менее тревожными и более любопытными.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/23648059
Сегодня генная инженерия на людях для нас недоступна. Но мы немного можем повлиять на ремонт и защитить ДНК и повышать MTH1 с помощью магния. Лучший способ поддерживать необходимый уровень магния в крови - это добавки цитрата магния 300-400 мг элементарного магния в сутки.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/24929814
Магний важен для функционирования многих ферментов, вовлеченных в копирование и восстановление повреждений ДНК. Хронический дефицит магния в пище приводит к окислительному стрессу и накоплению повреждений ДНК.
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/18705541
- www.ncbi.nlm.nih.gov/pubmed/2472534
- www.ncbi.nlm.nih.gov/pubmed/11295157
- www.ncbi.nlm.nih.gov/pubmed/18448487
Также важно, что люди, имеющие самые высокие в пределах нормы уровни магния в плазме крови и самое высокое его потребление, умирали на 34% реже — то есть имели на 34% меньшую смертность от всех причин.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/24259558
Вывод: в будущем мы сможем с помощью генной инженерии или генной терапии повышать экспрессию MTH1 и продлевать жизнь на 6-12 лет, защищая ДНК от повреждений. А сегодня для частичного достижения того же эффекта мы можем употреблять цитрата магния 300-400 мг в виде добавок. Тем более, что магний показал и снижение смертности у людей на 34%.
Заключение:
Чтобы добиться более существенных результатов в генной терапии старения, необходимо комбинировать разные подходы. Есть множество подтверждений тому, что воздействие сразу на несколько путей долголетия дает больший эффект на продолжительность жизни, чем воздействие на них по-отдельности. Необычайный долгожитель – голый землекоп – грызун, который живет дольше мыши в 10 раз, отличается от нее активацией целого набора путей долголетия: это и повышенная устойчивость к стрессам, защита от рака, стабильность белковых молекул, защита от нейродегенерации и пр. Таким образом, для того чтобы разработать генную терапию, радикально продлевающую жизнь, необходимо действовать одновременно на многие пути долголетия. То есть комбинировать те подходы генной терапии, которые разрабатываются сейчас для увеличения стабильности генома, омоложения гипоталамуса, уничтожения сенесцентных клеток, увеличения устойчивости к стрессам, улучшения работы митохондрий, поддержания ниш стволовых клеток и пр. Но важно помнить, что не проверенные в исследованиях комбинации воздействия на по отдельности полезные механизмы могут и сократить жизнь!!!
Если сейчас терапия одним геном не приводит к увеличению продолжительности жизни более чем на 20-30%, то мы надеемся, что в будущем, за счет комплексной терапии старения, можно будет добиться поистине фантастических результатов.
В лабораториях в США, в лабораториях в Китае и Великобритании объявили о планах или текущих исследованиях о примении технологии редактирования генома crispr для человеческих эмбрионов. Правда пока эти попытки неудачны. Но всё начинается с проб и ошибок.
Ссылки на источники:
- www.technologyreview.com/s/535661/engineering-the-perfect-baby
- www.ncbi.nlm.nih.gov/pubmed/25894090
Выводы.
- Все подходы к генной терапии старения делятся на те, где в организм доставляется ген долголетия, и на те, где «выключается» ген или путь старения.
- В сравнении с другими подходами к продлению жизни генную терапию достаточно провести только один раз за всю жизнь.
- Внедрение гена теломеразы (TERT), нарушение работы гена Agtr1a, нокаут GHRKO, нарушение в генах, кодирующих рецепторы к ИФР-1, сверхэкспрессия FGF21, нокаут AC5, удаление RIP3, редактирование гена PCSK9, сверхэкспрессия Klotho, нокаут RAGE, сверхэкспрессия BubR1, сверхэкспрессия MTH1 - всё это примеры самых эффективных способов генной инженерии или генной терапии, позволяющих продлевать жизнь.
- Чтобы добиться более существенных результатов в генной терапии старения и в генной инженерии против старения, необходимо комбинировать разные подходы.
- Сегодня частично повторить эффекты генотерапии можно с помощью лекарств и добавок: цитрат магния, доксициклин, метформин, витамин Б6, капуста брокколи,телмисартан, валсартан + флувастатина, снижение ИФР-1 до оптимального с помощью коротких циков голода, диета FMD, пропранолол, литий, трегалоза,аспирин, активированный уголь.
Благодарю Дениса Варванца, Володю Милованова и Александра Фединцева, благодаря которым написаны некоторые материалы из данной статьи.
Предлагаем Вам оформить почтовую подписку на самые новые и актуальные новости, которые появляются в науке, а также новости нашей научно-просветительской группы, чтобы ничего не упустить.
Уважаемые читатели ресурса www.nestarenie.ru. Если Вы думаете, что статьи настоящего ресурса полезны для Вас, и желаете, чтобы этой информацией могли пользоваться и другие люди многие годы, то имеет возможность помочь в развитии этого сайта, потратив на это около 2-х минут Вашего времени. Для этого кликните по этой ссылке.
Рекомендуем ещё почитать следующие статьи:
- Метформин - самое изученное лекарство, которое может продлевать жизнь.
- Подробная программа продления жизни научно доказанными способами.
- Витамин K2 (МК-7) сокращает смертность
- Витамин B6+магний снижают смертность на 34%
- Глюкозамин Сульфат эффективно продлевает жизнь и защищает от многих видов рака
- Фолаты для предупреждения раннего старения
- Как победить метилглиоксаль — вещество, которое нас старит.
Обязательно оставляйте свои комментарии под статьей, которую Вы читаете. Это очень важно для нас.
Предлагаем Вам оформить почтовую подписку на самые новые и актуальные новости, которые появляются в науке, а также новости нашей научно-просветительской группы, чтобы ничего не упустить. Обязательно оставляйте свои комментарии под статьей, которую вычитаете. Это очень важно для нас.

Автор статьи
Веремеенко Дмитрий Евгеньевич
Телефон:
Почта:
Сфера деятельности - data science в медицине
Основатель проекта, изучающего терапии, направленные на увеличение продолжительности жизни человека (nestarenie.ru/slb-expert_.html)
Со-основатель IT сервиса продления жизни
Основатель форума о продлении жизни Nestarenie Camp (nestarenie.ru/camp.html)
Со-автор книги "Бонусные годы" (nestarenie.ru/kniga-3.html)
Создатель справочного блога о старении человека (nestarenie.ru)
Социальные сети:
- Карта Viza (доллары): 4215 8901 1587 0138 для переводов за пределами РФ
- Карта МИР в Сбере (рубли): 2202 2032 1501 6686 (МАЙЯВИ Ч.) - на территории РФ
Свежие комментарии
Подпишитесь на свежие статьи
Предлагаем Вам оформить почтовую подписку на самые новые и актуальные новости, которые появляются в науке, а также новости нашей научно-просветительской группы, чтобы ничего не упустить.
95 комментариев
Здравствуйте, Дмитрий. Вы пишете, что низкокалорийное питание не продевает жизнь. Но в рекомендациях к лечению нейродегенеративных заболеваний мозга врачи советуют питаться именно низкокалорийными продуктами, где животные жиры исключаются???
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Вам придется выбрать, чему доверять, врачам, либо исследованиям. Мои друзья врачи неврологи не рекомендуют
Добрый день, что делать если обнаружен вариант полиморфизма, предрасполагающий к развитию тромбоза?
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
ничего
он скорее всего не работает
Прекрасный сайт и очень интересные ,науные обследования!
Дмитрий, добрый день! Статья безусловно очень интересная, но она была вами написана в середине 2017 года, а сейчас конец 2019. Что изменилось за это время? В своих более поздних статьях по внеклеточному матриксу вы говорите, что никакое омоложение клеток (а значит, и никакая генная терапия) не даст длительного эффекта если не устранить старение матрикса – значит ли это, что все перечисленные тут методы даже при одновременном их применении будут на человеке почти бесполезными? Или нет? Я бы сделал все перечисленные генетические вмешательства на себе – думаю, лет через пять у меня появится такая возможность – скажите, в свете современных представлений о внеклеточном матриксе имеет ли это смысл?
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Все, что в этой статье не позволяет прожить больше 110-120 лет
Спасибо, Дмитрий! Поясните пожалуйста ещё такой момент – является ли старение матрикса первичным, а старение клеток – зависимым вторичным процессом? Или всё несколько сложнее, и хотя старение матрикса имеет ведущую роль в общем процессе старения организма, но старение клеток само по себе так же может ускорять старение матрикса? Этот момент критично важен для понимания ситуации, поскольку если верно второе (т.е. если замедлив старение клеток мы замедлим и старение матрикса тоже), то применение генной терапии в более раннем возрасте даст более сильный эффект, чем в более позднем. Ну а если старение клеток на старение матрикса не влияет, то раннее начало генетической терапии не так критично. Ваше мнение?
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Старение клеток почти не влияет на старение матрикса
Дмитрий, у меня низкие: инсулин <2, с- пептид=0,7, видимо, генетически обусловлены. Как следствие, глюкоза, гликированный гемоглобин у верхней границы нормы . Аутоимунный процесс исключен. Мне 50 лет, ИМТ-17.3, ИФР-1 – 180. В чем негативное влияние немного повышенного сахара в крови при том , что инсулин низкий?
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Гликирование
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Часто пишут в СМИ, что сейчас в науке нет способов продлевать жизнь, есть только способы ее не сократить. Это ИМХО в корне не верно.
Нужно четко определять, что такое Максимальная Продолжительность Жизни человека (около 120 лет). И что такое Ожидаемая Продолжительность Жизни.
Так у моего знакомого Ожидаемая Продолжительность Жизни была 40 лет. Он умер от инсульта. А если бы перестал вести плохой образ жизни и начал бы лечить свои болезни, то ожидаемая продолжительность жизни могла бы быть и 70 и 80 – кто знает.
Другое дело, что он никак не мог бы конечно прожить больше 120.
Ну тогда так и нужно говорить, что сегодня в науке нет способов продлить Максимальную Продолжительность Жизни в 120 лет. Иначе люди то понимают, что теперь можно жить как хочешь.
Кто-то возразит. “Но ведь просто веди здоровый образ жизни, не сокращай себе жизнь курением, и гиподинамией и живи дольше – просто не сокращай”. Тут я тоже возражу. У Вас может быть, например, генетически другие циркадные ритмы. В итоге вы имеете синдром задержки фазы сна. Как бы вы не старались вести здоровый образ жизни, вы проживете меньше, чем если начнете ложиться спать позже и вставать позже, поменяв свою работу. Либо начнете применять светотерапию и мелатонин и перепрограммируете свои циркадные ритмы. Тогда вы сможете прожить дольше. И здоровый образ жизни тут не причем. Тут речь идет о генетической особенности, которую нужно диагностировать и с ней считаться. Другая ситуация. У Вас могут быть наследственные проблемы с усвоением витамина б12 в ЖКТ. И какой образ жизни вы бы не вели, он у Вас будет в дефиците. Это сократит Вашу жизнь. Заметьте – вы сами свою жизнь не сокращаете. Это от Вас не зависит. Вы можете даже вести здоровый образ жизни. Но Вам это не поможет.
Учитывая все выше сказанное, считаю верным говорить, что сегодня в науке существуют разные способы продлить свою ожидаемую продолжительность жизни. Для каждого человека они индивидуальны.
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Часто пишут в СМИ, что сокращения калорий в одних исследованиях продлевали жизнь мышам, а в других нет. И чаще нет. А где-то даже сокращали.
Вот тут важный момент.
1. Важно чтобы сокращение калорий не сократило их слишком сильно. Вообще правильно говорить оптимизация калорий, так как некоторым из нас не мешало бы наоборот употреблять больше пищи – слишком худым.
2. Многие исследования проводились с целью понять за счет каких механизмов сокращения калорий у мышей продлевали жизнь. А для этого выполняется, например, нокаут каких-то генов, чтобы получить эффект сокращения калорий без сокращения. Так мышам, например, нокаутировали ген, кодирующий рецепторы гормона роста. В итоге у этих мышей уже стал низкий ИФР-1. И снижение ИФР-1 с помощью сокращения калорий для этих мышей уже не продлевал жизнь дополнительно ncbi.nlm.nih.gov/pubmed/27688483 Другой пример, мышам нокаутировали ген, кодирующий Аденилатциклазу 5-го типа (АС5), а еще и посадили их на низкокалорийное питание. В итоге эти мыши умерли через 2 месяца, так как такое ограничение калорий практически задублировалось, а мыши были истощены.
3. “Низкокалорийное питание” жизнь не продлевает. Видимо в будущем ученые должны будут менять в своих исследованиях эту формулировку на “оптимизация калорийности питания”. Сокращение калорий – это лишь инструмент профилактики инсулинорезистентности у людей. И если человек и так имеет хорошую чувствительность к инсулину и уже и так стройный и не толстый, но ему сокращение калорий в питании только повредит и может сократить жизнь. И наоборот. Нужно оптимизировать калорийность питания, а не слепо сокращать.
Дмитрий, а есть ли смысл переживать о пассивном цитомегаловирусе в раннем возрасте (до 40 лет)? У меня повышенный IGG (но не IGM).
Два раза тестиировал. Индекс igg 2,2 и 2,7 был. Норма меньше <0,9. Я в свое время даже принимал Valganciclovir (Valcyte) несколько месяцев, но он почему-то не снизил CMV IGG.
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
А Вы его уже никогда не выгоните. Следите, чтобы он не повышал воспаление и спал
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Внедрение в клинику редактирования генома in vivo для лечения генетических заболеваний человека требует тщательных доклинических исследований на соответствующих моделях животных для оценки безопасности и эффективности. Перспективным подходом к лечению гиперхолестеринемии является инактивация секретируемого белка PCSK9, антагониста рецептора LDL. Однократные введения шести приматам аденоассоциированного вирусного вектора, экспрессирующего спроектированную мегануклеазу, нацеленную на PCSK9, приводят к дозозависимому разрушению PCSK9 в печени, а также к стабильному снижению циркулирующего PCSK9 и холестерина в сыворотке. Животные испытывали переходные, бессимптомные повышения сывороточных трансаминаз из-за образования Т-клеток против трансгенного продукта. Экспрессия векторной ДНК и мегануклеазы быстро снижалась, оставляя устойчивые популяции гепатоцитов с модифицированным геномом. Мегануклеаза второго поколения, специфичная для PCSK9 , показала снижение немишенных надрезов. Эти исследования демонстрируют эффективное, физиологически релевантное редактирование in vivo у приматов, и подчеркивают соображения безопасности для клинического внедрения.
Жене 29 лет. Вы, кстати, не ответили на мой вопрос… Если не сложно – может ли это быть какой-то генетический момент? Если конечно вам известно что-нибудь про это? Если не сложно поясните – у ашкеназских евреев, у которых есть мутации, – у них ИФР-1 низкий? Или он высокий но есть дефект рецепторов? Про вегетерианство -я понял. Это логично. Но хотелось бы понять что это не генетика. Просто совсем не вяжется таккой уровень там с другими биомаркерами, состоянием человека…
Насчет APOE то что у вас E3/E4 – это кстати какой RSID посмотреть можно для этого? Мое мнение – что такая картина потому – что он сейчас как бы отключен или работает на малую силу. А вот с годами больше шансов что он включится. Ибо хватает случаев – когда и вес идеальный, а холестерин повышен – у моей тещи так. Худая, белка мало ела по жизни, по узи печени все норм – а холестерин повышен (я бы сказал шкалит). И ей 65 лет. Притом это все ближе к 60 годам случилось. Я о том – что еще не настали те условия чтобы этот APOE включился. И верно обратное – совсем не обязательно что он включится вообще за всю жизнь. Нужно чтобы какие то условия сложились.
Вот какие… в этом конечно вопрос и нужно ученым искать разгадку.
Моя логика из серии – что вот если есть в генах предрасположенность к дерматику/псориазу – как у меня – притом с полового созревания, то мне стоит или стресс получить или на кофе посидеть недели 2 – как будет обострение. Я делаю вывод – что эти “вредные” гены включаются и кофе например это сильнейший включатель какой-то группы генов. Это 100%. Опять же никто не знает какой именно конкретно. А вот другой человек – и стресс и кофе а ничего такого нет и потом – оказывается что и гены по этим делам нормальные.
То есть тут вопрос – когда и при каких условиях влючаются и отключаются определенные гены. Тут конечно и метилирование стоит во главе этого процесса и другие пока что не известные моменты для человека.
По поводу intergenic. если зайти в личный кабинет 23andme в tools – browse raw data и вбить туда rs4420638 то в столбце genes – будет написано intergenic. Но с другой стороны – если вбить этот SNP в google или даже открыть книгу Москалева, то будет написано что этот полиморфизм относится к гену APOE. (snpedia.com/index.php/Rs4420638)
То есть вопрос в том почему у меня rs4420638 относится не к гену а находится в межгенном пространстве, которое называется intergenic. Это плохо или хорошо? Почему так случилось? Ну просто я задал вопрос – с той надеждой что вы друг изучали этот вопрос.
eupedia.com/forum/threads/28480-Help-with-23andme-s-browse-raw-data – вот тут пару слов про это есть. Но я не понял почему так все равно…
Вот посмотрите у себя rs4420638 – что там в столбце genes ?
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Мне пока сложно комменировать этот момент. Я его как раз сейчас изучаю в генетике. тут много вопросов. Еще совсем недавно считалось, что межгенное пространство – это мусорные регионы ДНК. Они действительно не кодируют, но могут влиять на транскриптом.
Дмитрий, может что то прояснилось по теме intergenic ? Просто интересен ваш взгляд на это…
Дмтрий здравствуйте! Я с вами согласен, что многие вопросы по генетике и ее практическому применению пока не раскрыты. Я вот недавно получил результаты 23andme V5 (у них версия чипа поменялась). Но не суть. Суть в том, что есть такое понятие – как SNP панель метилирования. Она описывает один из главнейших циклов – цикл метилирования. Он на сегодня наверное изучен больше всего. По нему тьма работ и исследований написано. Как вы знаете, Дмитрий, именно слаженная работа цикла метилирования отвечает за включение/отключение генов у человека. Да и вообще метилирование имеет огромное число задач. И если у человека по каким то причинам истощаются метильные группы – то это плохо.
Тот же переворот гомоцистеина в метионин – это все цикл метилирования.
ncbi.nlm.nih.gov/pubmed/19144510
ncbi.nlm.nih.gov/pubmed/25449138
ncbi.nlm.nih.gov/pubmed/26149435
ncbi.nlm.nih.gov/pubmed/19967264
Вот допустим у меня там по результатам такой анализ:
RS731236: TT – это ген VDR (рецепторы к витамину D)
RS1801133: AG – это ген MTHFR
rs1801131: TT – это также MTHFR
RS4680: AG – это ген COMT
Смотрят отношение между собой RS1801133 (C677T- Variation) и RS4680 (V158M – Variation).
Именно MTHFR является ключевым в метаболизме фолата. О пользе которого вы писали в одной из статей на сайте. У меня допустим есть гетерозиготная мутация. Именно эта мутация ингибирует возможность организма производить из фолиевой кислоты метилтетрагидрофолат (L-5-MTHF) который так нужен в цикле метилирования. У меня допустим снижена эта возможность на 35%.
А мутация например RS731236: TT – это ген VDR говорит о том что у меня не работают рецепторы витамина D как следует и это значит что как бы я не был на солнце то у меня синтез его будет очень низок. Отсюда нужен прием как я понимаю в виде препарата. Да у меня кстати и из препарата медленно он растет в крови этот витамин D.
Я о чем это пишу. О том что есть вот такие полимофизмы, которые изучены с ног до головы. И которые как раз связаны с нашим продлением жизни не напрямую но опосредовано. И если допустим у человека есть вот такие мутации – то значит ему 100% не фолиевая кислота там а метилфолат. И здесь же кстати в этом цикле метилирования напрямую замешан витамин B12. Эти же мутации говорят о том что цианокобаламин мне не пойдет. А нужен только метилкобаламин.
Дмитрий а какие результаты у вас по этим SNP (просто интересно). И вообще что вы думаете по этому поводу что я написал.. Очень бы хотел от вас статьи по циклу метилирования и генов которые за это отвечает. Еще раз хочу заметить – что этот вопрос досконально изучен на сегодняшний день. Можете сами убедиться.
То есть понимаете – вот вы писали там про гоцистеин в одном из статей – о том что его важно снижать – но причина то вот может быть у многих (а эта мутация есть как я понял почти у 50% людей) – но по сути не хватает метилирования. Добавляешь метилфолат – и метилкобаламин и гомоцистеин снижается. И общее состояние должно приходить в норму – так как ты даешь организму того чего ему не хватает хронически. И это косвенно должно отражаться на продолжительности жизни через те же гомоцистеины и прочие биомаркеры.
Вот кстати вы писали – http://nestarenie.ru/uroven-gomocisteina-i-starenie-cheloveka.html – что
Существуют средства, позволяющие уже накопленный гомоцистеин превращать обратно в метионин. Это витамин B 12 и фолиевая кислота. Таким образом, 500 мкг витамина В12 отдельно от других витаминов (не в комплексах — в комплексах он совсем не усваивается) ежедневно на протяжении всей жизни позволяет эффективно предупреждать преждевременное старение человека из-за накопления гомоцистеина.
Но так как допустим у меня есть мутация то фолиевая и цианокоболамин – мне пить не то чтобы нельзя – но не желательно. Тот же цианокоболамин содержит молекулу цианида, которую организму нужно обезвредить. А сделать это ему накладно как и проводить детоксикацию других ядов – из за опять же сбоя в метилировании. Поэтому вот вы писали – http://nestarenie.ru/folatyi.html и http://nestarenie.ru/glutation-2.html – уже ближе к истине – но не раскрывалась основная причина которая как раз и приводит к постепенному недостаку активных форм B9 и B12.
Другими словами в http://nestarenie.ru/interpretator.html – неправильно ставить в рекомендации там пить цианокобаламин если есть сбой в метилировании. Все таки вот эти основные вещи с B12 и B9 уже изучены и надо писать на мой взгляд – если есть полиморфизмы такие то – то пить активные формы B12 а если все ок – то можно и цианокоболамин (почему бы и нет)
Еще раз хочу сказать – метилирование очень хорошо изучено. Я могу десятки если не сотни ссылок скинуть на исследования пары тройки полиморфизмов касающихся этого цикла, которые имеют прикладное практическое значение (тот же уровень гомоцистеина чего стоит). Чего стоит врач В США Amy Yasko – которая стояла первой у истоков изучения этого метилирования. Теперь к ней едут со всего мира за помощью.
nejm.org/doi/full/10.1056/NEJM200104123441517
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Юрий. Все не так.
Если у Вас нет мутации в MTHFR, то вы будете курсами применять метилтетрагидрофолат примерно по 400 мкг в сутки потому что он Вам необходим все равно.
Если у Вас есть мутации, то вы будете принимать все те же 400 мкг метилтетрагидрофолата и не больше, иначе у Вас может быть рак от его переизбытка.
Если у Вас нет мутации в RS731236, то загорать по любому вы не будете – риск меланомы и Вы будете пить витамин Д3 нормализуя его по результатам анализов.
Если у Вас есть мутация RS731236, то вы все равно будете пить витамин Д3 нормализуя его по результатам анализов.
Далее Вы пишите, что “Эти же мутации говорят о том что цианокобаламин мне не пойдет. А нужен только метилкобаламин.”
Нет – не так. Просто у Вас он конвертируется в метилкобаламин хуже – иначе Вы уже давно бы умерли.
В итоге если у Вас есть мутации замедляющая конвертацию цианокобаламина в метилкобаламин, то согласно нашим программам Вы все равно проколите цианокобаламин до определенного уровня – до 600 нг/мл. И он меньше, но все же будет конвертироваться в метилкобаламин. И если Вы доведете его до уровня 600 нг/мл, то, как показывают исследования, это гарантирует достаточный уровень и самого метикобаламина даже при мутации. А кроме того, согласно нашим алгоритмом Вы все равно будете употреблять метилкобаламин курсами, независимо есть у Вас такие мутации или нет.
Гомоцистеин вообще не нужно снижать и не нужно смотреть, так как он косвенный маркер скорости клубочковой фильтрации почек и уровня витамина Б12. И Если у Вас витамин Б12 в норме – не менее 600 нг/мл и СКФ в норме и вырегулярно курсами применяете 400 мкг метилтетрагидрофолата в сутки, то Вам нормализация гомоцистеина ничего не даст, так как он не является самостоятельным фактором риска (либо об этом пока неизвестно) и будет в норме почти всегда при этом – вот только нормы у него уже будут иными, так как до 7 – это косвенный маркер, а если Б12 и СКф в норме, то гомоцистеин вполне будет в норме и даже до 16.
Что касается изученности метилирования, то как раз оно крайне плохо изучено, и я этот вопрос очень долго и плотно изучаю. В том числе читаю и учебники по генетике и метилированию и слушал лекции Москалева, и читал самый полный секретный сборник по исследованиям в области метилироваия, которые мне любезно предоставил Алексей Москалев, но просил никому не показывать, так что он пока в секрете.
—
Вывод:
1. Сделаете Вы секвенирование генома или нет – это ничего не поменяет и тактика лечения будет все той же.
http://not-aging.com
Поэтому я и говорю, что генетический код ничего нового в наше лечение не добавит и по сути лишняя трата денег. Если Вы думаете мы специально упираемся. Да мы сами делали свой тест на ДНК. И сами много ищем и копаемся в полиморфизмах, но пока это просто гороскоп. Это никак не меняет нашу тактику лечения.
2. Про метилирование. Как раз про него ничего не известно особо. Известно только как оно возникает и как работает. Но как его отрегулировать кроме эпигенетического отката, пока никто не знает. И будете Вы принимать витамина Б12 больше, только заметилируете полезные гены, которые будут молчать. Будете Вы принимать витамина Б12 меньше, недометилируете молчащие вредные гены, которые начнут работать. И тут регуляторных механизмов никаких не существует пока.
Дмитрий спасибо за исчерпывающий ответ! Да я согласен с вами – что можно этим метилированием повключать “спящие” плохие гены если например переборщить. Но также можно и не включить хорошие если не дометилировать. И что сейчас нет возможности как то точечно и главное выверенно это делать – теми же какими нить препаратами. Но это наверняка будущее.
Насчет генетического анализа – я тоже копаюсь. Уже кучу сервисов поиспользовал платных и бесплатных для составления отчетов разных. И скажу так – многие вещи про меня. Допустим есть
Насчет B12 – у меня он 450 единиц (цианокоболамин по крови). Вы говорите что он должен быть 600 и выше. Дмитрий, вот тут вопрос. Что лучше уколы (по 500 мкг) или метилкоболамин (по 1 грамму). То есть колоться мне не охота… Другими словами будет ли равноценной замена уколами таблетками ввиде метилкоболамина?
И если мои мутации не влияют по вашим словам на форму фолата и на его количество – так может мне 400 мкг фолиевой кислоты? Зачем этот метилгидрофолат – если фермент все равно отработает на 65% и сделает метилтетрагидрофолата в % отношении столько и не иначе. Ну как я это все понимаю – чем больше в крови фолиевой кислоты – тем больше метилтетрагидрофолата будет сделано ферментом но с ограничением в 65%.
и кстати вот тут есть у вас норма по цианокоболамину.. Но ведь фолиевую кислоту тоже можно сдать по крови. Но сколько ее надо иметь в крови – я не нашел у вас на сайте… Нет таких нормальных исследований на эту тему?
И еще по анализам у меня серьезный затык в метаболизме B6 и меди (серьезней чем по B9 и B12). B6 – это гены ALPL и NBPF3 а медь – это SMIM1 и SELENBP1 и их определенные полиморфизмы (например rs4654748 (CT) по B6 витамину) и rs2769264 (AC) по меди. Верна ли и тут ваша логика по B9 о которой вы мне выше написали. Другими словами не улушчу ли я свое состояние добавив еще B6. По ощущениям скажу – что мне B6 и магний значительно помогают для организма. Но они как будто бы быстро истощаются… То есть надо постоянно принимать. Как будто бы магний в мочу выходит как раз из за того что B6 мало метаболизируется в кровь. Там же у B6 тоже активная форма есть витамина. А мы пьем в магний цитрате неактивную. Еще цинк в дозировке в минимальной 6 мг – значительно улучшает состояние здоровья, например, на корню снимая хронический тонзилит. Я еще конечно проверю свои биомаркеры о которых вы написали на сайте nestarenie на этом фоне. Но факт есть факт. Такое ощущение что цинк медь и B6 с магнием уходят в мочу. Я это подозревал давно – но тут уже и генетические маркеры тоже показывают такую вероятность.
И еще я с 20 лет лысею потихоньку. И как оказалось все до одного гены которые известны на сегодняшний день имеют полиморфизмы с гомозиготной мутацией (так показывают платные отчеты и бесплатные которые я заказывал по здоровью). Если интересно какие конкретно SNP смотрят – я могу скинуть. При этом отец начал лысеть с 50 лет а отец мамы – вообще наверное итого позже. А у меня вот так. Так что как итог скажу- безусловно работа с генами – это будущее и оно уже близко. И тут и зарыт весь секрет нашего состояния. Но никто не знает как эти гены между собой взаимодействуют. Наверное там не линейное взаимодействие. И как раз исскуственный интелект тут будет в помощь ученым. Которые как раз и поможет вскрыть эти взаимодействия. Но нужна огромная статистическая база на которой делать машинное обучение. И тогда можно будет многие вещи понимать. Я надеюсь ученые уже пошли поэтому пути. Видимо американцы как раз эту базу и собирают.
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
ВЫ ПИШИТЕ: “И скажу так — многие вещи про меня. ”
МОЙ ОТВЕТ: “Прям как в гороскопе? У меня в моем тесте ДНК тоже многие вещи про меня. Вот только я на них повлиять никак не могу. Генную терапию я себе сделать не имею возможности пока. Тем не менее все что в этом тесте про меня не дает мне никакой пользы, так как я и так все это предупреждаю образом жизни и ничего в моей тактике лечения это не меняет. А прием дополнительных препаратов может свести на ноль все мои усилия или даже сократить жизнь. Ди и все, что нужно определяется маркерами анализов крови, МРТ, УЗИ. И это гораздо более достоверно, и на это можно влиять и управлять этим. Для меня ДНК анализ пока бесполезная вещь – шуточная игрушка.”
ВЫ ПИШИТЕ: “Что лучше уколы (по 500 мкг) или метилкоболамин (по 1 грамму).”
МОЙ ОТВЕТ: “Уколы конечно. Не у всех метилкобаламин усваивается вообще. А уколы надежнее”
ВЫ ПИШИТЕ: “так может мне 400 мкг фолиевой кислоты? Зачем этот метилгидрофолат — если фермент все равно отработает на 65% и сделает метилтетрагидрофолата в % отношении столько и не иначе.”
МОЙ ОТВЕТ: “Фолиевая кислота накапливается. Она очень медленно конвертируется и может создавать большой запас, который вреден”
ВЫ ПИШИТЕ: “фолиевую кислоту тоже можно сдать по крови. Но сколько ее надо иметь в крови — я не нашел у вас на сайте”
МОЙ ОТВЕТ: “Анализ то есть, но сколько ее должно быть в крови – еще нужно выяснять. Пока данные противоречивые. Возможно и не нужно на анализ ориентироваться вообще.”
ВЫ ПИШИТЕ: “И еще по анализам у меня серьезный затык в метаболизме B6 и меди”
МОЙ ОТВЕТ: “Я бы на Вашем месте по меди вообще бы не беспокоился, так как именно при участи меди образуются конечные продукты гликирования из жиров. И по мне – так лучше ее будет дефицит некоторый. Так как я даже иногда встречал данные о легком дефиците меди в долгоживущих”
ВЫ ПИШИТЕ: “не улушчу ли я свое состояние добавив еще B6”
МОЙ ОТВЕТ: “Для этого не нужно было сдавать ДНК тест. Витамин Б6 и так, если нет противопоказаний, то нужно обязательно всем пить и он есть у всех в программах. Кроме того, если Вы будете на основании своей ДНК составлять коктейль из БАДов и лекарств, то только сократите жизнь. НЕ важно, что у Вас нехватает. У долго живущих животных много чего и часто нехватате. Например, у голого землекопа вообще почти отсутствует витамин Д. И это для него не слишком полезно, однако это замедляет его метаболизм и живут он все таки дольше в 7 раз. Тактика добавлять в свой рацион то, чего вроде как нехватает – ИМХО не верна. Так как а кто решил, что нехватате. Может это даже хорошо, что нехватает. Нет данных что при децифите меди резко сокращается жизнь мышей, нет данных что при дефиците витамина цинка и много еще чего резко сокращается жизнь мышей. Если данные есть, то это уже давно для профилактики добавлено в программу антистарения, либо в программу диагностики – например, витамин Б12.”
ВЫ ПИШИТЕ: “Там же у B6 тоже активная форма есть витамина. А мы пьем в магний цитрате неактивную.”
МОЙ ОТВЕТ: “Все формы витамина б6 активны. Но мы пьем самую активную – пиридоксаль”
ВЫ ПИШИТЕ: ” Еще цинк в дозировке в минимальной 6 мг — значительно улучшает состояние здоровья, например, на корню снимая хронический тонзилит.”
МОЙ ОТВЕТ: “Однако цинк легко может сократить жизнь и его дополнительный прием для продления жизни не доказан”
ВЫ ПИШИТЕ: “И еще я с 20 лет лысею потихоньку.”
МОЙ ОТВЕТ: “Лысеют мужчины из-за дегибротестостерона. Можно заблокировать тестостерон, но это вряд ли продлит жизнь. Лучше его не трогать. Просто сделайте себе пересадку волос. ”
ВЫ ПИШИТЕ: “Так что как итог скажу- безусловно работа с генами — это будущее и оно уже близко. ”
МОЙ ОТВЕТ: “У Вас может 1-2 гена способствовать повышению мочевой кислоты, а она в анализах будет даже сниженной. Я даже знаю человека, который имея такие полиморфизмы, тем не менее не измеряю мочевую кислоту начала себе ее снижать. В итоге у начался дефицит, когда он сдал анализы на мочевую кислоту. А ее дефицит сильно повышает смертность и риск Паркинсона. Он перестал снижать, а она все равно был внизу нормы, несмотря на гены. А это потому что свойства каких-то генов сегодня расшифровали, а львиной доли – нет. И может 2 гена быть за снижение мочевой кислоты и 100 против, о которых вы можете даже не знать. И только анализы покажут истинную результирующую картину. Есть даже исследования 2017 года, которые доказали, что диагностика оп ДНК коду бесполезна. У Вас даже может быть какой-то полиморфизм, а регуляторная РНК изменит генетическую информацию при транкрипции. В итоге в гене записано одно, а регуляторная РНК заставляет ген работать подругому. Это называется эпигенетика. И этого Вы не увидите на тесте ДНК”
Дмитрий спасибо за исчерпывающий ответ! Да я и не спорил с вами. Просто хотел узнать ваше мнение. Но с другом стороны есть же гены к которым и вы в статьях обращаетесь типа FOXO3, APOE и так дале – значит тут уже изучено – раз есть реальный результат воздействия на них.
По меди – возможно вы и правы. Просто в научных статьях пишут про то что если в организме недостаток меди, то аневризма обеспечена. Так как медь отвечает за эластичность сосудов очень сильно.
Я полностью согласен с вами, что недостаток чего-либо – это не обязательно плохо. И тут есть конечно логика – так как вот даже по наблюдениями – что все беды от избытка чего либо, а не от недостатка. В эту логику вписывается и похудение (таже диета FMD) (недостаток) – которое здорово омолаживает организма и включает правильные гены и выключает неправильные.
Насчет цинка – спорить не буду. Я лишь про ощущения своего организма говорил. Но он и экспрессию генов ускоряет и ИФР-1 поднимает (что вредно) – он как бы реально здоровье дает – но надолго ли:) И в куче ферментных реакциях учавствует – то есть делает все и сразу. Наверное цинк совершенно точно улучшит состояние и продлит жизнь если знать на 100% что его у тебя недостаток. А вот если давать тому у кого и так с ним ок – то тут явно и рак можно заработать. Как вы писали как то люди с высоким ИФР-1 имеют здоровье лучше в молодости, а потом рак. Может и тут так. Но качки глотают цинк – так как он ростит тестостерон и позволяет мышцы нарастить.
Дмитрий, еще вопрос. У моей жены повышен значительно ИФР-1. Все другие анализы идеальны (начиная от общего анализа крови, биохимии, кучи других гормонов) (даже не за что схватиться). а ИФР-1 – больше 300 единиц. Вес и ИМТ в абсолютной норме – 21.91 (ИМТ). Но интересно что она у меня относительно низкого роста – 157 см. А вот ИФР-1 такой огромный. И как бы и худеть ей некуда да и не получится (у нее всегда давление низкое по жизни (95-100 на 55-60) не больше. Если она не поест там то давление на 5 единиц снижается и все сил нет. Белок ест конечно – но не фанатично.
Вопрос – что это может быть? Какие анализы надо сдать чтобы понять – это функционально что то не так или это допустим какой то генетический дефект там рецепторов ИФР-1 к примеру. Может это быть генетический вариант (есть к примеру ген который кодирует рецепторы к ИФР-1 – IGF1R – это его смотреть? Я вот у себя его глянул – у меня нет к сожалению мутации ашкеназских евреев:))) и вообще там normal стоит везде. Но его ли смотреть? Или допустим надо еще сдать на сам гормон роста (она не сдавала, но по идее – он же тоже должен быть высокий) и уже отсюда плясать? Ну просто понять причину надо… У нее не так ситуация чтобы там FMD практиковать… Наверное причина в другом. и как раз тут о генетике вспомнили – как о варианте такой картины.
И второй вопрос по себе.
Я вот в книге Москаленко (дожить до 120 лет) прочитал про такой вариант rs2149954 (у меня CT) – и что он принадлежит гену EBP1. Или допустим там же в этой книге (да и в других источниках тоже так написано) вариант rs4420638 (у меня AA) принадлежит гену APOE. Так вот у меня эти варианты не EBP1 и не APOE – а intergenic.
Я почитал – это какое то межгенное пространство. Так вот вопрос – это плохо или хорошо? почему так вообще произошло? ОЧень-очень интересно – может просто вы изучали этот вопрос.
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Сколько лет Вашей жене? Если больше 65, то ИФР-1 не важен. Если меньше 65, то пусть практикует вегетарианство.
ВЫ ПИШИТЕ: “Но с другом стороны есть же гены к которым и вы в статьях обращаетесь типа FOXO3, APOE ”
МОЙ ОТВЕТ: “FOXO – это фактор транскрипции, который влияет на работу генов. Тем не менее он не всегда работает. АPOЕ у меня Е3/Е4 – это очень плохо для меня. Но я ничего не поменял, потому что это значит у меня должен быть плохой холестерин, но он у меня хороший. И я и так отслеживаю холестерин в анализах крови. Поэтому и этот ген для меня оказался бесполезным. НУ не знал бы я, что у меня Е3/Е4. Чтобы было иначе? Ничего. Я так же веду образ жизни, который предупреждает последствия такой генетики.
ВЫ ПИШИТЕ: “Или допустим там же в этой книге (да и в других источниках тоже так написано) вариант rs4420638 (у меня AA) принадлежит гену APOE. Так вот у меня эти варианты не EBP1 и не APOE — а intergenic.”
МОЙ ОТВЕТ: Не понял вопрос и проблему. Можете подробнее описать.
Дмитрий, за прошедшие почти четыре года выводы и информация по метилированию генов не дополнилась? По-прежнему ничего не понятно?
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Стало понятно, что это не имеет отношения к скорости старения. Метилированием управляет матрикс. И перепрограммировать клетки не возможно в организме. Также как невозможно вылечить человека от простуды, если он продолжает сидеть в ледяной воде. Матрикс напрямую через механорецепторы, актовые нити и интегралы активизирует факторы транскрипции, которые управляют метилированием.
Дмитрий, а какие еще есть известные генные анализы крови типа как наличие определенных BRCA1/2 мутаций у женщин и/или APOE расшифровка, которые можно 1 раз в жизни сдать и знать в какую группа риска какой-то болезни ты входишь ?
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Yrisk.ru тут все эти анализы
СПАСИБО! Yrisk.ru достаточно полно раскрыл часть вопроса, касаемую рака. Но относительно не раковых болезней (типа как APOE ген) – пока вопрос не раскрыт до конца.
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Относительно остальных генов – знать есть они или нет не имеет никакой практической ценности? Я узнал, что у меня есть плохой АПОЕ. Что это изменило? ДА ничего. Я и так в рамках программы дел все для предупреждения. А вот если я узнаю, что у меня редкая мутация раковая из теста Yrisk.ru, то программ изменится сильно с акцентов на антирак и более частые аппаратные обследования в более раннем возрасте
Дмитрий, Вы конечно же правы частично правы по поводу мнения о генах типа АПОЕ (относящихся к другим “не раковым” вероятностям) – но отчасти. Пока не уверен насколько эта часть правоты превосходит 50%, но как минимум на 1% превосходит – т.е. Вы больше правы чем не правы с таким мнением и особенно аргументом к нему. У меня же цель докопать вопрос до конца, если будет случайно встречаться информация и дадите знать об этом каким-то образом в виде случайной оговорки в каком-нибудь Вашем ответе – спасибо.
Кстати, ели АПОЕ расстроил Вас по БА, возможно порадует по гиперлипопротеинемии.
Дмитрий, а что вы думаете о работах Яманаки и возможностях эпигенетического отката? Проводятся какие-то исследования в этой области?
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Воопервых в опытах не было эпигенетического омоложения — то есть не было отката старения вспять. И ничто еще не обращало старение вспять ИМХО. Во вторых — зпигенетический откат не может сильно продлить жизнь сам по себе и не продлевал в исследованиях, потому что мутации ДНК и ошибки не дают этого сделать у долгоживущих мышей. Скажем так долгоживущим мышам никакое эпигенетическое вмешательство не продлевало жизнь больше, чем диетическое вмешательство, связанное с различными изменениями в ИФР-1. Поэтому я считаю эти факты неверными. Вмешательства в FGF-21, в ИФР-1, в АС5 и другие продлевали куда больше. Мышам с нокаутом генов кодирующих рецепторы гормона роста мы ничем не можем продлить жизнь (Сигнальный путь HR/IGF-1) – в том числе и факторы Яманаки не помогут. А люди, которые прожили больше 100 лет — это как раз и есть люди с мутациями чаще всего в HR/IGF-1 сигнальном пути. И таким людям ни воздействие на HR/IGF-1 жизнь не продлит уже ни эпигенетический откат тоже жизнь не продлит. Сегодня рекорд продления жизни на мышах принадлежит именно мышке с нокаутом генов, кодирующих рецепторы гормона роста. Так, что про эпигенетику – это очень спекулятивно.
А как же опыты Бельмонте? У мышей наблюдалось снижение всех критических маркеров старения, а также снижалась продукция митохондриальных активных форм кислорода и удлинялись теломеры.
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
НЕ всех маркеров, а только тех, что измеряли в исследовании. И если бы там было омоложение, то почему же мыши умерли. И там было продление жизни прогерейных мышей, которые живут всего 5 месяцев на 40%, тогда как таким мышам низкокалорийное питание продлевает жизнь в 2-3 раза. Кроме того сами теломеры вызывают рак из-за повышения мутагенеза в ДНК
Да, возможно, но когда он спрашивает врачей об этом, то они как правило говорят: генетика такая…
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Пока уровень науки не может с помощью генетического кода достоверно определить ваши проблемы.
1-2 гена, которые наука может знать, могут способствовать заболеванию, а 10-50 генов, которые наука может не знать, может защищать от заболевания. Результат такого компота мы видим по биомаркерам старения. Но определять это по генетическому коду, пока что, больше напоминает гороскоп.
Дмитрий, я уже как-то писала, что у моего племянника низкий ИМТ- 18-18,5. Сейчас ему 29 лет. Вес если и удается немного набрать, то он быстро уходит.
Пытался есть гейнер, заниматься в спорт зале, повышал калорийность, но пока все тщетно. Недавно он сдал генетический тест в Генотеке.
Результат очень насмешил- ВЫСОКИЙ РИСК ОЖИРЕНИЯ- 40% при 9% среднем риске. Скоро предстоит консультация с генетиком по скайпу. О каких мутациях в генах можно еще спросить, из известных вам? Как они правильно называются?
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Люба. Генетика не ответит Вам на Ваши вопросы. Из огромного количества генов только малая часть известно как работает. Поэтому я уже много раз говорил, что генетический тест не даст никакой практической информации, а смотреть нужно по биомаркерам.
Добрый день, Дмитрий!
Отличный сайт у Вас, много интересной и полезной информации.
Хотелось бы узнать, как влияет регулярная сдача крови (донорство) на старение?
Спасибо за ответ!
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Если у Вас высокий ферритин – выше 80, то хорошо.
Если у Вас ферритин ниже 50, то плохо
Спасибо.Теперь только в лимонной буду все растворять.А вы какую воду пьёте? Я например только дисстелят.
На счет магния.Ацетат или сульфат магния сильно уступают цитату или самое главное соблюдать количество элементарного магния.Спасибо за ответ.
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Дело именно в самом веществе ЦИТРАТ. Оно обладает геропротекторными свойствами
Дело в том, что цитраты это все го лишь минеральные соли лимонной кислоты.Если геропротекторы только цитраты в отличии от других солей например таких как сульфаты, ацетаты,нитриты и т.д, получается дело в самой лимонной кислоте,вообще при экспериментах на усвоение цитраты минералов усваивались лучше всех,но ацетат уступал цитратам незначительно скажем на 0,5%.В случаи перерасчета массовой доли элементов все выравнивалось.А не в лимонной кислоте ли дело? Ваше мнение?
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Не понял Вашего вопроса.
Нам нужен цитрат вместе с магнием, которые показывали во многих клинических испытаниях многие геропротекторные свойства, обусловленные свойствами и магния и самого цитрата. Наприме мочевая кислота – маркер старения. При её повышенном уровне развиваются сахарный диабет, гипертония, камни в почках, падагра, деменция. И уровень мочевой кислоты растёт с возрастом. Цитрат вместе с магнием в виде магния цитрата доказано в клинических испытаниях блокируют камнеобразование, развите падагры и т.д, что не могут другие формы магния, даже более биодоступные. Так как сам цитрат снижает мочевую кислоту и даже употребление большого количества лимонного сока без сахара снижает мочевую кислоту. Сам магний тоже геропротектор. И вместе они показывают мощные эффекты. И если вы употребляете другие биодоступные формы магния, то вам придётся ещё и лимонную кислоту употреблять. Но будет ли это такде работать – нужно проверять. Часто очевидные сочетания в клинике не подтверждаются. Я предпочитаю проверенные в испытаниях способы
Теперь понятно.Я сам делаю себе ацетат цинка, магния и т.д.В уксусе оксиды металлов лучше растворяются чем в лимонной кислоте.Лимонная кислота или лимон? В лимоне фруктоза есть все таки? Предпочтительнее что по вашему?
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Лимонная кислота
Дмитрий,Вы как-то писали, что паразиты модулируют иммунитет у человека и с некоторыми не надо бороться. Какие могут быть полезны?
Здравствуйте Дмитрий, наткнулся на статью о паразите который отключает программу стараения у тихоокеанского лосося, продливая тем самым жизнь в несколько раз. Существуют ли еще в природе подобные примеры? Прочитать можно здесь arctic-plus.com/nauka/280-dolgozhitel-parazit-prodlevayushhij-zhizn-xozyaina
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Программа старения бывает у животных, которые умирают сразу после размножения, либо немного позже. У человека такой программы нет
Дмитрий,в статье написано ” А сегодня некоторые лекарства от артериального давления (валсартан и лозартан) доказано у людей повышают klotho, а также повышает klotho, по крайней мере у грызунов, использование активированного угля.”
А в статье именно про телмисартан тоже указано повышение klotho . Вопрос : для повышения klotho лучше лозартан или телмисартан или телмисартан не эффективен ?
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
все.
Дмитрий, сообщение написали с ее страницы КрисТина ,если не сложно проверьте пожалуйста сообщения.
Добрыий день Дмитрий ! Помогите пожалуйста разобраться .Моей дочке 20 лет ,сдали генетический тест Атлас сказали обсудить со спартивным врачом тему спорта . Мы будем очень благодарны вам!Cейчас принимает Фолаты ,Магний Б6 ,Вит Д+Вит К ,Вит Б12( в таб по анализу у нее 312 )В Facebook я написала вам пароль .Еще раз Спасибо!
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Пароля на фейсбуке у меня нет.
А разве по генетическому тесту можно решать вопросы по спорту – сомневаюсь.
А что у дочки не так – напишите
Что этот дедок такой энергичный, то это может и не из-за маточного молочка. Вопрос в другом: маточное молочко и гтрутневый гомогенат в плане продления жизни (т.е. в долгосрочной перспективе) не навредят? А то 70 с хвостиком это еще не показатель долголетия.
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
По маточному молочку в исследованиях нет данных по продлению жизни.
Один знакомый дедок очень расхваливает трутневый гомогенат и маточное молочко (из маточного молочка делают препарат апилак). Ему уже за 70, а бегает как молодой. Даже потенцией хвастает. Я конечно со свечкой не стоял, но судя по его энергии у гомогената и маточного молочка есть какието положительные свойства.
Дмитрий, а как они влияют на продолжительность жизни? Возможно есть и какие нибудь подводные камни.
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
То что он бегает – не значит, что это изза маточного молочка
Получается во время FMD и голоданий нельзя принимать Пропланолол и Литий,т.к совмещать генетическую блокаду рецепторов гормона роста и Аденилатциклазу 5-го типа (АС5) нельзя ?
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Да. Я пил. Жив.
А что означают красные и синии линии на этой картинке?
http://nestarenie.ru/wp-content/uploads/2017/05/dd2-44.jpg
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Синие – это колебания случаев. Красная – это средняя
Спасибо, Дмитрий, очень полезная статья. Пожалуйста, подскажите дозировку телмисартана. Видела микардис 0.08 и 0.04.
“1 раз в полгода комбинацией препаратов валсартана 20 мг + флувастатина 10-20 мг, либо телмисартан + аторвастатин 10 мг.” Спасибо.
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
телмисартан 10 мг – если нет повышенного давления.
Дмитрий! Ваш труд бесценен!!!!
Дмитрий! Огромное спасибо Вам за труд и интереснейшие статьи и огромный труд! Ни от одного врача не узнаешь то , что узнаешь из Ваших публикаций!!!! Вам нам сам Бог послал!!!!
Нет в русском языке названия страны “Ашкеназия” 🙂
“Ашкеназ” – семитское название средневековой германии, “ашкеназы” – субэтнос евреев, сформировавшийся в Центральной Европе (и ныне ашкеназы составляют большую часть (около 80 %) евреев мира).
“у евреев долгожителей Ашкеназии” лучше всего написать как “у долгожителей евреев-ашкеназов”, думаю.
Как горский-еврей, согласен с написанным
Тут очень перспективны исследования в области факторов Яманаки и их использования на практике, чем например ныне занимается группа Бельмонте. Хотя такое обратное омоложение к стволовой клетке с торможением его в нужном месте – дело наверное минимум 20-30 лет будущих исследований, тема очень интересная. Хотя такой технологией наверное будет пользоваться только круг суперэлиты, поживём увидим, что будет, а для этого нужно уже сейчас как можно медленнее стареть с помощью уже открытых методов.
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Факторы Яманки ничем не лучше остальных способов. Старение может победить только генотерапия с ремонтом днк по образцу.
Яйцеклетка же побеждает своё старение при оплодотворении, скидывает все накопившееся и обнуляет возраст, иначе дети бы уже пожилыми рождались бы. И всё это происходит без ремонта ДНК по образцу.
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Она не побеждает. Иначе бы дети от братьев и сестёр не были бы опасными.
Дети от братьев и сестёр и даже от самого себя – прекрасно существуют в природе и рождаются молодыми в отличие от давшей им начало пожилой яйцеклетки (инбридинг, гермафродитизм), но в этом случае у них хуже приспособляемость к изменяющейся окружающей среде и теряются преимущества полового размножения.
А то, что мутации при таком случае лучше укореняются – так это следствие не приобретённых мутаций, а изначально при рождении уже существующих, т.е. возраст тут уже не причём, например брат и сестра в течение жизни накапливают разные мутации, но при их скрещивании опасны для потомства именно те одинаковые мутации, которые были даны им обоим при рождении.
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
У них мутаций, а изначально при рождении уже существующих потому что они после рождения были не единым организмом. А вы единый организм. И в течении жизни у Вас накапливаются мутации. Чтобы и перекрыть – нужен другой организм у которого этих же мутаций нет. Ваши клетки сливаются в одну. Мутации буд-то “латаются” ВОт пример примитивный. М – мутация. 1 нормальный ген.
Вот человек №1 11111111111111111M1111111111111M1111111111111M1111111111111111111
Вот человек №2 1111111M11111111111111M111111111111111M1111111111M111111111111111
Видите – у них мутации в разном месте. И они скрещиваясь получают признаки от мамы и папы.
Нет совпадения мутаций в одном и том же месте.
На выходе получим 111111111111111111111111111111111111111111111111111111111111111111 – это очень грубо и образно.
А если на выходе получим нежизнеспособный организм, то он просто не вырастет до зрелого возраста и не даст потомства.
————–
В будущем будет создан идеальная ДНК. И будет терапия, которая будет исправлять мутации в Вашем ДНК в соответствии с этой идеальной ДНК.
————–
Иначе никак. Стволовые клетки хоть медленнее, но всё равно стареют и накапливают мутации. И половые клетки накапливают, но очень медленно в отличии от Ваших
С мутациями не всё однозначно, они тоже нужны для приспосабливаемости к изменениям окружающей среды, да, большая часть мутаций как бы вредны, но вообще без них тоже нельзя, иначе – тупик.
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Жизнь нашу ограничивают мутации. Если бы они не накапливались – мы бы не старели, либо старение могли бы лечить легко
жар .. ну это дмитрий написал одна идеальная днк .. практичней конечно несколько оптимальных для различных условий и не останавливаясь продолжать создавать улучшения и варианты
Тут всё же интересно потеоретизировать, возьмём для упрощения животных гермафродитов, с их бесполым размножением, они в течение жизни накапливают мутации и тоже с помощью какой то части из этих мутаций приспосабливаются к изменениям окружающей среды и передают их своим детям – клонам, хотя уже не совсем клонам так как возникшие мутации тоже передаются.
Так вот при зачатии их яйцеклетки таки сбрасывают накопленный возраст, иначе рождались бы пожилые дети этих гермафродитов, но при этом часть накопленных за жизнь мутаций передаются детям-почти клонам, что правда им не мешает размножаться и не ухудшаться из поколения в поколения, а также рождаться как и все дети – с нулевым возрастом.
Получается что накопление мутаций это только часть явления старения и в общем то они не мешают сбрасывать возраст яйцеклетки при зачатии.
Жар, в омоложении участвуют не только гены, стволовые клетки, фармпрепараты и т.д. но и другие, более “продвинутые” и скорее всего,самые трудно уязвимые, биологические механизмы – это биогенные поля-матрицы ДНК-клетки-органа-организма-вида-рода….Эта иерархия и есть главный источник управления и устойчивости любого живого организма-клетки. Открыли и наглядно /на фото/ продемонстрировали действие этого механизм ещё в 50 годах русские биологи из Алма-Аты – супруги Кирлиан. Сейчас это направление управления развитием-старением ой как далеко ушло вперёд.
Спасибо за статью, за ваш труд! Очень интересно.
Спасибо Дмитрий. Вы молодец.
Очень грамотный и хороший материал публикуете.
Дай Бог Вам здоровья, и избежания мести номенклатурных академиков России/их у нас аж 2500 тыс. /. Не все из них конечно номенклатурные/назначенные/, есть и настоящие. Но таковых мало.
Дмитрий очень интересно*** спасибо!
Что вы думаете по магнию треонату я принимаю его*
ru.iherb.com/pr/life-extension-neuro-mag-magnesium-l-threonate-90-veggie-caps/40244
Второй вопрос все же меня беспокоит риск возникновения лекарственного гепатита, нас учили что приём более 5 лекарств приведёт именно к этому !
Мы в косметологии давно используем фактор роста фибробластов и весьма успешно!!! Единственное смущал вопрос лимита хейфлика)
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Треонат магния сильно уступает цитрату магния, так как цитрат – это лимонная кислота и вместе с магнием имеет очень много доказанных в КИ свойств для продления жизни на людях, которых у треоната нет
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Факторы роста фибробластов бывают разные. 21 – ый наоборот защищает теломеры.
в программе не лекарств, которые негативно влияют на печень. И анализы многих читателей это подтверждают.
Здравствуйте спасибо за статью, у меня вопрос? На протяжении двух лет я придерживаюсь определённого распорядка, уром метформин 500 ,карведилол 12,5 вечером рамиприл 2,5 и магний В6, естественно придерживаюсь диеты, из простых углеводов оставил бананы после тренировки, и вопрос я всегда считал что высокой уровень соматотропина показатель здоровья? Получается это не так, или я что-то не понял? То есть тренировки со штангой вредны, так как способствуют выбросу гормона роста?
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Да. Вредны. Полезны умеренные физнагрузки.
Превосходная статья, Дмитрий! Поздравляю. ))
Только небольшая поправка: Цитрата магния не 300-400 мг в сутки, а 1.9-2.4 гр (1/2 чайной ложки), что в пересчете соответствует 300-400 мг чистого магния в сутки.
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
ДА. Я имел ввиду элементарного магния.
А что можете сказать насчет сульфата магния?
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Сульфат магния не снижает мочевую кислоту, что очень важно
Все же это технологии будущего, да и не всегда доступные для большинства.У нас в стране так мало выделяется средств для науки и медицины.
Дмитрий , а генная терапия делается по результатам генетического теста?
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Мы собираемся в Китай ехать в рамках школы долголетия – в тот институт, который делает на людях генотерапию. И будет там договариваться сначало делать генотерапию на нас самих. Думаю – это дело 5-10 лет, когда можно будет уже свободно заниматься редактированием