Обновлено: 29 декабря 2023
Радикальное продление жизни – часть 13. В поисках модели изучения старения человека
Скорость старения и продолжительность жизни животных определяются тем, как эволюция подстраивает вид для улучшения его шансов на выживание и успешное размножение. Эволюция может сократить продолжительность жизни, если это усиливает конкурентоспособность вида за счет ускорения размножения, либо привести к увеличению продолжительности жизни животных тогда, когда большинство особей вида не погибает в молодости, что позволяет особям в более старшем возрасте активно участвовать в размножении и передаче своих генов. В таких условиях особи, способные поддерживать здоровье и репродуктивную функцию на протяжении более длительного времени, получают эволюционное преимущество, ведь они могут оставить больше потомства, способствуя тем самым увеличению средней продолжительности жизни вида. Скорее всего голые землекопы стареют также, как и другие млекопитающие, а представление о пренебрежимом старении изменится через 5-10 лет наблюдения. Максимальная продолжительность жизни гренландской акулы составляет не менее 272 лет, а ее артериальное давление в 5-7 раз ниже, чем у человека. Люди умирают прежде всего от сердечно-сосудистых заболеваний. Поэтому признаки старения мышей оставим для тех, кто является не долгоживущей мышью.
Скорость старения и продолжительность жизни животных определяются тем, как эволюция подстраивает вид для улучшения его шансов на выживание и успешное размножение
Представим, что в ванной комнате есть кран, который люди обычно закрывают сами после наполнения ванны водой. Но что, если кто-то забудет закрыть кран? Изначально вода из крана была необходима, чтобы наполнить ванну. Но если кран оставить открытым, вода продолжит литься, бесполезно переливаясь через края ванны и заливая комнату. Таким образом, первоначально полезное действие (открытие крана для наполнения ванны) превращается во вредное (затопление комнаты).
 Это можно сравнить с процессом старения в организме. У организма есть своя программа развития, которая хорошо работает до определенного возраста. В дикой природе животные редко доживают до глубокой старости, поэтому эволюция не совершенствовала эту программу для работы в старости. Таким образом, системы организма, изначально способствующие его развитию и благополучию, с возрастом могут начать работать неэффективно и приводить к различным проблемам, связанным со старением.
Это можно сравнить с процессом старения в организме. У организма есть своя программа развития, которая хорошо работает до определенного возраста. В дикой природе животные редко доживают до глубокой старости, поэтому эволюция не совершенствовала эту программу для работы в старости. Таким образом, системы организма, изначально способствующие его развитию и благополучию, с возрастом могут начать работать неэффективно и приводить к различным проблемам, связанным со старением.
Среди большинства видов животных в дикой природе и среди людей в древние времена лишь единицы доживали до старости, и очень немногие умирали от старости [pubmed.ncbi.nlm.nih.gov/18156807] [pubmed.ncbi.nlm.nih.gov/18811399] [pubmed.ncbi.nlm.nih.gov/11295518]. Наши предки, неандертальцы, которые являются одними из ближайших родственников современного человека, редко доживали до пожилого возраста. Большинство из них не проживало более 30 лет. Найдены лишь несколько неардентальцев в возрасте 40 лет [scientificamerican.com/article/the-evolution-of-grandparents-2012-12-07]. Основная часть найденных неардентальцев умерла в возрасте значительно более молодом, чем 30 лет. Бабушки и дедушки были редкостью в древних популяциях [scientificamerican.com/article/the-evolution-of-grandparents-2012-12-07].
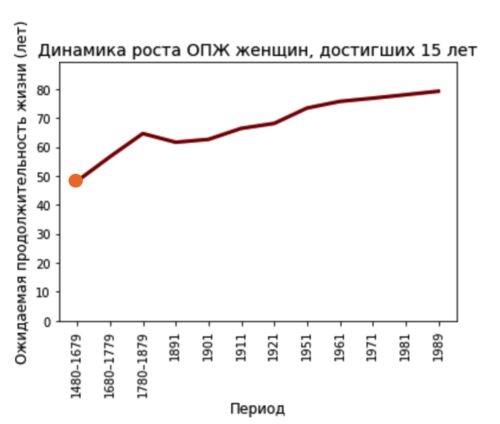 Рисунок. Рост ожидаемой продолжительности жизни (ОПЖ) женщин, достигших 15 лет [journals.sagepub.com/doi/10.1258/jrsm.2008.08k037].
Рисунок. Рост ожидаемой продолжительности жизни (ОПЖ) женщин, достигших 15 лет [journals.sagepub.com/doi/10.1258/jrsm.2008.08k037].
Однако все изменилось 30 000 лет назад, когда количество пожилых людей возросло в 5 раз, а люди начали жить дольше из-за культурных изменений [onlinelibrary.wiley.com/doi/10.1002/ajpa.20360]. Однако еще высокой оставалась детская смертность. Еще 200-250 лет назад в Швеции младенческая смертность составляла 40%, а сегодня в США - 0,54% [cdc.gov/reproductivehealth/maternalinfanthealth/infantmortality.htm].
Детская смертность стала низкой из-за здравоохранения, санитарии, иммунизации, доступа к чистой воде и лучшему питанию [cambridge.org/core/journals/journal-of-developmental-origins-of-health-and-disease/article/abs/early-cohort-mortality-predicts-the-rate-of-aging-in-the-cohort-a-historical-analysis/BC4A4FE7F8364BE7C69EB05FFB44BF85].
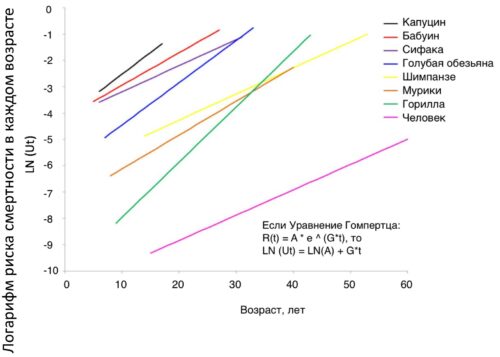 Рисунок. Данные о возрастных показателях смертности в нескольких популяциях разных родов приматов и людей [pubmed.ncbi.nlm.nih.gov/34135334] [pubmed.ncbi.nlm.nih.gov/21393544] [ncbi.nlm.nih.gov/pmc/articles/PMC3396421/bin/NIHMS384294-supplement-Supplementary.pdf].
Рисунок. Данные о возрастных показателях смертности в нескольких популяциях разных родов приматов и людей [pubmed.ncbi.nlm.nih.gov/34135334] [pubmed.ncbi.nlm.nih.gov/21393544] [ncbi.nlm.nih.gov/pmc/articles/PMC3396421/bin/NIHMS384294-supplement-Supplementary.pdf].
С точки зрения эволюции, люди совсем недавно стали доживать до старости. Поэтому, хотя продолжительность жизни людей и выросла, скорость их старения еще практически не отличается от некоторых видов приматов. Например, женщины стареют примерно с такой же скоростью, как самки шимпанзе – наклоны кривых смертности похожи (см. рисунок).
А живут люди больше из-за «оптимизации». Но чтобы люди стали медленнее стареть, чем остальные приматы, нужны еще миллионы лет эволюции, при условии низкой смертности в молодости.
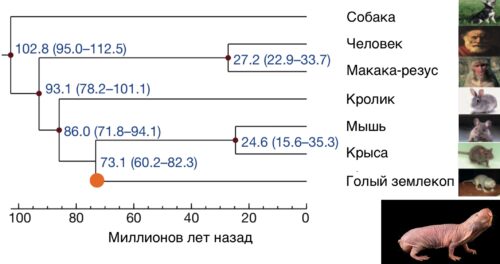 Рисунок. Так голый землекоп эволюционировал 73 млн. лет, чтобы стареть медленнее мыши и жить в 10 раз дольше [pubmed.ncbi.nlm.nih.gov/21993625]. Чтобы голый землекоп, стал голым землекопом, старел медленнее мыши и жил в 10 раз дольше эволюция добавила ему 45 новых генов, ассоциированных с долголетием. А вообще в сумме эволюция устранила 320 генов у голого землекопа и добавила 750 новых генов. Но среди них только 45 генов мутировали таким образом, что их изменения помогли грызунам жить дольше, чем их общие с мышами предки [pubmed.ncbi.nlm.nih.gov/21993625].
Рисунок. Так голый землекоп эволюционировал 73 млн. лет, чтобы стареть медленнее мыши и жить в 10 раз дольше [pubmed.ncbi.nlm.nih.gov/21993625]. Чтобы голый землекоп, стал голым землекопом, старел медленнее мыши и жил в 10 раз дольше эволюция добавила ему 45 новых генов, ассоциированных с долголетием. А вообще в сумме эволюция устранила 320 генов у голого землекопа и добавила 750 новых генов. Но среди них только 45 генов мутировали таким образом, что их изменения помогли грызунам жить дольше, чем их общие с мышами предки [pubmed.ncbi.nlm.nih.gov/21993625].
Эволюция может сократить продолжительность жизни, если это усиливает конкурентоспособность вида за счет ускорения размножения
Эволюция иногда формирует более короткую продолжительность жизни у животных для выживания вида. Это было продемонстрировано в эксперименте с нематодами, где ученые изменяли ген Age1, замедляя старение и увеличивая продолжительность жизни в 9 раз [genetics.org/content/204/3/905]. Однако, когда этих долгоживущих мутантных червей поместили в одну среду с червями дикого типа, которые живут значительно меньше, через несколько поколений в среде остались только короткоживущие черви. Это произошло потому, что быстрое размножение дало короткоживущим червям эволюционное преимущество в конкуренции, подчеркивая, что в определенных условиях эволюция отдает предпочтение короткой продолжительности жизни для обеспечения выживания вида.
В природе существуют различные стратегии выживания, включая генетические адаптации, которые могут сокращать продолжительность жизни отдельных особей, но способствуют выживанию вида в целом. Такое явление называется эволюцией адаптационного типа. В природе некоторые животные и растения имеют уникальные генетические особенности, которые сокращают их жизнь, но это помогает выжить всему виду.
Например, тихоокеанский лосось умирает сразу после того, как отложит икру, передавая таким образом питательные вещества своим потомкам. Некоторые виды агавы цветут только один раз за всю жизнь и затем умирают, но при этом производят множество семян для распространения вида. Октопауки-самки часто умирают вскоре после выметывания яиц, обеспечивая их защиту. Однодневки, насекомые с очень коротким жизненным циклом, живут всего один день во взрослом состоянии, но за это время успевают размножиться. Эти стратегии позволяют видам сохраняться и развиваться, даже ценой короткой жизни отдельных особей.
С другой стороны, эволюция часто работает так, что увеличивает время, в течение которого живут разные виды животных. Вот почему сегодня люди и даже другие приматы живут гораздо дольше, чем древний общий предок людей, приматов и собак. Важно не путать животных, которым эволюция ускорила старение для выживания вида, с животными, которые в прошлом дольше не жили.
Эволюция способствует увеличению продолжительности жизни животных тогда, когда большинство особей вида не погибает в молодости, что позволяет особям в более старшем возрасте активно участвовать в размножении и передаче своих генов. В таких условиях особи, способные поддерживать здоровье и репродуктивную функцию на протяжении более длительного времени, получают эволюционное преимущество, ведь они могут оставить больше потомства, способствуя тем самым увеличению средней продолжительности жизни вида
Эволюция способствует увеличению продолжительности жизни животных тогда, когда большинство особей вида не погибает в молодости. Так, если животные успешно избегают ранней смерти, например, от хищников, естественный отбор начинает работать в пользу увеличения продолжительности их жизни. Размер тела животного, как правило, связан с меньшим количеством внешних угроз, ведь крупные животные реже становятся жертвами хищников. Но размер не единственный фактор: например, летучие мыши, благодаря способности летать, избегают многих угроз и живут дольше, чем другие млекопитающие схожего размера.
Голый землекоп – отличный пример того, как вид может обрести долголетие, используя уникальные стратегии для избегания внешних угроз. Эти животные живут гораздо дольше, чем другие мелкие животные, благодаря тому что прячутся под землей, где их сложно найти хищникам.
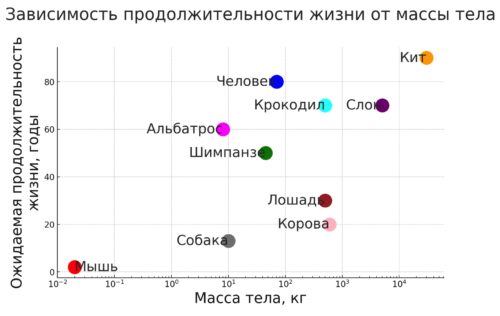 Рисунок. Зависимость продолжительности жизни от массы тела. Масса тела плохо коррелирует с долголетием. Почему, например, корова весит больше, чем шимпанзе, а живет меньше?
Рисунок. Зависимость продолжительности жизни от массы тела. Масса тела плохо коррелирует с долголетием. Почему, например, корова весит больше, чем шимпанзе, а живет меньше?
Это показывает, что не только размер, но и другие адаптации, такие как умение прятаться или летать, могут влиять на продолжительность жизни животных в эволюционном контексте. В итоге именно способность избегать ранней смерти влияет на скорость эволюционного развития долголетия у различных видов.
Важно понимать, что долгая жизнь голых землекопов по сравнению с мышами не должна создавать ложное представление о взаимосвязи между размером животного и его продолжительностью жизни. То, что землекопы живут в 10 раз дольше мышей, не означает, что существует какое-то биологическое правило, согласно которому животные одинакового размера должны иметь схожую продолжительность жизни. Размер тела скорее является фактором, влияющим на способность избегать хищников, но не является определяющим фактором долголетия. Истинное "выдающееся" долголетие — это когда продолжительность жизни животного превышает человеческую, то есть длится более 120 лет, и здесь весовая категория не играет ключевой роли. Примеры таких животных включают гренландских акул и некоторых видов китов.
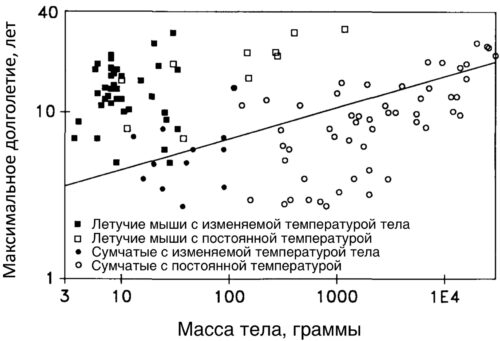 Рисунок. Показана связь между продолжительностью жизни и размером тела животных. Он демонстрирует, что не скорость обмена веществ, а способность избегать опасностей влияет на продолжительность жизни. Летучие мыши, отмеченные черными квадратиками, живут дольше, чем ожидалось для животных их размера, потому что они могут улетать от хищников, увеличивая свое долголетие на 80% по сравнению с сумчатыми того же размера. Сумчатые животные, в свою очередь, становятся более устойчивыми к угрозам по мере увеличения размера тела, что также способствует более долгому сроку жизни [pubmed.ncbi.nlm.nih.gov/1997563].
Рисунок. Показана связь между продолжительностью жизни и размером тела животных. Он демонстрирует, что не скорость обмена веществ, а способность избегать опасностей влияет на продолжительность жизни. Летучие мыши, отмеченные черными квадратиками, живут дольше, чем ожидалось для животных их размера, потому что они могут улетать от хищников, увеличивая свое долголетие на 80% по сравнению с сумчатыми того же размера. Сумчатые животные, в свою очередь, становятся более устойчивыми к угрозам по мере увеличения размера тела, что также способствует более долгому сроку жизни [pubmed.ncbi.nlm.nih.gov/1997563].
Это подчеркивает, что факторы, определяющие продолжительность жизни, могут быть разнообразными и не всегда связаны с размером тела, как видно из того, что человек живет дольше, чем слон, а некоторые приматы — дольше, чем коровы.
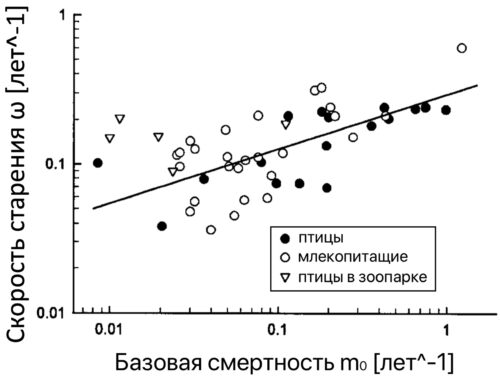 Рисунок. Показана взаимосвязь между базовой смертностью животных — то есть риском смерти от естественных причин, — и скоростью их старения. Здесь мы видим, что птицы и млекопитающие, которые подвержены большему риску смерти в молодом возрасте из-за хищников или других внешних факторов, стареют быстрее. Это наблюдение справедливо, несмотря на различия в размере тела и метаболической активности между видами. Так, птицы, живущие в зоопарках, где они защищены от хищников, показывают более медленную скорость старения по сравнению с их сородичами в дикой природе, что подтверждает, что безопасность может существенно увеличивать продолжительность жизни.
Рисунок. Показана взаимосвязь между базовой смертностью животных — то есть риском смерти от естественных причин, — и скоростью их старения. Здесь мы видим, что птицы и млекопитающие, которые подвержены большему риску смерти в молодом возрасте из-за хищников или других внешних факторов, стареют быстрее. Это наблюдение справедливо, несмотря на различия в размере тела и метаболической активности между видами. Так, птицы, живущие в зоопарках, где они защищены от хищников, показывают более медленную скорость старения по сравнению с их сородичами в дикой природе, что подтверждает, что безопасность может существенно увеличивать продолжительность жизни.
Птицы могут улететь от хищника и имеют больше шансов не погибнуть, вероятно, из-за этого, живут дольше, несмотря на высокий уровень глюкозы в крови. Птицы значительно дольше живут, чем млекопитающие аналогичного размера [pubmed.ncbi.nlm.nih.gov/7874580] [jstor.org/stable/3884204].
 Это говорит о том, что для разработки методов замедления старения человека важно учитывать не только физиологические, но и экологические факторы, влияющие на долголетие. До сих пор неясно, в какой степени знания о механизмах старения, полученные в короткоживущих модельных организмах, могут быть переданы долгоживущим видам, таким как человек. Специфические приспособления, способствующие долгой и здоровой жизни, из огромного эволюционного инструментария могут быть полностью упущены [pubmed.ncbi.nlm.nih.gov/34079817]. Сомнительно, что механизмы продления жизни, выявленные у короткоживущих видов, имеют большое значение для долгоживущих видов, таких как человек [pubmed.ncbi.nlm.nih.gov/28698112].
Это говорит о том, что для разработки методов замедления старения человека важно учитывать не только физиологические, но и экологические факторы, влияющие на долголетие. До сих пор неясно, в какой степени знания о механизмах старения, полученные в короткоживущих модельных организмах, могут быть переданы долгоживущим видам, таким как человек. Специфические приспособления, способствующие долгой и здоровой жизни, из огромного эволюционного инструментария могут быть полностью упущены [pubmed.ncbi.nlm.nih.gov/34079817]. Сомнительно, что механизмы продления жизни, выявленные у короткоживущих видов, имеют большое значение для долгоживущих видов, таких как человек [pubmed.ncbi.nlm.nih.gov/28698112].
Когда в природе животные регулярно доживают до пожилого возраста, самцы, которые лучше сохраняют здоровье на протяжении жизни, имеют больше шансов спариться с самками. Это дает возможность эволюции отдавать предпочтение тем чертам, благодаря которым животные могут жить дольше и оставаться здоровыми до старости [pubmed.ncbi.nlm.nih.gov/11295518].
Голые землекопы тоже стареют
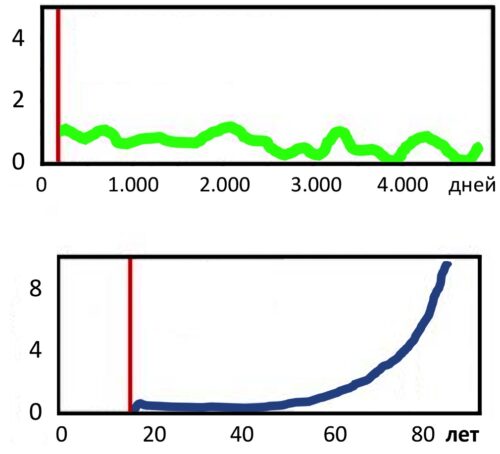 На рисунке показаны кривые смертности для голых землекопов (зеленая линия) и человека (синяя линия), которые отражают вероятность смерти в зависимости от возраста. Выборка животных > 3200 особей [elifesciences.org/articles/31157] – более половины животных еще живы.
На рисунке показаны кривые смертности для голых землекопов (зеленая линия) и человека (синяя линия), которые отражают вероятность смерти в зависимости от возраста. Выборка животных > 3200 особей [elifesciences.org/articles/31157] – более половины животных еще живы.
Зеленая линия, представляющая голых землекопов, остается относительно стабильной и не показывает увеличения риска смерти с возрастом в течение 5000 дней наблюдений. Это, возможно, ложно предполагает, что голые землекопы могут быть пренебрежимо мало стареющими, то есть их вероятность умереть не увеличивается со временем, как это видно на примере людей до 50 лет, где синяя линия также остается плоской. Однако это не означает, что голые землекопы не стареют вовсе, так как для окончательных выводов необходимо наблюдение до естественной смерти всех особей в выборке. Ведь это не значит, что люди не стареют, если их наблюдать только до 50 лет.
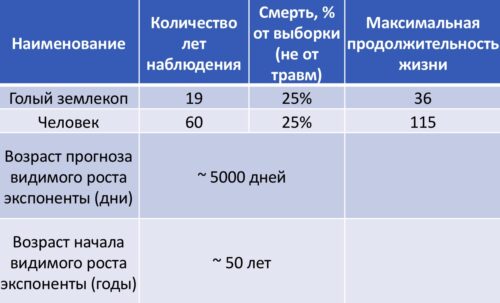 Таблица на рисунке сравнивает наблюдаемые данные по продолжительности жизни и смертности для голых землекопов и человека.
Таблица на рисунке сравнивает наблюдаемые данные по продолжительности жизни и смертности для голых землекопов и человека.
Для голых землекопов максимальная зафиксированная продолжительность жизни составила 36 лет при 19 годах наблюдения, в течение которых умерла четверть выборки, если исключить случайную смертность от травм. В случае с людьми максимальная продолжительность жизни достигает 115 лет, при этом к 60 годам также умерла четверть наблюдаемых в США, если исключить случайную смертность от травм [pubmed.ncbi.nlm.nih.gov/30099284]. Отмечено, что видимый рост смертности для людей начинается примерно с 50-летнего возраста, что может указывать на начало видимого процесса старения, в то время как для голых землекопов такой точный возрастной порог пока не определен и предполагается, что он может проявиться после 5000 дней наблюдений, что составляет около 14 лет. Если это так, то через 5 лет мы узнаем стареют ли голые землекопы.
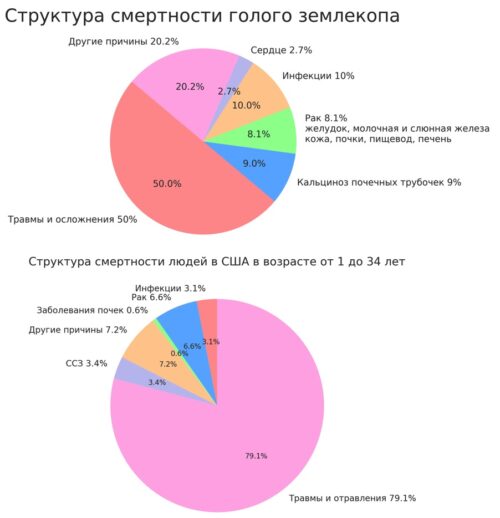 На первом рисунке представлена структура смертности голых землекопов [pubmed.ncbi.nlm.nih.gov/29486700].
На первом рисунке представлена структура смертности голых землекопов [pubmed.ncbi.nlm.nih.gov/29486700].
Большая часть смертей (50%) происходит из-за травм и осложнений, связанных с ними. Остальные причины смерти распределяются между инфекциями (10%), раком различных органов (8.1%), кальцинозом почечных трубочек (9%) и заболеваниями сердца (2.7%), а также другими причинами (20.2%). Это указывает на разнообразие причин смерти среди голых землекопов, не связанных напрямую со старением.
На втором рисунке показана структура смертности людей в США в возрасте от 1 до 34 лет [pubmed.ncbi.nlm.nih.gov/30099284].
Подавляющее большинство смертей в этой возрастной группе (79.1%) происходит в результате травм и отравлений. Инфекции (3.1%), рак (6.6%), и другие причины (7.2%) составляют меньшую часть. Это демонстрирует, что в молодом возрасте смертность у людей, как и у голых землекопов, в основном вызвана внешними факторами, а не процессами старения.
Сравнивая оба рисунка, можно увидеть, что структура смертности у голых землекопов и у людей моложе 34-36 лет довольно схожа, с доминированием внешних причин, таких как травмы, над возрастными заболеваниями. Это сходство говорит о том, что механизмы долголетия у голых землекопов, вероятно, не дают уникальных уроков для увеличения продолжительности жизни человека, поскольку оба вида в возрасте до 34-36 лет подвержены смерти в основном от не связанных со старением причин.
Один из способов оценить возраст — использовать эпигенетические маркеры, которые изучают химические изменения в ДНК. Но на данный момент такие методы, включая популярные "Часы Хорвата" первого поколения, не идеальны и могут давать ошибку от 18 до 40% [pubmed.ncbi.nlm.nih.gov/29718110], потому что они не основаны на долгосрочных данных — на изменении этих маркеров со временем. Тем не менее, эти методы тоже заслуживают внимания при оценке возраста.
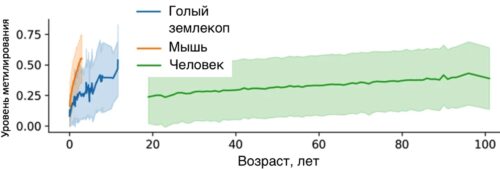 Рисунок. Голый землекоп эпигенетически по оценке уровня метилирования стареет медленнее, чем мышь, и намного быстрее, чем люди, что соответствует их максимальной продолжительности жизни. Изменение среднего уровня метилирования сайтов CpG ДНК по вертикальной оси в зависимости от возраста у голого землекопа, мыши и человека. Стандартное отклонение для каждой линии показано светлым цветом вокруг основной линии графика [pubmed.ncbi.nlm.nih.gov/35039495].
Рисунок. Голый землекоп эпигенетически по оценке уровня метилирования стареет медленнее, чем мышь, и намного быстрее, чем люди, что соответствует их максимальной продолжительности жизни. Изменение среднего уровня метилирования сайтов CpG ДНК по вертикальной оси в зависимости от возраста у голого землекопа, мыши и человека. Стандартное отклонение для каждой линии показано светлым цветом вокруг основной линии графика [pubmed.ncbi.nlm.nih.gov/35039495].
Максимальная продолжительность жизни гренландской акулы составляет не менее 272 лет, а ее артериальное давление в 5-7 раз ниже, чем у человека
 Рисунок. В 2022 году на берег Англии выбросилась 100-летняя гренландская акула, которая погибла из-за бактериального менингита [pubmed.ncbi.nlm.nih.gov/37244160]. Это единственный случай, когда известна причина смертности гренландской акулы до 2022 года. Другие причины, почему они умирают, пока не известны.
Рисунок. В 2022 году на берег Англии выбросилась 100-летняя гренландская акула, которая погибла из-за бактериального менингита [pubmed.ncbi.nlm.nih.gov/37244160]. Это единственный случай, когда известна причина смертности гренландской акулы до 2022 года. Другие причины, почему они умирают, пока не известны.
Радиоуглеродный анализ ядер хрусталика глаза 28 самок гренландской акулы показал, что максимальная продолжительность жизни составляет не менее 272 лет. Возраст наступления половой зрелости гренландской акулы составляет не менее 156 ± 22 лет [pubmed.ncbi.nlm.nih.gov/27516602].
Артериальное давление у гренландской акулы может быть ниже 2 кПа, что примерно в 5-7 раз ниже, чем у человека и ниже, чем у других рыб, что может снизить механический стресс и износ эластиновых волокон у акул этого вида. Эластин в стенке аорты гренландской акулы организован более диффузно, чем в аорте позвоночных, что обеспечивает упругость при низких давлениях. Область, занимаемая эластином в ее аорте, составляет 27 ±2.5%. Это вдвое меньше, чем в аортах млекопитающих [pubmed.ncbi.nlm.nih.gov/30104302]. Средняя гренландская акула (224 кг) нуждается в поддерживающем рационе из 61-193 г рыбы или добычи морских млекопитающих в день. Гренландская акула, потребляющая очень мало энергии из пищи и имеющая низкое кровяное давление, ведет себя очень медленно и экономно расходует энергию. Из-за своей медлительности эта акула иногда называется летаргической, так как она кажется вялой и не проявляет агрессии. Это животное настолько неторопливо, что может совершать лишь несколько медленных взмахов хвостом за минуту. Она избегает конфликтов с более быстрыми и агрессивными хищниками, предпочитая охотиться на неподвижную (спящую) или больную добычу, а также питаться останками умерших животных [pubmed.ncbi.nlm.nih.gov/35258589].
Люди умирают прежде всего от сердечно-сосудистых заболеваний. Поэтому признаки старения мышей оставим для тех, кто является не долгоживущей мышью
Учеными установлены признаки старения мышей [ncbi.nlm.nih.gov/pubmed/23746838]:
- Накопление сенесцентных клеток
- Утрата функция митохондрий
- Сокращение теломер
- Нарушение стабильности ДНК
- Повышение окислительного стресса
- Эпигенетические изменения
- Сокращение стволовых клеток
- и др.
Человек - это долгоживущий организм. И механизмы старения короткоживущих животных могут не иметь отношения к организмам долгоживущих животных. Например, у голых землекопов в 10 раз выше уровень перекисного окисления липидов, в два раза выше уровень продуктов окисления липидов, в 2-8 раз выше уровень повреждения ДНК, в 1,5-2 раза выше уровень повреждения белков в сравнении с мышами, но это не мешает им жить в 10 раз дольше мышей [pubmed.ncbi.nlm.nih.gov/17054663].
Известные биологам признаки старения, могут уже даже не иметь отношения даже к долгоживущими мышам в сравнении с их короткоживущими собратьями. Так сокращение калорийности питания или голодания замедляют сокращение теломер [pubmed.ncbi.nlm.nih.gov/22237065] [pubmed.ncbi.nlm.nih.gov/11446772], задерживают накопление сенесцентных клеток [pubmed.ncbi.nlm.nih.gov/30562419], уменьшают повреждения ДНК, например, из-за снижения экспрессии SIRT6 [pubmed.ncbi.nlm.nih.gov/26940461], замедляют возрастное ухудшение функции митохондрий [pubmed.ncbi.nlm.nih.gov/17341128], задерживают возрастное изменение метилирования ДНК [pubmed.ncbi.nlm.nih.gov/28912502], омолаживают стволовые клетки [pubmed.ncbi.nlm.nih.gov/24905167] [pubmed.ncbi.nlm.nih.gov/30562419]. Но мышам Ларона, которые живут очень долго, сокращать калории и голодать бесполезно для продления жизни [ncbi.nlm.nih.gov/pubmed/19747233]. Так как у мышей Ларона очень низкий уровень инсулин-подобного фактора роста 1-го типа (ИФР-1).
Дикие мыши естественно имеют низкий уровень инсулин-подобного фактора роста 1-го типа (ИФР-1), который связан с долголетием [pubmed.ncbi.nlm.nih.gov/12094015]. В отличие от них инбрендные линии мышей, полученные в результате контролируемого скрещивания близкородственных особей в лабораторных условиях, потеряли свои природные черты долголетия и здоровья и имеют повышенный уровень ИФР-1, что считается неоптимальным. Однако ученые смогли вмешаться в этот процесс, регулируя жизненные условия и генетический фон, что позволило восстановить продолжительность жизни инбрендных мышей до уровня, характерного для диких мышей. Следует отметить, что дикие мыши – это мыши, обитающие в естественной среде, тогда как мыши дикого типа – это лабораторные мыши, которые не подвергались инбридингу и ближе по своему генетическому профилю к естественным популяциям. Таким образом, изучение процессов старения на примере инбрендных линий может не всегда давать точное представление о старении даже диких мышей, естественных популяций и долгоживущих мышей, не говоря уже о старение человека.
Также и сокращение стволовых клеток с возрастом - это не причина старения. Клетки могут жить, как минимум в разы дольше самих животных. Максимальная продолжительность мышей дикого типа 1 000 дней. Гемопоэтические стволовые клетки мышей могут жить минимум 3 000 дней [ncbi.nlm.nih.gov/pubmed/37377].
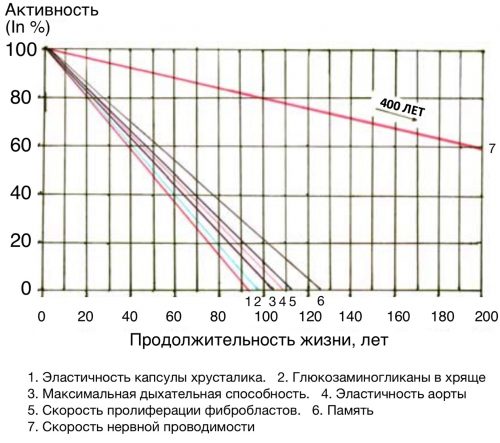 График. Старение частей организма. Возрастное снижение нескольких физиологических функций с указанием приблизительного возраста, когда функции достигнут нулевого уровня [pubmed.ncbi.nlm.nih.gov/18175202].
График. Старение частей организма. Возрастное снижение нескольких физиологических функций с указанием приблизительного возраста, когда функции достигнут нулевого уровня [pubmed.ncbi.nlm.nih.gov/18175202].
А клетки Т-лимфоциты мышей жили 3 650 дней (10 лет), оставаясь компетентными реагировать на вакцинацию, несмотря на увеличение исходной популяции в 1040 раз, Т–клетки не демонстрировали потери контроля над пролиферацией, выполняли антимикробные функции и формировали клетки памяти [nature.com/articles/s41586-022-05626-9].
Приблизительный верхний предел продолжительности жизни человека ограничивается на отметке 100-120 лет эластичными свойствами сердца, сосудов и системы дыхания [pubmed.ncbi.nlm.nih.gov/18175202].
Эластин в аорте может сокращаться в среднем не более 3 млрд. раз [pubmed.ncbi.nlm.nih.gov/22702062].
Эластические волокна постепенно разрушаются во время старения за счет механических воздействий (усталость) и действия ферментов (например, матриксных металлопротеаз или катепсина), уровень которых повышается из-за воспаления в результате старения иммунной системы и воспалительных заболеваний.
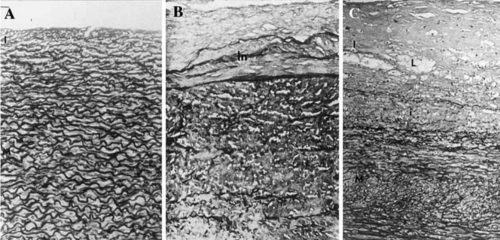
Рисунок. Гистологические срезы аорты человека, показывающие возрастное разрушение эластических волокон, прогрессирующее от внутренней стороны аорты к более глубоким частям: (a) около 20 лет; (b) около 60 лет; (c) около 85 лет [pubmed.ncbi.nlm.nih.gov/18175202].
В результате старения прогрессирует фрагментация эластиновых волокон - теряется непрерывность. При старении в медианной оболочке артерии прогрессирует нарушении организации с потерей упорядоченного расположения волокон и пластин эластина. Они подвергаются истончению, расщеплению, стиранию и фрагментации.
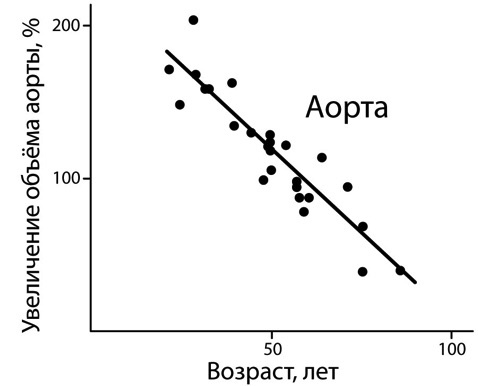 Рисунок. Возрастная потеря эластичности аорты [ncbi.nlm.nih.gov/pubmed/16706654].
Рисунок. Возрастная потеря эластичности аорты [ncbi.nlm.nih.gov/pubmed/16706654].
К 100 годам аорта теряет свою эластичность на столько, что наступает состояние несовместимое с жизнью [ncbi.nlm.nih.gov/pubmed/16706654].
Чтобы прокачать кровь через не эластичную аорту, сердце перенапрягается. Повышение систолического артериального давления увеличивает систолическую нагрузку на левый желудочек сердца, что приводит к увеличению потребления кислорода, гипертрофии левого желудочка сердца и его фиброзу. Все эти события предрасполагают к развитию возрастной сердечной недостаточности
[cyberleninka.ru/article/n/zhestkost-sosudov-i-diastolicheskaya-serdechnaya-nedostatochnost].
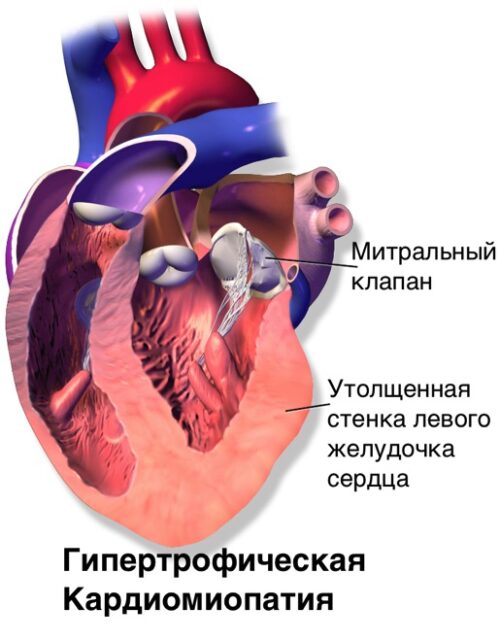 Рисунок. Увеличение отделов сердца при гипертрофической кардимиопатии.
Рисунок. Увеличение отделов сердца при гипертрофической кардимиопатии.
Читатель спросит, почему увеличение отделов сердца не фатально для молодых спортсменов. У них ведь тоже отдельные отделы сердца могут гипертрофироваться. Разница заключается в том, что сердце молодого спортсмена при гипертрофии не накапливает фиброз, а сама гипертрофия обратима. При старении сердце реагирует на нагрузку неадекватно, необратимо фиброзируется, теряя эластичность. Экспериментальные исследования показывают, что если стресс умеренный, применяется постепенно, а животное молодое и здоровое, то развивается физиологическая гипертрофия сердечной мышцы с нормальной сократительной способностью. В таком случае гипертрофию сердца можно рассматривать как полезную адаптацию к повышенной гемодинамической нагрузке. Когда провоцирующий стресс сильный, применяется внезапно, либо животное старое или ослабленное, то развивается патологическая гипертрофия. В этом случае сердечная мышца заменяется фиброзной тканью и проявляет пониженную сократительную способность [pubmed.ncbi.nlm.nih.gov/6448546]. Такие же результаты показывает гипертрофия сердечной мышцы при экспериментальной гипертензии у молодых и старых животных. У старых животных с артериальной гипертензией наблюдаются увеличение количества дистрофических и некротических клеток, а также увеличение очагов фиброза [pubmed.ncbi.nlm.nih.gov/6235863]. Эксперименты показывают, что старение препятствует восстановлению сердца после гипертрофии, препятствует восстановлению функции желудочков сердца после кардиомиопатии, вызванной изопротеренолом. После инфузии изопротеренола у пожилых мышей развивается сердечная недостаточность с гипертрофией клеток и фиброзом сердечной ткани. После отмены действия изопротеренола у молодых самок мышей наблюдается полное обращение вспять вызванной изопротеренолом сердечной недостаточности. И наоборот, обращение вспять сердечной недостаточности нарушено у пожилых животных. Не происходит восстановления фракции выброса, у старых наблюдается гипертрофия клеток сердца, сохраняется фиброз сердца. Пожилые животные, в отличие от молодых, демонстрируют нарушение обратного восстановления сердца, сохраняют фиброз сердечной мышцы, нарушение функции сердца даже после отмены действия изопротеренола [pubmed.ncbi.nlm.nih.gov/35008601]. Сшитый коллаген устойчив к деградации ферментами, значительно стабилизируя фиброз, делая его необратимым [pubmed.ncbi.nlm.nih.gov/33688918].
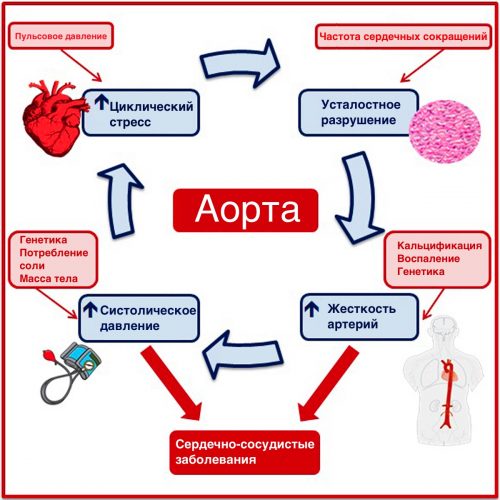
Рисунок. Циклический стресс, который испытывают артерии из-за регулярных сокращений сердца, является причиной усталости и разрушения эластина в аорте, так как эластин во взрослом организме не восстанавливается. Чем чаще сокращается сердце в течение жизни, тем больше циклический стресс. И это является основной причиной повышения жесткости аорты. Дополнительными причинами, ускоряющими разрушение эластина, являются воспаление и кальцификация аорты, о которых мы поговорим ниже. Жесткость аорты приводит к повышению систолического артериального давления, которое в свою очередь усиливает циклический стресс, и патологический круг замыкается [pubmed.ncbi.nlm.nih.gov/32102569].
Из-за того, что артерии становятся более жесткими, скорость распространения пульсовой волны увеличивается, усиливается пульсирующий ток в микрососудах мозга, почек. А возрастание сопротивления, которое оказывает восходящая аорта прохождению волны кровотока, приводит в конечном итоге к сердечной недостаточности даже в отсутствии атеросклероза [pubmed.ncbi.nlm.nih.gov/20733089].
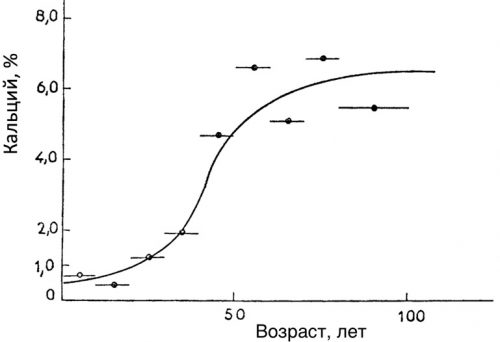 Рисунок. Увеличение содержания кальция с возрастом в очищенном эластине аорты человека [pubmed.ncbi.nlm.nih.gov/18175202].
Рисунок. Увеличение содержания кальция с возрастом в очищенном эластине аорты человека [pubmed.ncbi.nlm.nih.gov/18175202].
Вода наделяет эластин эластичными свойствами. С возрастом в эластине вода вытесняется кальцием и холестерином
[pubmed.ncbi.nlm.nih.gov/18175202]Устойчивый высокий уровень концентрации кальция в межклеточной жидкости, окружающей эластичные волокна, достаточен для постепенного насыщения кальцием доступных участков эластина в течение первых шести десятилетий жизни человека. Уровень кальция повышается при гиперпаратиреозе и терапии высокими дозами витамина D, если нет его дефицита. Поглощение липидов и кальция постепенно увеличивается в течение, по крайней мере, первых шести десятилетий жизни, быстрее у людей с образом жизни и питанием, благоприятствующими повышению уровня холестерина [pubmed.ncbi.nlm.nih.gov/18175202]. Также эластин подвергается гликированию [pubmed.ncbi.nlm.nih.gov/15036419], а для этого нужно не допустить развития сахарного диабета.
Меры по предупреждению ускоренного износа эластина
- Отказ от курения [pubmed.ncbi.nlm.nih.gov/35700534].
- Оптимальный уровень паратгормона в крови не более 9,4 пмоль/л и общего кальция ≤ 2,58 ммоль/л [pubmed.ncbi.nlm.nih.gov/18175202], не злоупотреблять корицей
- Лечение высокими дозами витамина D является классическим способом индукции кальцификации артерий в экспериментах на животных [pubmed.ncbi.nlm.nih.gov/16690876]
- Оптимальный уровень глюкозы < 6 ммоль/л и уровня систолического артериального давления < 130 мм.рт.ст. [pubmed.ncbi.nlm.nih.gov/32102569]
- Оптимальный уровень с-реактивного белка в крови < 1 мг/л [pubmed.ncbi.nlm.nih.gov/32102569]
- Предупреждать, либо правильно лечить хроническую болезнь почек, сахарный диабет и хронические воспалительные заболевания [pubmed.ncbi.nlm.nih.gov/30581820]
- Упражнения на растягивания мышц и аэробные физические нагрузки 150 минут в неделю, но исключить чрезмерные спортивные нагрузки
- Оптимальная окружность талии – не более половины высоты роста своего тела
- Лечить состояния не оптимальной (тахикардия) частоты сердечных сокращений.
Обязательно оставляйте свои комментарии под статьей, которую Вы читаете. Это очень важно для нас.
Предлагаем Вам оформить почтовую подписку на самые новые и актуальные новости, которые появляются в науке, а также новости нашей научно-просветительской группы, чтобы ничего не упустить. Обязательно оставляйте свои комментарии под статьей, которую вычитаете. Это очень важно для нас.

Автор статьи
Веремеенко Дмитрий Евгеньевич
Телефон:
Почта:
Исследователь, изобретатель, сфера деятельности - data science в медицине
Основатель проекта, изучающего терапии, направленные на увеличение продолжительности жизни человека (nestarenie.ru/slb-expert_.html)
Со-основатель IT сервиса продления жизни https://nestarenie.expert/
Основатель форума о продлении жизни Nestarenie Camp (nestarenie.ru/camp.html)
Со-автор книги "Бонусные годы" (nestarenie.ru/kniga-3.html)
Создатель справочного блога о старении человека (nestarenie.ru)
Социальные сети:
- Карта Viza (доллары): 4215 8901 1587 0138 для переводов за пределами РФ
- Карта МИР в Сбере (рубли): 2202 2032 1501 6686 (МАЙЯВИ Ч.) - на территории РФ
Свежие комментарии
Подпишитесь на свежие статьи
Предлагаем Вам оформить почтовую подписку на самые новые и актуальные новости, которые появляются в науке, а также новости нашей научно-просветительской группы, чтобы ничего не упустить.
3 комментария
Великолепная статья. Понимание механизмов эволюции есть один из столпов представления как устроена Реальность. Наряду с интуитивным пониманием физических законов и теории вероятностей. Жизненный цикл эластичности тканей дает нам крайне простое, понятное и реалистичное понимание основного механизма лимитирующего продолжительность жизни. Механизм простой, а вот борьба с ним невероятно сложна.. Зная это, нужно не мечтать о волшебной таблетке, а ценить оставшееся время жизнии и продлевать ее реалистичными методами, заодно улучшая качество.
А что дают упражнения по растяжению мышц в плане замедления деградации эластина в сердце, сосудах и легких?
Рекомендует только врач. Я не врач, но делюсь данными исследований.
Отрезайте у ссылок http:
Только в периферических артериях.