Дата создания: 9 августа 2022
Обновлено: 29 декабря 2023
Радикальное продление жизни — часть 4. Как восстановить или омолодить иммунитет
С возрастом снижается количество иммунных наивных Т-клеток и разнообразие их рецепторов, необходимых для эффективной реакции на незнакомые вирусы; снижается эффективность отбраковывания аутореактивных Т-лимфоцитов иммунной системы, способных вызывать хроническое воспаление и аутоиммунные заболевания
Иммунитет — система реакций, призванная защитить организм от атаки бактерий, вирусов, грибов и других вредоносных агентов. По мере старения иммунная защита организма снижается, что приводит к гибели пожилых людей в результате различных инфекций. Например, в США ежегодно от пневмококковой инфекции, вызывающей воспаление легких, умирает 40 000 человек - прежде всего людей старше 65 лет [pubmed.ncbi.nlm.nih.gov/9132580]. Из-за старения иммунитета снижается эффективность вакцинации пожилых людей [pubmed.ncbi.nlm.nih.gov/29242543], снижается функция иммунитета, направленная на уничтожение раковых опухолей [pubmed.ncbi.nlm.nih.gov/28966805] [pubmed.ncbi.nlm.nih.gov/30585859].
В 2010 году Тюбингенская группа иммунологии старения и опухолей опубликовала статью о том, что возрастные изменения иммунитета могут также способствовать возрастному росту заболеваемости большинством видов рака, ухудшая способность иммунных клеток распознавать и уничтожать раковые клетки [ncbi.nlm.nih.gov/pubmed/20656212].
Старение повышает восприимчивость к тяжелым инфекциям (к инфекциям мочевыводящих и дыхательных путей, пневмонии, коклюшу, гастриту, вызванному Helicobacter pylori, к вирусу ветряной оспы), которые являются одной из основных причин заболеваемости и смертности среди пожилого населения [pubmed.ncbi.nlm.nih.gov/23677590].
Также у пожилых людей утрачивается иммунитет, полученный в результате вакцинации в молодости.
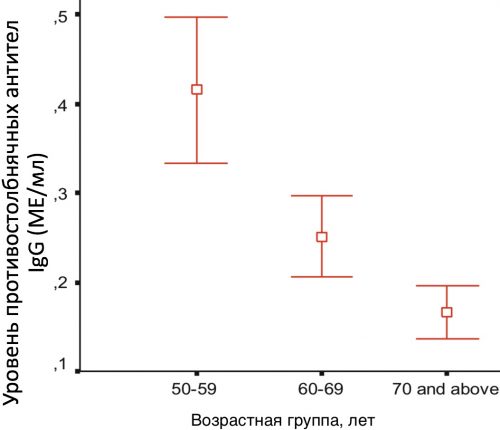 Например, в недавнем исследовании, проведенном среди турецких фермеров старше 50 лет, сообщалось, что присутствие в крови антител против столбняка в разных возрастных группах было разное и снижалось с возрастом: у 51,5% пациентов в возрасте 50-59 лет, у 36,4% пациентов в возрасте 60-69 лет, у 9,5% пациентов в возрасте старше 70 лет [pubmed.ncbi.nlm.nih.gov/21185104].
Например, в недавнем исследовании, проведенном среди турецких фермеров старше 50 лет, сообщалось, что присутствие в крови антител против столбняка в разных возрастных группах было разное и снижалось с возрастом: у 51,5% пациентов в возрасте 50-59 лет, у 36,4% пациентов в возрасте 60-69 лет, у 9,5% пациентов в возрасте старше 70 лет [pubmed.ncbi.nlm.nih.gov/21185104].
Рисунок 1. Среднее значение и 95 % доверительный интервал уровней столбнячного IgG в зависимости от возрастных групп [pubmed.ncbi.nlm.nih.gov/21185104].
В Соединенных Штатах в период с 2001 по 2008 год наибольшая доля умерших от столбняка - 20 случаев из 26 заболевших находится в возрастной группе старше 65 лет [pubmed.ncbi.nlm.nih.gov/21451446].
Вакцины являются эффективными в борьбе со многими инфекционными заболеваниями, но могут не подходить для лечения пожилых людей, поскольку иммунная система пожилых людей реагирует по другим правилам, чем у более молодого взрослого человека.
Все иммунные клетки организма образуются в костном мозге от гемопоэтических стволовых клеток, которые дают начало либо миелоидно-ориентированным, либо лимфоидно-ориентированным предшественникам клеток [ashpublications.org/blood/article/125/17/2587/34094/Introduction-to-a-review-series-on-hematopoietic]. Клетки приобретенного иммунитета происходят от лимфоидно-ориентированных предшественников и называются лимфоцитами, тогда как клетки врожденного иммунитета могут происходить от обоих предшественников.
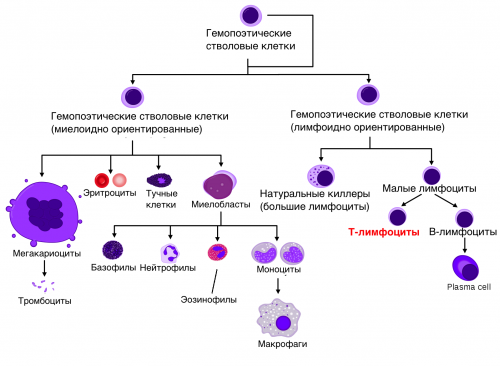 Рисунок 2. Гемопоэтическая стволовая клетка дает начало клеткам — предшественницам миелоидной и лимфоидной линий дифференцировки, из которых дальше образуются все типы клеток крови.
Рисунок 2. Гемопоэтическая стволовая клетка дает начало клеткам — предшественницам миелоидной и лимфоидной линий дифференцировки, из которых дальше образуются все типы клеток крови.
Клетки врожденного иммунитета не определяют точную принадлежность вредоносных агентов к тому или иному виду, а лишь сигнализируют о том, что иммунитет столкнулся с чужаками, и уничтожает их.
К клеткам врожденного иммунитета относятся следующие:
- макрофаги и дендритные клетки, которые поглощают и переваривают вредоносные агенты, а также создают сигналы для клеток адаптивного иммунитета
- нейтрофилы, которые поглощают вредоносные агенты, а после погибают - это клетки камикадзе
- эозинофилы, базофилы и тучные клетки, которые выделяют в окружающую ткань содержимое своих гранул — химическую защиту против крупных вредоносных агентов, например, паразитических червей. Однако такая защита вовлечена в развитие аллергической реакции
- натуральные киллеры, которые выделяют специальные белки для борьбы уже не с вредоносными агентами, а с зараженными клетками организма, в которые проник вредоносный агент
Итак, дендритные клетки (иммунные клетки врожденного иммунитета) создают сигналы для клеток адаптивного иммунитета, таких как Т и В лимфоциты, чтобы эти лимфоциты также уничтожали вредоносные агенты, но уже более "профессионально". Однако, старение влияет на экспрессию микро РНК (молекул, влияющих на то, как будут работать гены), регулирующих активацию воспалительного пути ядерного фактора κB в mDCs, способствуя снижению активации дендритных клеток иммунитета из-за нарушения активации толл-подобных рецепторов (TLR), расположенных на дендритных клетках [pubmed.ncbi.nlm.nih.gov/23252865]. Из-за нарушения активации толл-подобных рецепторов помимо ослабления синтеза дендритными клетками цитокинов (белковых молекул, привлекающих иммунные клетки для борьбы с вредоносными агентами), также ослабляется и экспрессия костимулирующей молекулы CD80, связанной с защитным ответом на вакцинацию против гриппа [pubmed.ncbi.nlm.nih.gov/20100933] [pubmed.ncbi.nlm.nih.gov/17471428]. Поэтому для повышения эффективности вакцин у пожилых людей необходимо увеличить и чувствительность толл-подобных рецепторов на дендритных клетках иммунитета [pubmed.ncbi.nlm.nih.gov/23677590]
Адаптивный иммунитет.
Вторгаясь в организм, вредоносные агенты оставляют молекулярные «следы», которые обнаруживают клетки иммунитета. Такие следы называются антигенами. Т-лимфоциты, а также B лимфоциты способны распознавать множество индивидуальных антигенов вредоносных агентов благодаря специализированным рецепторам на своей поверхности. Эти рецепторы называются Т-клеточными и В-клеточными соответственно. Каждый Т-лимфоцит или B-лимфоцит несет свой собственный уникальный рецептор к конкретному, уникальному антигену. Т-лимфоциты можно разделить на CD8+ Т-лимфоциты и CD4+ T-лимфоциты. В-лимфоциты несут на своей поверхности В-клеточный рецептор [nature.com/collections/htgxbjhfsy]. При контакте с антигеном эти клетки активируются и превращаются в особый клеточный подтип — плазматические клетки, обладающие уникальной способностью секретировать свой B-клеточный рецептор в окружающую среду. Такие B-клеточные рецепторы, секретируемые в окружающую среду, называются антителами. Развитие адаптивного иммунного ответа требует достаточно много времени (от нескольких дней до двух недель), и для того, чтобы организм мог защищаться от уже знакомой инфекции быстрее, из Т и В-клеток, участвовавших в прошлых битвах, формируются так называемые клетки памяти, которые, если появляется знакомый им вредоносный агент, вновь активируются, быстро делятся и целой армией атакуют вредоносный агент. Т-лимфоциты, успешно прошедшие отбор в тимусе (специализированном первичном лимфоидном органе иммунной системы), попавшие в кровь, но не имевшие контакта с антигеном, называются наивными Т-клетками. Основной функцией наивных Т-клеток является реакция на вредоносные агенты, прежде не известные иммунной системе организма. После того, как наивные Т-клетки распознают антиген, они становятся активированными. Часть активированных клеток трансформируется в Т-клетки памяти. Т-клетки памяти сохраняются в неактивной форме после первичного контакта с антигеном до тех пор, пока не наступает повторное взаимодействие с тем же антигеном. Таким образом, Т-клетки памяти хранят информацию о ранее действовавших антигенах и обеспечивают вторичный иммунный ответ, осуществляющийся в более короткие сроки, чем первичный.
Существуют и другие клетки иммунитета, представляющие иммунитет нервной системы, например, микроглия. Но о них мы исчерпывающе говорите, когда рассматривали причины болезни Альцгеймера.
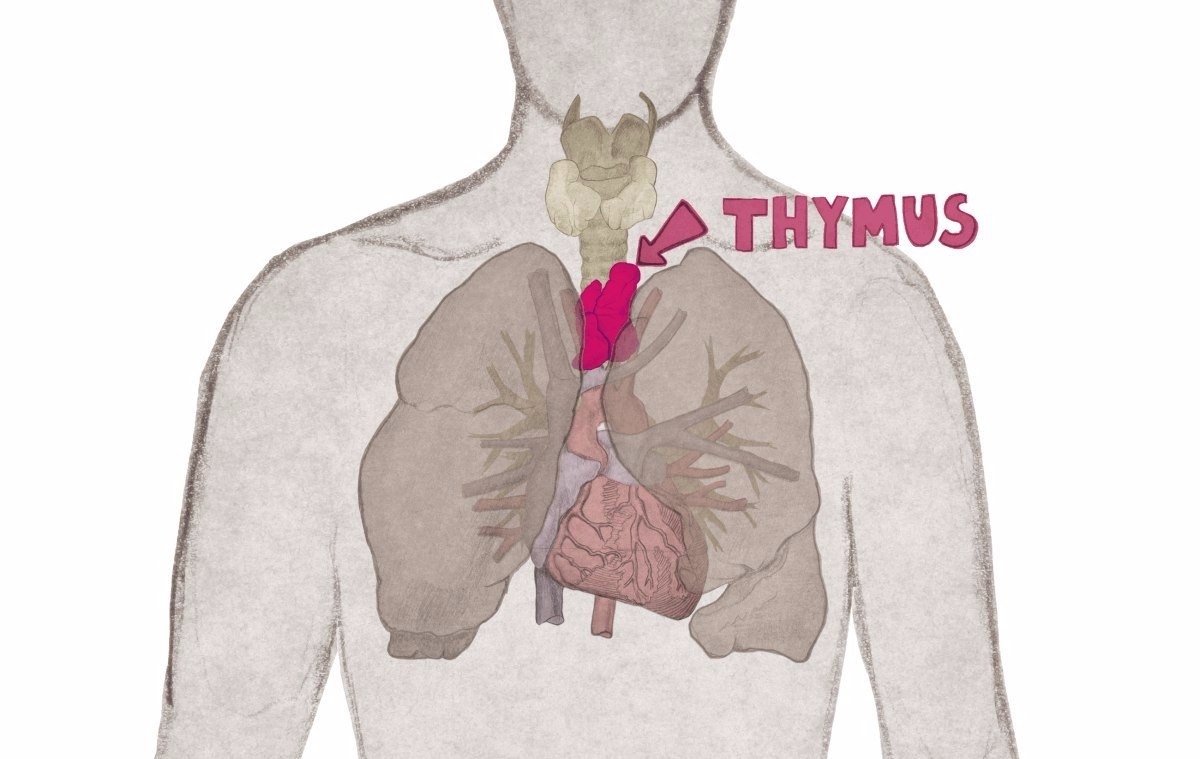
Предшественники Т-клеток (разновидность лимфоцитов) иммунитета созревают в костном мозге (ткань, находящаяся в губчатых частях костей) из гемопоэтических стволовых клеток.
Рисунок 3. Затем гемопоэтические стволовые клетки с кровью попадают в тимус (специализированный первичный лимфоидный орган иммунной системы).
Внутри тимуса созревают Т-лимфоциты (или Т-клетки). Но еще в костном мозге, в процессе своей специализации гемопоэтические стволовые клетки превращаются либо в миелоидно-ориентированные, либо в лимфоидно-ориентированные. Именно от лимфоидно-ориентированных происходят предшественники Т-клеток иммунитета. Но с возрастом гемопоэтические стволовые клетки становятся все чаще миелоидно-ориентированными. В результате создается все меньше Т-клеток предшественников. Возрастное уменьшение размеров истинной ткани тимуса и недостаточность гемопоэтических стволовых клеток играют важную роль в старении иммунитета [ncbi.nlm.nih.gov/pubmed/22830639].
Когда организм атакуют неизвестные вредоносные агенты, то на защиту в первую очередь встают клетки врожденного иммунитета. Дендритные клетки, поглотившие вредоносный агент, передают информацию о нём Т и В-лимфоцитам. Те активируются и перемещаются в местонахождение вредоносных агентов. В итоге вредоносные агенты гибнут, а часть T и B-лимфоцитов образуют клетки памяти, которые ждут, когда их помощь снова понадобится организму.
Повреждение собственных органов и тканей организма иммунной системой называется аутоиммунным процессом. К сожалению, иногда иммунные клетки организма начинают атаковать собственные клетки организма. За аутоиммунные поражения организма могут быть ответственны как Т, так и В-лимфоциты. Например, при рассеянном склерозе атакуется миелиновая оболочка нейронов (нервных клеток), при ревматоидном артрите — суставы, а при сахарном диабете первого типа — островки Лангерганса в поджелудочной железе. Отбор и удаление аутореактивных Т-лимфоцитов, способных вызывать аутоиммунные заболевания, осуществляется в тимусе. Стареющий, атрофированный тимус продолжает выделять Т-клетки на протяжении всей жизни человека. Однако атрофированный тимус менее эффективно отбраковывает аутореактивные Т-лимфоциты, высвобождая их в кровь, тем самым увеличивая предрасположенность стареющего человека к аутоиммунным заболеваниям [ncbi.nlm.nih.gov/pubmed/26318588]. Накопление аутореактивных Т-лимфоцитов также способствуют росту хронического воспаления по мере старения без явных источников воспаления [ncbi.nlm.nih.gov/pubmed/31988649]. С возрастом иммунная система претерпевает изменения. Эти изменения происходят во всех лейкоцитах и влияют на функцию врожденного и адаптивного иммунитета. Некоторые специфические иммунные реакции с возрастом ослабевают, другие не изменяются или даже усиливаются. Как это ни парадоксально, состояние вялотекущего хронического воспаления также часто наблюдается у пожилых людей. Такое хроническое воспалительное состояние получило название «воспалительное старение» [pubmed.ncbi.nlm.nih.gov/20200405].
У молодых пациентов обычно имеется огромное количество наивных Т-клеток иммунитета, которые никогда не сталкивались с вирусом. Риск тяжелого течения COVID-19 зависит от возраста [ncbi.nlm.nih.gov/pubmed/32240634]. Наибольший риск умереть от COVID-19 имеют пожилые люди в возрасте старше 65 лет (летальность – 5-14 %) [ilpost.it/2020/03/11/rapporto-istituto-superiore-sanita-coronavirus-italia]. Уже с первого года жизни ребёнка функциональная ткань тимуса заменяется на жировую. В результате в возрасте от 35 до 45 лет тимус уменьшается в размере каждый год жизни на 3%, а после 45 лет - на 1%. В 70 лет жировая ткань занимает 90% тимуса [pubmed.ncbi.nlm.nih.gov/23831111].
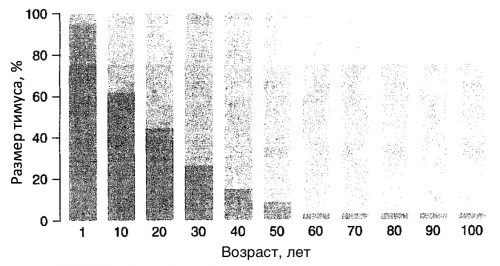 Рисунок 4, Инволюция тимуса начинается сразу после рождения и продолжается всю жизнь. Хотя общий размер тимуса человека остается почти таким же, объем истинной ткани тимуса (тимоцитов, эпителия, дендритных клеток и макрофагов; обозначенных темным штрихом на рисунке) уменьшается, а объем жировой ткани (светлый штрих на рисунке) увеличивается [pubmed.ncbi.nlm.nih.gov/8962629].
Рисунок 4, Инволюция тимуса начинается сразу после рождения и продолжается всю жизнь. Хотя общий размер тимуса человека остается почти таким же, объем истинной ткани тимуса (тимоцитов, эпителия, дендритных клеток и макрофагов; обозначенных темным штрихом на рисунке) уменьшается, а объем жировой ткани (светлый штрих на рисунке) увеличивается [pubmed.ncbi.nlm.nih.gov/8962629].
Экстраполяция данных, полученных при вскрытии после внезапной смерти, а также в результате биопсии у относительно здоровых пациентов, указывает на то, что полная потеря тимуса произойдет в возрасте 120 лет, а тимус перестанет создавать новые Т-клетки примерно в возрасте 105 лет [pubmed.ncbi.nlm.nih.gov/8962629].
Именно в тимусе Т-клетки наивные "обучаются" распознавать вирусы, с которыми они еще никогда не встречались. Это происходит путем "перетасовки" определенных регионов ДНК, благодаря которой создается гигантское разнообразие возможных вариантов Т-клеточных рецепторов. В результате такого огромного разнообразия Т-клеточных рецепторов наивных клеток иммунитета существует высокая вероятность того, что при проникновении в организм какого-либо нового вируса найдётся Т-клетка, рецепторы которой окажутся подходящими для того, чтобы его обезвредить [pubmed.ncbi.nlm.nih.gov/24510963].
После наступления полового созревания производство тимусом наивных Т-клеток быстро снижается. Далее на протяжении всей взрослой жизни активность тимуса остаётся на низком уровне. Созданное за детский период жизни разнообразие Т-клеточных рецепторов с какого-то возраста начинает сокращаться.
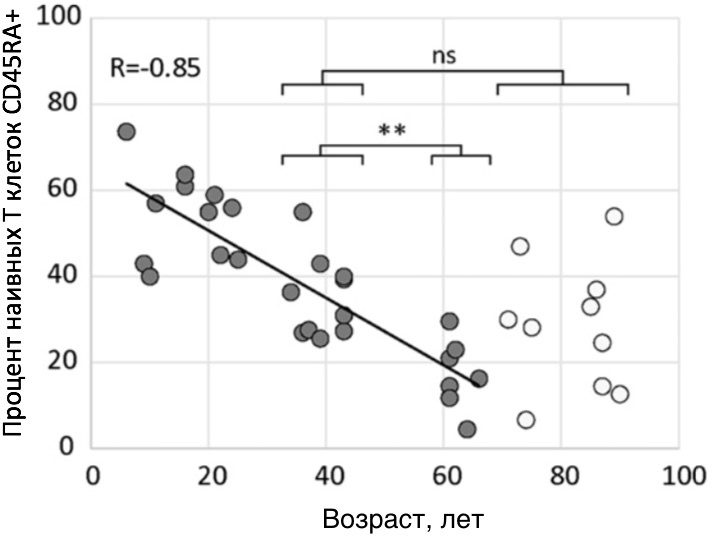 Рисунок 5. Снижение процента наивных Т клеток CD4+ иммунитета с возрастом.
Рисунок 5. Снижение процента наивных Т клеток CD4+ иммунитета с возрастом.
Доля наивных Т-клеток человека линейно уменьшается с возрастом. В детстве она составляет 50–80% от всего количества Т-клеток, но уменьшается на 0,75% каждый год. К 70 годам она составляет около 25% и ниже от первоначального изобилия [ncbi.nlm.nih.gov/pubmed/24510963]. Такое падение наблюдается до 70-летнего возраста. Однако у тех, кто живет дольше 70 лет, такого падения не наблюдается (рис.5). Люди возрастной группы 70+ уже, видимо, перешагнули определённый возрастной порог, пройдя в некотором смысле проверку на прочность. Их процент наивных Т-клеток и разнообразие Т-клеточных рецепторов значительно выше, чем у тех, кто, видимо, не пережил 70-летний барьер (рис. 5).
Количество наивных Т- клеток имеет положительную связь с их разнообразием Т -клеточных рецепторов, что положительно сказывается для защиты от вирусов, а также от онкологических заболеваний [ncbi.nlm.nih.gov/pubmed/24510963]. Примерно к 100-летнему возрасту абсолютное число наивных Т - клеток становится крайне низким [pubmed.ncbi.nlm.nih.gov/10779432].
Итак, наличие достаточного количества наивных Т-клеток и разнообразия их рецепторов необходимо для того, чтобы иммунная система постоянно реагировала на незнакомые вирусы. В то время, как это разнообразие снижается с возрастом [pubmed.ncbi.nlm.nih.gov/9786427] [pubmed.ncbi.nlm.nih.gov/12165524] [pubmed.ncbi.nlm.nih.gov/18562142].
Все иммунные клетки организма формируются в костном мозге от гемопоэтических стволовых клеток, которые могут оставаться молодыми, но стареют под воздействием стареющей стволовой ниши, что также сопровождается старением клеток врожденного и адаптивного иммунитета
Все иммунные клетки организма образуются в костном мозге от гемопоэтических стволовых клеток, которые дают начало либо миелоидно-ориентированным, либо лимфоидно-ориентированным предшественникам клеток [ashpublications.org/blood/article/125/17/2587/34094/Introduction-to-a-review-series-on-hematopoietic]. Однако гемопоэтические стволовые клетки стареют с возрастом.
Хорошая новость заключается в том, что гемопоэтические стволовые клетки совсем не обязаны стареть, а их заставляет стареть стволовая ниша. Ниша стволовых клеток относится к микросреде в определенном анатомическом месте (где находятся стволовые клетки), которая взаимодействует со стволовыми клетками, регулируя судьбу этих клеток. По мере старения стволовая ниша заставляет стареть и гемопоэтические стволовые клетки.
То, что гемопоэтические стволовые клетки могут жить значительно дольше, чем сам организм и не стареть, подтверждают исследования. Так мышиные гемопоэтические стволовые клетки способны давать начало новым клеткам, в том числе эритроцитам, в течение более 3000 дней, что превышает максимальную продолжительность жизни мышей в несколько раз. Это было установлено путем последовательной пересадки одних и тех же гемопоэтических стволовых клеток более молодым мышам-донорам [ncbi.nlm.nih.gov/pubmed/37377]. То есть молодой мышке с анемией пересадили стволовые клетки, убедились, что анемия прошла и потом, когда она состарилась, забрали те же самые стволовые клетки, и снова пересадили их молодой мышке. И так несколько раз. А ведь у каждого нового животного, была и новенькая стволовая ниша. Примечание: анемия — состояние, для которого характерно уменьшение количества эритроцитов в крови и снижение содержания гемоглобина в единице объема крови; гемоглобин — железосодержащий белок животных, обладающих кровообращением, способный связываться с кислородом, обеспечивая его перенос в ткани.
В костном мозге, в процессе своей специализации гемопоэтические стволовые клетки дают начало либо миелоидно ориентированным, либо лимфоидно ориентированным. Именно из от лимфоидно ориентированных происходят предшественники Т-клеток иммунитета. Но с возрастом гемопоэтические стволовые клетки все чаще дифференцируются в миелоидно ориентированные [ncbi.nlm.nih.gov/pubmed/22830639]. Интересное открытие заключается в том, что миелоидная или лимфоидная ориентация могут зависеть от возраста стволовой ниши, окружающей стволовые клетки. Например, молодые гемопоэтические стволовые клетки дифференцировались преимущественно в сторону миелоидного клона при трансплантации старым мышам [ncbi.nlm.nih.gov/pubmed/15827136] [ncbi.nlm.nih.gov/pubmed/23047952]. Напротив, трансплантация старых гемопоэтических стволовых клеток в молодые ниши приводит к уменьшению дифференцировки клеток в сторону миелоидно ориентированных [ncbi.nlm.nih.gov/pubmed/22289892].
Развитие В-лимфоцитов иммунитета критически зависит от ниши в костном мозге, так как В-лимфоциты дифференцируются от гемопоэтических стволовых клеток. В результате старения стволовой ниши, В-лимфоциты, которые созревают в костном мозге, утрачивают разнообразие своих рецепторов [ncbi.nlm.nih.gov/pubmed/25938781] [ncbi.nlm.nih.gov/pubmed/15314072]. Разнообразие рецепторов В-лимфоцитов является залогом того, что для новой инфекции найдутся специфичные В-лимфоциты, распознающие антигены, характерные для данного вредоносного агента. Более того, адипоциты (клетки жировой ткани), которые увеличиваются в стареющем костном мозге, по-видимому, подавляют образование новых В-клеток [ncbi.nlm.nih.gov/pubmed/23002443].
Натуральные киллеры - клетки врожденного иммунитета. Натуральные киллеры развиваются в костном мозге, а их количество и активность (токсичность для зараженных клеток) снижаются с возрастом [ncbi.nlm.nih.gov/pubmed/25009085]. Исследования показали, что причиной этому явлению может быть старение костного мозга [ncbi.nlm.nih.gov/pubmed/24058177] [ncbi.nlm.nih.gov/pubmed/25399821] [ncbi.nlm.nih.gov/pubmed/25677698].
Тимус - это специализированный первичный лимфоидный орган иммунной системы. Внутри тимуса созревают Т-лимфоциты иммунитета. Уменьшение размеров истинной ткани тимуса с возрастом приводит к уменьшению количества наивных Т-клеток иммунитета [ncbi.nlm.nih.gov/pubmed/15964201] [ncbi.nlm.nih.gov/pubmed/16717190], к увеличению количества Т-клеток памяти, уменьшению разнообразия Т-клеточных рецепторов, необходимых для эффективной реакции на незнакомые вирусы и раковые опухоли [ncbi.nlm.nih.gov/pubmed/17218073] [ncbi.nlm.nih.gov/pubmed/18332179], к снижению функциональной активности Т-лимфоцитов - к иммунному старению [ncbi.nlm.nih.gov/pubmed/16782020] [ncbi.nlm.nih.gov/pubmed/21436838]. Более того, возрастное уменьшение размеров истинной ткани тимуса вызывает потерю эффективности отбраковывания аутореактивных Т-лимфоцитов в тимусе, способных вызывать хроническое воспаление и аутоиммунные заболевания, при которых иммунитет атакует свой же организм [ncbi.nlm.nih.gov/pubmed/26318588].
Тимус - это орган иммунной системы, придающий Т-лимфоцитам иммунные свойства. Он важен для юного организма, иммунитет которого только учится распознавать вредоносные агенты. Однако для взрослого организма тимус уже не так важен. Удаление тимуса в раннем возрасте, когда иммунитет еще не сформировался, сокращает продолжительность жизни. Удаление же тимуса в возрасте 40-60 лет практически не влияет на ожидаемую продолжительность жизни
Тимус растет до десятилетнего возраста ребенка, а после совершеннолетия – уменьшается.
Некоторые блогеры делают громкие утверждения, что "Как же тимус может помочь остановить старение организма?" [econet.ru/articles/timus-kak-ostanovit-starenie?]. В общем тимус сегодня на хайпе.
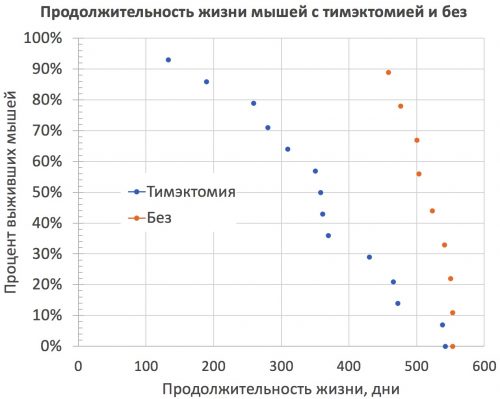 Основная цель тимуса – придать Т-лимфоцитам иммунные свойства. Это нужно, когда человек растет, а иммунитет только формируется. Однако для взрослых это уже не так актуально [pubmed.ncbi.nlm.nih.gov/870559]. А что будет, если у животного или у человека вообще удалить тимус - сделать тимэктомию? Сократит ли это жизнь?
Основная цель тимуса – придать Т-лимфоцитам иммунные свойства. Это нужно, когда человек растет, а иммунитет только формируется. Однако для взрослых это уже не так актуально [pubmed.ncbi.nlm.nih.gov/870559]. А что будет, если у животного или у человека вообще удалить тимус - сделать тимэктомию? Сократит ли это жизнь?
Рисунок 6. Такой эксперимент был поставлен еще в 1971 году, как показано на рисунке [pubmed.ncbi.nlm.nih.gov/5120098] [10.1097/00007890-197112000-00021] [ur.booksc.me/book/59137476/a7dc6f]. В результате изменилась средняя продолжительность жизни мышей. Но максимальная продолжительность жизни значимо не изменилась. Последняя живая мышь с удаленным тимусом умерла в возрасте 542 дней, а последняя мышь с тимусом умерла в возрасте 553 дней. Что практически одно и тоже, учитывая размер выборки. Это говорит о том, что тимус не влияет на скорость старения, но влияет на уязвимость к вирусам и опухолям, может влиять на продолжительность жизни.
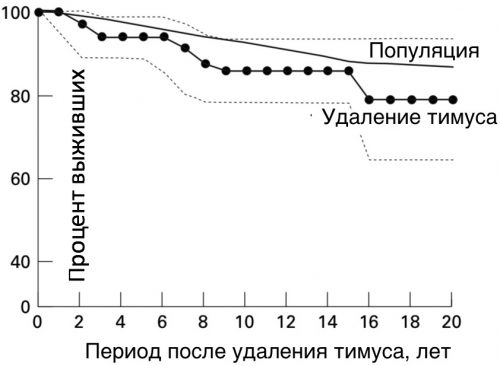 Миастения гравис - аутоиммунное нервно-мышечное заболевание, характеризующееся патологически быстрой утомляемостью поперечнополосатых мышц.
Миастения гравис - аутоиммунное нервно-мышечное заболевание, характеризующееся патологически быстрой утомляемостью поперечнополосатых мышц.
Рисунок 7. При миастении у пациентов часто удаляют тимус (он причина аутоиммунных заболеваний в этих случаях), и пациенты живут достаточно долго вовсе без тимуса [pubmed.ncbi.nlm.nih.gov/9436732] - почти также, как и здоровые люди в популяции.
Дело в том, что, как мы увидели из эксперимента с мышами, животным удаляли тимус в довольно раннем возрасте, когда иммунитет еще не сформировался. Совсем иное дело, когда тимус удаляют взрослым людям в возрасте 40-60 лет, когда его роль уже не такая значительная, как в детстве. И вот у пациентов с миастенией удаление тимуса практически не влияет на ожидаемую продолжительность жизни.
Количество общих, либо наивных T-клеток и T-клеток памяти, CD4+ или CD8+ Т-клеток оценивали в крови 288 здоровых людей в возрасте от 20 до 107 лет. Абсолютное количество общих и наивных Т-клеток прогрессивно снижалось с возрастом, как в популяциях CD4+, так и в популяциях CD8+ Т-клеток. Количество наивных T-клеток памяти снижалось, а количество Т-клеток памяти CD4+, но не CD8+ значительно увеличивалось с возрастом. Только абсолютное количество Т–клеток памяти CD8+ у женщин после поправки на возраст коррелировало с увеличением смертности, но вклад этого изменения в изменение риска смертности был очень маленьким, на уровне 0.7%, что эквивалентно потере около 1 месяца жизни [pubmed.ncbi.nlm.nih.gov/29375577]. Вероятно, поэтому утрата истинной ткани тимуса, в котором Т-лимфоциты приобретают иммунные свойства, не так критична для выживания в пожилом возрасте, в современном мире при хорошей гигиене. Тем более, что уменьшение размеров истинной ткани тимуса с возрастом может быть необходимым явлением для снижения потребления энергии пожилого человека с целью выживания [pubmed.ncbi.nlm.nih.gov/29375577].
Хроническая вирусная инфекция может привести к необратимому повреждению иммунной системы, что выражается в снижении иммунной защиты от вредоносных агентов и раковых опухолей
Длительный хронический вирусный гепатит (воспалительное заболевание печени) может привести к необратимому повреждению иммунной системы человека, что выражается в снижении иммунной защиты от рака печени и повышении риска этого заболевания. Противовирусное лечение хотя и подавляет репликацию (образование вирусов в процессе заражения в клетках) вируса, но редко приводит к ликвидации вируса. В отличие от вируса гепатита B, хроническое заболевание, вызванное вирусом гепатита C можно вылечить с помощью противовирусной терапии. Поэтому модель, изучающая состояние иммунной системы, после эффективного лечения гепатита, вызванного вирусом гепатита C, может показать, способна ли восстановиться иммунная система человека после избавления от вируса. К сожалению, очистка от вируса гепатита C хотя и приводит к снижению уровня маркеров активации и истощения Т-клеток иммунитета, к восстановлению функции натуральных киллеров иммунитета, но функция Т-клеток и разнообразие натуральных киллеров восстанавливаются лишь частично даже спустя годы [pubmed.ncbi.nlm.nih.gov/33133084].
Постоянная инфекция различными вирусами герпеса и другими паразитами способствует потере иммунитета и преждевременному истощению Т-клеток [pubmed.ncbi.nlm.nih.gov/19789136].
«Воспалительное старение» может быть состоянием адаптационной повышенной готовности иммунитета для быстрого ответа на угрозу от вредоносных агентов в условиях, когда адаптивная иммунная система терпит неудачу из-за старения, а следовательно, медикаментозное подавление "воспалительного старения" без восстановления функции адаптивного иммунитета может создавать угрозу выживания
Клаудио Франчески выдвинул концепцию хронического воспалительного состояния, возникающего по мере старения, называемого «воспалительным старением» [pubmed.ncbi.nlm.nih.gov/20200405]. Но эта концепция не имела ответа на 2 вопроса:
- Является ли «воспалительное старение» причиной, ускоряющей старение, либо является механизмом адаптации к старению.
- Должны ли мы пытаться вмешиваться, чтобы снижать уровень "воспалительного старения"?
«Воспалительное старение» и снижение функции адаптивного иммунитета прогрессируют параллельно - образуют порочный круг. Повышенная выработка медиаторов воспаления, характерных для "воспалительного старения", способствует снижению адаптивного иммунного ответа. Напротив, снижение адаптивного иммунного ответа усиливает стимуляцию врожденного иммунного ответа, что проявляется, как «воспалительное старение - необходимая адаптация для защиты организма от инфекций в условиях, когда адаптивный иммунитет терпит неудачу. В результате, если мы попытаемся вмешаться и с помощью лекарств "грубо" подавить «воспалительное старение" пожилого человека, это может создать угрозу для его жизни, в условиях, когда адаптивный иммунитет не работает эффективно. Отсюда следует вопрос: какие иммунные изменения у пожилых людей могут быть полезными? Например, уменьшение размеров истинной ткани тимуса с возрастом может быть необходимым явлением для снижения потребления энергии с целью выживания. А увеличение доли регуляторных B-клеток иммунитета, наблюдаемое у пожилых людей, может предотвратить аутоиммунную атаку собственных тканей организма. «Воспалительное старение» может быть состоянием повышенной готовности для быстрого обезвреживания вирусов и потенциально продлевать жизнь пожилых людей, если уровень воспаления оптимален - не высокий и не слишком низкий [pubmed.ncbi.nlm.nih.gov/29375577].
Если предположить, что «воспалительное старение» является адаптацией, чтобы обеспечить наилучшую возможную защиту от вредоносных агентов, когда адаптивная иммунная система терпит неудачу, то предлагаемый в настоящее время подход к омоложению иммунитета без учета функции адаптивного иммунитета, вероятно, будет вреден для пожилого организма. Поэтому правильно будет - не снижать уровень воспаления, а улучшать функцию адаптивного иммунитета, тогда и «воспалительное старение» будет не актуально, а снижение уровня воспаления будет полезным. Именно так работает здоровый образ жизни.
Чтобы на основании анализов иммунных клеток в крови предсказывать, как то или иное воздействие (диеты, лекарства и др.) повлияло на риски смертности, нужно на основании машинного обучения создавать модели, учитывающие возраст, год рождения, пол, генетику, окружающую среду, питание, микробиоту, пожизненное воздействие вредоносных агентов (вирусов, бактерий и др.), доступ к медицине, эпидемии и войны
Доля наивных Т-клеток человека линейно уменьшается с возрастом [ncbi.nlm.nih.gov/pubmed/24510963]. Такое падение наблюдается до 70-летнего возраста. Однако у тех, кто живет дольше 70 лет, такого падения не наблюдается. Люди возрастной группы 70+ уже, видимо, перешагнули определённый возрастной порог, пройдя в некотором смысле проверку на прочность. Их процент наивных Т-клеток и разнообразие Т-клеточных рецепторов значительно выше, чем у тех, кто, видимо, не пережил 70-летний барьер. Количество наивных Т- клеток имеет положительную связь с разнообразием Т-клеточных рецепторов [ncbi.nlm.nih.gov/pubmed/24510963], а наличие достаточного количества наивных Т-клеток и разнообразия их рецепторов необходимо для того, чтобы иммунная система постоянно реагировала на незнакомые вирусы. В то время, как это разнообразие снижается с возрастом [pubmed.ncbi.nlm.nih.gov/9786427] [pubmed.ncbi.nlm.nih.gov/12165524] [pubmed.ncbi.nlm.nih.gov/18562142]. Определить соотношение наивных Т-клеток к Т-клеткам памяти можно с помощью анализа крови "Соотношение наивных и клеток памяти (наивные CD4 лимфоциты/клетки памяти или CD4/45RO, CD4/45RA)" в медицинских офисах ДНКОМ. Если указанное соотношение не менее единицы, то есть количество наивных Т-клеток не меньше, чем количество Т-клеток памяти, то пациент имеет хороший Т-клеточный иммунитет по данному параметру.
Для выявления маркеров старения иммунитета были проанализированы иммунограммы 276 долгожителей в возрасте 90–104 лет. У людей от 92 и старше, имеющих дефицит Т-клеток CD8+, увеличивались случаи старческих заболеваний мозга (нейродегенеративных заболеваний), а также заболеваний мышц, костей и желудочно-кишечного тракта. Этот факт может намекать на то, что уровень Т-клеток CD8+ может быть маркеров старения иммунитета [pubmed.ncbi.nlm.nih.gov/25826990].
Хотя параметры иммунитета, такие как уровень Т-клеток CD8+ или отношение CD4/45RO к CD4/45RA, и связаны с рисками у пожилых людей, но остается вопрос, может ли оптимизация этих параметров диетами, либо лекарствами, увеличить продолжительность жизни.
Найти маркеры старения иммунитета, предсказывающие старение иммунитета в контексте продолжительности жизни, чтобы их оптимизация приводила к снижению риска смертности - сложная задача для будущих исследований. Простой набор параметров иммунитета, вероятно, никогда не будет применим в качестве общего биомаркера влияния иммунного старения на выживаемость. У разных людей разные значения параметров функции иммунной системы будут приводить к различным результатам. Иными словами, что полезно для одних, будет вредно для других. Чтобы на основании анализов иммунных клеток в крови предсказывать, как то или иное воздействие (диеты, лекарства и др.) повлияло на продолжительность жизни человека, нужно учитывать возраст, год рождения, пол, генетику, окружающую среду, питание, микробиоту, пожизненное воздействие вредоносных агентов (вирусов, бактерий и др.), особенно цитомегаловирусов, доступ к медицине, эпидемии, войны [pubmed.ncbi.nlm.nih.gov/29185165]. Поэтому, чтобы предсказывать влияние параметров иммунитета на продолжительность жизни с целью их оптимизации для долголетия, нужно создавать модели, учитывающие все эти факторы.
Как строятся модели на основании машинного обучения? Например, после применения машинного обучения была построена модель, предсказывающая возраст иммунитета, которая получила название "часы иммунитета". Качество модели по показателю R2 достигло 80,3%, а стандартная ошибки оценки - 4,74 года. Возраст людей для валидации модели варьировался от 32 до 84 лет, со средним возрастом 54,60 ± 10,70 [pubmed.ncbi.nlm.nih.gov/33979432].
Формула модели: возраст иммунитета = 93,943 - 0,23 * Активность натуральных киллеров - 0,001 * PHA-стимулированная лимфопролиферация - 0,022 * Хемотаксис нейтрофилов - 0,02 * Фагоцитарный индекс нейтрофилов - 0,019 * Хемотаксис лимфоцитов
Примечание: phytohemagglutinin (PHA); хемотаксис – процесс активного движения к химическим раздражителям; активность (токсичность для зараженных клеток) измеряется в литических единицах; фагоцитарный индекс – показатель способности поглощать частицы латекса.
Провести такое обследование, чтобы рассчитать возраст иммунитета не представляется возможным в обычном медицинском центре. Но эту модель могут взять на вооружение медицинские центры. Также это пример того, что специалисты по машинному обучению или специалисты по Data Science в медицине потенциально могут создать другие "часы иммунитета" основанные на тех параметрах организма, которые являются общедоступными для анализа пациентов медицинских центрах, а также дополнительно на перечисленных выше факторах
Введение интерлейкина 7-го типа и фактора роста кератиноцитов, трансплантация эпителиальных клеток тимуса, использование внеклеточной матрицы в качестве каркаса для клеток с целью регенерации тимуса, излечение аутоиммунных заболеваний с помощью анти-CD19 CAR-T-клеточной терапии, а также пересадка костного мозга - перспективные методы омоложения иммунной системы
Лечение 211 пожилых добровольцев в возрасте старше 65 лет в течение шести недель эверолимусом в дозе 0,5 мг ежедневно, либо 5 мг еженедельно (обе дозы оказались эффективны) снижало процент CD4 и CD8 Т-лимфоцитов, экспрессирующих рецептор запрограммированной смерти-1 (PD-1), который подавляет передачу сигналов Т-клетками и более высоко экспрессируется с возрастом, а также улучшило реакцию на вакцинацию против гриппа 20%, если вакцинация выполнялась через 2 недели после окончания курса лечения эверолимусом [pubmed.ncbi.nlm.nih.gov/25540326].
Введение рекомбинантного интерлейкина 7-го типа (IL-7) пожилым макакам-резусам, не увеличило значительно функцию тимуса, но привело к двукратному росту количества Т-клеток, а также к росту разнообразия Т-клеточных рецепторов [pubmed.ncbi.nlm.nih.gov/26416281]. А после вакцинации инактивированным штаммом гриппа, у половины животных, после введения интерлейкина 7-го типа, антитела увеличились более чем в 8 раз после первой дозы вакцины, что говорит о том, что интерлейкин 7-го типа повысил эффективность вакцинации у старых животных [ncbi.nlm.nih.gov/pubmed/17378748].
CCR9 (C-C-рецептор хемокина 9) — продукт гена CCR9. Посредством слияния ДНК CCR9 и IL-7 получили плазмиду. N-концевой внеклеточный домен CCR9 объединили с интерлейкином 7-го типа, чтобы нацелить этот белок на тимус и уменьшить неблагоприятные системные эффекты повышенного интерлейкина 7-го типа для других частей организма, так как благодаря CCR9, действие интерлейкина 7-го типа сосредоточивалось на тимусе. В результате такой терапии у мышей произошло восстановление архитектуры тимуса и увеличилось количество Т-клеток, аналогично молодым животным. Старые мыши, получавшие такую терапию, демонстрировали улучшение функции CD8 T-клеток и снижение вирусной нагрузки после заражения вирусом гриппа по сравнению с теми мышами, которые не получили такое лечение [pubmed.ncbi.nlm.nih.gov/16148161].
Фактор роста кератиноцитов (KGF), является мощным фактором роста клеток эпителия в тимусе. Сегодня в медицине KGF одобрен для лечения мукозита, вызванного токсичными химиотерапевтическими средствами, используемыми для предотвращения отторжения при трансплантации костного мозга у людей, и имеет торговое наименование - палифермин. У мышей, после подкожного введения KGF в течение 3-х дней, увеличивались количество наивных Т-клеток иммунитета CD4+, выработка антител, увеличивалась скорость деления клеток эпителия в тимусе в 4 раза (до уровня молодых мышей) [ncbi.nlm.nih.gov/pubmed/17138819]. Однако исследования на людях противоречивы, что требует дальнейших клинических испытаний [sciencedirect.com/topics/biochemistry-genetics-and-molecular-biology/keratinocyte-growth-factor].
Грелин представляет собой пептидный гормон, уровень которого повышается в желудке в ответ на голод или дефицит энергии, стимулирует чувство голода. Введение грелина 14-месячным мышам значительно улучшило возрастные изменения в тимусе, а также увеличило разнообразие Т-клеточных рецепторов [ncbi.nlm.nih.gov/pubmed/17823656]. Вероятно, поэтому курсы голоданий, о которых мы поговорим позже, могут восстанавливать некоторые параметры иммунитета.
Внутримышечная трансплантация эпителиальных клеток тимуса, выделенных из растущих тимусов, либо полученных из плюрипотентных стволовых клеток, приводит к росту тимуса у мышей и к увеличению количества Т-клеток [pubmed.ncbi.nlm.nih.gov/25870244].
При старении увеличивается уровень аутоиммунных заболеваний. Современные технологии позволят в будущем успешно решать эту проблему. Например, уже сегодня группе немецких ученых из Университета Фридриха Александра Эрланген-Нюрнберг удалось добиться ремиссии красной волчанки у 5 пациентов с помощью анти-CD19 CAR-T-клеточной терапии. Нарушенная активация В-клеток играет ключевую роль в системной красной волчанке (СКВ). Выделили из организма Т-клетки (лейкофарез). С помощью генной технологии (внедрение самоинактивирующегося лентивирусного вектора) изменили Т-клетки так, чтобы они могли атаковать собственные В-клетки пациента. Ввели полученные Т-клетки обратно в кровь. Созданные химерные Т-клетки находили B-клетки с нарушенной активацией, имеющие рецепторы антигена и убивали их вводя им токсин.
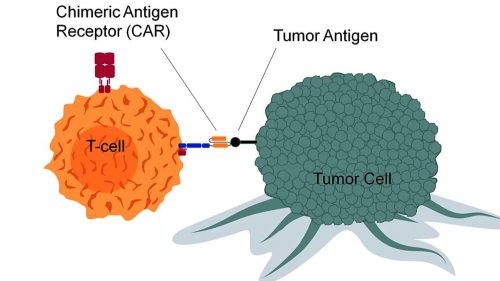 Рисунок. Рецептор Т-клетки захватывает рецептор антигена на раковой клетке. Аналогично Т-клетки могут захватывать рецепторы антигена на любых других клетках.
Рисунок. Рецептор Т-клетки захватывает рецептор антигена на раковой клетке. Аналогично Т-клетки могут захватывать рецепторы антигена на любых других клетках.
Наблюдалось глубокое истощение B-клеток, улучшение клинических симптомов. 8 месячная ремиссия СКВ в соответствии с критериями DORIS была достигнута у всех пяти пациентов через 3 месяца. Средний балл индекса активности СКВ через 3 месяца составил 0. Вновь появляющиеся В-клетки были наивными с нормальными рецепторами [pubmed.ncbi.nlm.nih.gov/36109639].
Тем не менее, внутримышечная трансплантация эпителиальных клеток тимуса малоэффективна. Дело в том, что основная причина возрастной инволюции тимуса обусловлена главным образом изменениями в строме тимуса, которая в процессе старения теряет свои физические свойства, а не в старении лишь эпителиальных клеток тимуса [pubmed.ncbi.nlm.nih.gov/27529161]. Поэтому в настоящее время разрабатываются новые методы с использованием внеклеточной матрицы в качестве каркаса для клеток с целью регенерации тимуса [pubmed.ncbi.nlm.nih.gov/34306981].
Почему модели мышей для поиска терапий восстановления иммунитета чаще всего не работают на людях? Так, диабет 1-го типа - это аутоиммунное заболевание, которое у мышей было предотвращено или обращено вспять сотни раз, но на сегодняшний день у людей эта болезнь до сих пор не лечится. Иммунология, если она продолжит фокусироваться на мышах, а не на людях, может испытать глубокий кризис, стать интересной биологией, но не иметь отношения к медицине. Вероятно, существуют новые иммунологические механизмы у долгоживущих, менее плодовитых млекопитающих, таких как люди, поскольку они должны оставаться здоровыми гораздо дольше, чем короткоживущие грызуны, чтобы вид выжил, порой приобретая аутоиммунные заболевания в качестве "жертвы" для усиления иммунной реакции, чтобы не умереть от инфекций. Люди обладают многими характеристиками — генетическим разнообразием и широким воздействием микробов окружающей среды, которых нет у инбредных моделей мышей. Люди также подвергаются множеству вмешательств: вакцины и постоянно растущий список лекарств [pubmed.ncbi.nlm.nih.gov/29490162].
Компьютерная томография ткани тимуса показала, что замена функциональной ткани тимуса на жировую положительно коррелирует с повышенным индексом массы тела в следствие ожирения и с курением [pubmed.ncbi.nlm.nih.gov/25925358]. С другой стороны, у пожилых людей, которые большую часть своей взрослой жизни занимались ездой на велосипеде, по сравнению с их менее активными коллегами, наблюдалось снижение возрастной потери функции тимуса, большее количество наивных Т-клеток иммунитета, увеличение доли регуляторных B-клеток, важных для предотвращения аутоиммунных атак собственных тканей организма, снижение маркеров воспаления, повышение уровня интерлейкина 7 и 15-го типов в сыворотке крови, что может способствовать сохранению функции тимуса с возрастом [pubmed.ncbi.nlm.nih.gov/29517845] [pubmed.ncbi.nlm.nih.gov/31175337]. Вывод: чтобы не ускорять старение иммунитета, нужно регулярно заниматься аэробными физическими упражнениями (бег, плавание, езда на велосипеде и т.п.) и избегать набора лишней жировой массы тела, а также и ее дефицита.
4-5 ежемесячных циклов голоданий по 4 дня подряд могут увеличивать долю наивных Т-клеток иммунитета у людей, что связано с ростом вероятности, что при проникновении в организм какого-либо нового вируса найдётся Т-клетка, рецепторы которой окажутся подходящими для того, чтобы его обезвредить
В 2020 году началась пандемия Covid-19. Около 81% людей с COVID-19 имели легкие симптомы и не нуждались в госпитализации. Почему, несмотря на опасность вызывающего Covid-19 вируса, многие люди переносят болезнь, как легкую простуду, либо вообще не болеют? Вероятно, их защищает адаптивный иммунитет. Наивные Т-клетки адаптивного иммунитета "обучаются" распознавать вирусы, с которыми они еще никогда не встречались. Это происходит путем "перетасовки", благодаря которой создается гигантское разнообразие возможных вариантов Т-клеточных рецепторов. В результате такого огромного разнообразия Т-клеточных рецепторов наивных клеток иммунитета существует высокая вероятность того, что при проникновении в организм какого-либо нового вируса найдётся Т-клетка, рецепторы которой окажутся подходящими для того, чтобы его обезвредить [pubmed.ncbi.nlm.nih.gov/24510963].
Предшественники Т-клеток иммунитета созревают в костном мозге из гемопоэтических стволовых клеток, а затем попадают в тимус. Но еще в костном мозге, в процессе своей специализации гемопоэтические стволовые клетки превращаются либо в миелоидно ориентированные, либо в лимфоидно ориентированные. Именно из лимфоидно ориентированных создаются предшественники Т-клеток иммунитета. Но с возрастом гемопоэтические стволовые клетки становятся все чаще миелоидно ориентированными. В результате создается все меньше Т-клеток предшественников. Возрастное уменьшение размеров истинной ткани тимуса и недостаточность гемопоэтических стволовых клеток играют важную роль в старении иммунитета [ncbi.nlm.nih.gov/pubmed/22830639].
В экспериментах на мышах было показано, что 4-8 циклов 3-х дневных голоданий каждые 2 недели восстанавливали соотношение миелоидных/лимфоидных гемопоэтических стволовых клеток [ncbi.nlm.nih.gov/pubmed/24905167]. В пилотном клиническом исследовании на людях короткие циклы голода также восстанавливали функцию гемопоэтических стволовых клеток [pubmed.ncbi.nlm.nih.gov/20157582]. Грелин представляет собой пептидный гормон, уровень которого повышается в желудке в ответ на голод. Введение грелина 14-месячным мышам значительно улучшило возрастные изменения в тимусе, а также увеличило разнообразие Т-клеточных рецепторов [ncbi.nlm.nih.gov/pubmed/17823656].
Наш проект NestarenieRU [nestarenie.ru/immunity.html] решил организовать пилотный эксперимент, целью которого было установить, можно ли с помощью коротких циклов голода, либо диеты, имитирующей голодания, восстановить соотношение наивных Т-клеток иммунитета к Т-клеткам памяти, которое уменьшается с возрастом [ncbi.nlm.nih.gov/pubmed/24510963], что связано с разнообразием Т-лимфоцитов, а следовательно, со способностью адаптивного иммунитета противостоять неизвестным вирусам. По условиях эксперимента перед циклами голоданий или перед циклами имитации голода, участники сдавали кровь на анализ в медицинских офисах ДНКОМ. Анализ крови назывался "Соотношение наивных и клеток памяти (наивные CD4 лимфоциты/клетки памяти или CD4/45RO, CD4/45RA). Затем ежемесячно с 1 по 4 числа (4 дня подряд) в течение 4-5 месяцев участники либо голодали, либо употребляли не более 500-700 калорий в сутки (всего было 4-5 циклов 4-дневного голода). Снижение калорийности рациона до 500-700 в сутки имитирует голодание у животных [ncbi.nlm.nih.gov/pubmed/27411588] и у людей [ncbi.nlm.nih.gov/pubmed/26094889]. А также имеет такой же механизм влияния на омоложение гемопоэтических стволовых клеток, как и само голодание - через снижение уровня инсулин подобного фактора роста 1-го типа (белок из семейства инсулиноподобных факторов роста по структуре и функциям похожий на инсулин) по время голода.
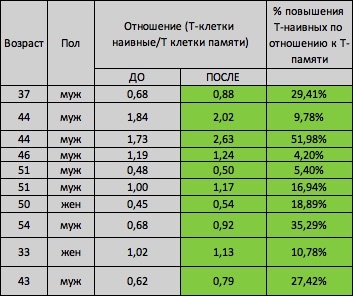
После снижения инсулин подобного фактора роста 1-го типа, уже после окончания голодания (в период употребления пищи) активизируется фактор транскрипции (белок, влияющий на то, как будут работать гены) FOXO1, который и обуславливает омоложение гемопоэтических стволовых клеток [ncbi.nlm.nih.gov/pubmed/25072352]. Через 4-5 месяцев, но не ранее, чем через 7 дней после последнего цикла голодания или цикла снижения калорийности рациона до 500-700 в сутки, анализ крови повторялся.
Рисунок 8. В результате у всех без исключения участников эксперимента, процент наивных Т-клеток иммунитета выросло на 4,2 - 51,98% (в среднем на 21%).
Влияние экстремального закаливания организма холодом на иммунитет не изучено и потенциально может повысить риск умереть
Человек относиться к млекопитающим. У млекопитающих температура тела примерно постоянная. Рассмотрим на примере мышей, которые также являются млекопитающими. Стандартная температура поверхности тела лабораторных мышей в исследовательских учреждениях немного «прохладная» колеблется в пределах 20-26 °C. Это ниже температуры, комфортной для этих животных, которая составляет 30-31 °С. К сожалению, мыши, проживающие в таких прохладных условиях, имеют хронический холодовой стресс, необходимый для поддержания постоянной температуры тела, который вызывает подавление противоопухолевого иммунного ответа и способствует росту раковых опухолей и их метастазированию [ncbi.nlm.nih.gov/pubmed/24248371]. Как проживание в прохладном помещении отразится на продолжительности жизни людей и на рисках рака, пока непонятно. Т-клетки иммунитета мышей более эффективны в борьбе с раком в теплой среде, нежели в прохладной [pnas.org/content/110/50/20176]. К тому же при воздействии тепла снижается уровень «белков холодового шока», а именно RBM3 и CIRBP, что снижает выживание раковых опухолей [ncbi.nlm.nih.gov/pubmed/19277990], поэтому лучше избегать проживания в постоянно прохладном помещении и чрезмерных закаливаний холодом [pubmed.ncbi.nlm.nih.gov/25066924] [pnas.org/content/110/50/20176] [nature.com/articles/ncomms7426].
Не существует доказательств эффективности добавок цинка и витамина D для снижения риска простудиться, заболеть, для сокращения продолжительности заболевания, а также для снижения симптомов аутоиммунных заболеваний
Многие бездоказательно утверждают, что будто витамин D укрепляет иммунитет. Однако, терапия витамином D в высоких дозах (100 000 МЕ 1 раз в 3 месяца) не снижала риск пневмонии у грудных детей [ncbi.nlm.nih.gov/pubmed/22494826] и не ускоряла выздоровление при инфекциях нижних дыхательных путей [ncbi.nlm.nih.gov/pubmed/29072165]. Лечение витамином D3 1000 МЕ/сут в рандомизированном контролируемом исследовании с участием 2259 человек (45–75 лет) не снизило частоту или продолжительность инфекционных заболеваний верхних дыхательных путей у взрослых с исходным уровнем 25-гидроксивитамина D ≥12 нг/мл в сыворотке крови [ncbi.nlm.nih.gov/pubmed/24014734]. У многих, кто пил витамин D для профилактики простудных заболеваний, не вызывает сомнения, что витамин D эффективен. «Что тут рассуждать? Ведь и так все понятно. Как стал пить витамин D, болеть ОРВИ стал реже». Нашему мозгу свойственны иллюзии понятности. Нам всегда все понятно и достаточно той информации, которую мы получили, чтобы сложить свое мнение. И это проблема.
На жалобу пациента о частых простудах, врач предлагает хорошо высыпаться и вести здоровый образ жизни. Пациент сомневается в компетенции врача и просит какое-то лекарство. Врач предлагает сходить в аптеку за витамином D для укрепления иммунитета. Но добавляет, что витамин D не будет работать на все 100%, если пациент не будет высыпаться. И вот уже довольный пациент бежит в аптеку с обещанием, что сегодня ляжет спать вовремя. Теперь он реже простужается и всем рассказывает про свой опыт. Эксперименты показали, что люди, которые имели худшее качество сна и меньше спали имели в разы больше риск заболеть, когда их инфицировали вирусом через назальные капли [ncbi.nlm.nih.gov/pubmed/19139325]. Помог ли пациенту витамин D, или хороший сон?
В результате рандомизированного контролируемого исследование был сделан вывод о том, что рассасывание леденцов с ацетатом цинка не сокращает срок выздоровления при простудах [bmjopen.bmj.com/content/10/1/e031662].
Псориаз — хроническое неинфекционное заболевание, дерматоз, поражающий в основном кожу. В настоящее время предполагается аутоиммунная природа этого заболевания. Псориаз имеет волнообразное течение с периодами стихания и обострения. Далеко не все люди это понимают и думают, что такие периоды стихания и обострения происходят из-за того, что они псориаз лечат какими-то лекарствами, травками. Это свойство нашего восприятия осознанно или неосознанно используют, возможно, недобросовестные медицинские работники, а также недобросовестные исследователи, которые делают выводы об эффективности лечения псориаза экстремально большими дозами витамина D на основании лишь того, что пациенты пили высокие дозы витамина D, и обострение уменьшилось [ncbi.nlm.nih.gov/pubmed/24494059]. Хотя на самом деле лечение совпало с естественным спадом обострения болезни. Для того, чтобы доказать, что обострение псориаза стихло из-за высоких доз витамина D, а не потому, что волна заболевания сама по себе пошла на спад до следующей волны, нужно в исследованиях использовать три экспериментальные группы. Одну группу лечить высокими дозами витамина D, вторую группу нужно лечить обычными дозами витамина D (400-1000 МЕ в сутки), а третью группу лечить плацебо (пустышкой). Но во всех трех группах исследуемые пациенты должны думать, что их лечат одинаково. Если обострение псориаза стихнет только в группе с высокими дозами витамина D, а в других группах симптомы псориаза останутся прежними, то можно говорить об эффективности. Но таких доказательств нет. Поэтому систематический обзор, опубликованный в 2019 году исследователями Университета Цинциннати, не находит доказательств эффективности высоких доз витамина D3 для лечения псориаза [ncbi.nlm.nih.gov/pubmed/31100992].
Иммуномодуляторы не входят ни в один международный стандарт лечения или профилактики простудных заболеваний из-за отсутствия доказательств эффективности
На российском рынке представлено около сотни иммуномодуляторов, разработанных внутри страны и практически не использующихся за пределами СНГ. В России эта группа веществ имеет значительные объёмы продаж, уступающие лишь антибиотикам и онкопрепаратам, при этом ряд препаратов, позиционируемых производителями в качестве иммуномодуляторов, часто прописываются врачами детям для лечения и профилактики простуды, в то время как иммуномодуляторы не входят ни в один международный стандарт лечения или профилактики ОРВИ или ОРЗ, плохо исследованы, а доказательства их эффективности и безопасности отсутствуют. В лучшем случае при простуде подобные препараты никак не повлияют на здоровье.
Рассмотрим пример. Объёмы продаж российского противовирусного препарата иммуномодулятора, созданного на основе полимеров хлопка, оценивается более чем в 2,5 млрд рублей [kommersant.ru/doc/2369403]. Он неоднократно включался в «Перечень жизненно необходимых и важнейших лекарственных препаратов», в частности в период с 2010 по 2015 годы [cdnimg.rg.ru/pril/article/108/92/12/u8akRanvTl4.pdf]. По сообщениям СМИ, вхождение в этот перечень с одной стороны, ограничивает максимальную стоимость препарата [vedomosti.ru/business/articles/2013/04/22/arbidol_bolshe_ne_pervyj], но с другой стороны, упрощает процедуру закупок и позволяет увеличить объём продаж. По данным представителей Формулярного комитета РАМН и ОСДМ (Общество специалистов доказательной медицины), эффективность препарата не доказана [rsci.ru/science_news/231270.php] [versia.ru/desyatki-milliardov-rublej-na-lekarstva-ot-prostudy-i-grippa-pustaya-trata-lichnyx-i-gosudarstvennyx-sredstv] [1tv.ru/news/2010-11-21/133538-v_rossiyskih_aptekah_prodayotsya_mnogo_lekarstv_effektivnost_kotoryh_ne_dokazana]. По состоянию на январь 2019 года рандомизированных двойных слепых плацебо-контролируемых исследований препарата не проводилось. А вместо этого имеются лишь материалы коллоквиума в журнале «Лечащий врач» [svoboda.org/a/24790122.html] [lvrach.ru/2009/10/10861672]. Коллоквиум – это научное собрание, целью которого является слушание и обсуждение доклада, претендующего на самостоятельное исследование. По европейским, американским медицинским стандартам и законодательству, а также по стандартам доказательной медицины данный препарат не может быть использован в медицинской практике. По состоянию на 2019 год препарат не упоминается в международной анатомо-терапевтической классификации (АТC) [whocc.no/atc_ddd_index]. Агрессивная маркетинговая политика включает также рассылку материалов, подписанных руководством предприятия-производителя, в которых содержатся угрозы преследовать в суде любого, кто публично выскажет сомнение в эффективности препарата [klnran.ru/wp-content/uploads/2015/12/BVZN_16.pdf#page=55]. По этой причине в данном примере название этого препарата мы опустим.
Повышение уровня гормонов стресса в результате воздействия хронического стресса увеличивает риск заболеть инфекционными заболеваниями
Снижайте уровень стресса. У наблюдаемых детей за две недели до обнаружения стрептококка и инфекций верхних дыхательных путей, число тревожных событий в семье увеличилось в 4 раза [ncbi.nlm.nih.gov/pubmed/6446472]. Стресс повышает гормоны стресса. Например, хроническая активация адренергических рецепторов адреналином ухудшает функцию иммунитета [ncbi.nlm.nih.gov/pubmed/8394164] [ncbi.nlm.nih.gov/pubmed/1319854].
Люди среднего и пожилого возраста, которые регулярно занимаются аэробными физическими упражнениями средней интенсивности, менее подвержены инфекциям, имеют лучшую реакцию на вакцинацию, повышенную способность наивных Т-клеток к делению и мобилизации, обладают повышенной способностью нейтрофилов к поглощению вредоносных агентов, большей цитотоксической активностью натуральных киллеров иммунитета, лучшей иммунной защитой от раковых опухолей
В результате старения ухудшается функция иммунитета, что сопровождается снижением мобилизации Т-клеток иммунитета. Регулярные аэробные физические упражнения снижают количество стареющих Т-лимфоцитов у пожилых людей, и даже одна аэробная тренировка может усилить мобилизацию наивных Т-клеток и Т-клеток памяти для борьбы с вредоносными агентами и раковыми клетками у пожилых людей [pubmed.ncbi.nlm.nih.gov/33794319]. Регулярные аэробные физические нагрузки связаны с усилением реакции на вакцинацию [pubmed.ncbi.nlm.nih.gov/19001887], повышением способности Т-клеток к делению, повышением способности нейтрофилов к поглощению вредоносных агентов, большей цитотоксической активностью натуральных киллеров иммунитета [pubmed.ncbi.nlm.nih.gov/22465452]. Общепризнано, что люди среднего и пожилого возраста, которые регулярно занимаются аэробными физическими упражнениями средней интенсивности, менее подвержены инфекциям, чем их коллеги, ведущие малоподвижный образ жизни [pubmed.ncbi.nlm.nih.gov/20029165]. Какие механизмы лежат в основе улучшения иммунной функции с помощью аэробных упражнений?
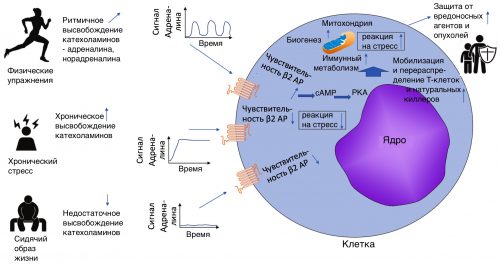 Рисунок 9. β2-адренергические рецепторы активизируются в результате действия адреналина и норадреналина во время стресса. Стресс может быть хроническим, что вредно, а может быть острым, но коротким, как при умеренной спортивной тренировке, что полезно. В ответ на хронический стресс хроническая активация β2 адренергических рецепторов (β2 АР) с помощью адреналина и норадреналина приводит к снижению чувствительности β2 адренергических рецепторов, что в свою очередь вызывает снижение мобилизации и перераспределения Т-клеток иммунитета, а также натуральных киллеров. При сидячем образе жизни низкая активность β2 адренергических рецепторов также снижает функцию иммунитета. Однако, при регулярных умеренных аэробных физических тренировках (30-60 минут в сутки, 5-6 раз в неделю), кратковременная периодическая, но не хроническая активация β2 адренергических рецепторов повышает их чувствительность, что в свою очередь вызывает повышение мобилизации и перераспределения Т-клеток иммунитета и натуральных киллеров для усиления защиты от раковых опухолей, вирусов и других вредоносных агентов. cAMP - циклический аденозинмонофосфат; PKA - протеинкиназа А [pubmed.ncbi.nlm.nih.gov/34302965]
Рисунок 9. β2-адренергические рецепторы активизируются в результате действия адреналина и норадреналина во время стресса. Стресс может быть хроническим, что вредно, а может быть острым, но коротким, как при умеренной спортивной тренировке, что полезно. В ответ на хронический стресс хроническая активация β2 адренергических рецепторов (β2 АР) с помощью адреналина и норадреналина приводит к снижению чувствительности β2 адренергических рецепторов, что в свою очередь вызывает снижение мобилизации и перераспределения Т-клеток иммунитета, а также натуральных киллеров. При сидячем образе жизни низкая активность β2 адренергических рецепторов также снижает функцию иммунитета. Однако, при регулярных умеренных аэробных физических тренировках (30-60 минут в сутки, 5-6 раз в неделю), кратковременная периодическая, но не хроническая активация β2 адренергических рецепторов повышает их чувствительность, что в свою очередь вызывает повышение мобилизации и перераспределения Т-клеток иммунитета и натуральных киллеров для усиления защиты от раковых опухолей, вирусов и других вредоносных агентов. cAMP - циклический аденозинмонофосфат; PKA - протеинкиназа А [pubmed.ncbi.nlm.nih.gov/34302965]
Интересно, что активация β2 адренергических рецепторов улучшает функцию иммунитета, а активация β1 адренергических рецепторов - наоборот, так как подавляет активность β2 адренергических рецепторов. Лекарственное средство пропранолол является блокатором β2 и β1 адренергических рецепторов. В итоге пропранолол, применяемый в дни тренировок, фактически может нейтрализовать полезные действия тренировки на иммунитет. С другой стороны, блокада β1 адренергических рецепторов усиливает активацию β2 адренергических рецепторов. И лекарственное средство, метопролол, которое является блокатором β1 адренергических рецепторов, может благодаря блокаде β1 адренергических рецепторов активизировать β2 адренергические рецепторы. В теории, метопролол, применяемый за несколько часов до тренировки, может усилить полезное действие тренировки на иммунитет [pubmed.ncbi.nlm.nih.gov/34302965]. Однако, это только в теории. Нужно подтвердить это в эксперименте на пациентах. Это важно для пожилых и ослабленных людей, которые не могут тренироваться много, но могут благодаря метопрололу, при отсутствии противопоказаний, усилить эффект тренировок на иммунитет. Однако, метопролол опасное для жизни лекарство. Его применяют только после консультации с врачом. Материал данной статьи предназначен только для иллюстративных и образовательных целей и не гарантирован для любого медицинского использования. Для получения более подробной информации, пожалуйста, обратитесь к вашему врачу.
Какая же интенсивность и продолжительность бега и других аэробных нагрузок полезны в долгосрочной перспективе - годами? Оптимальная нагрузка в исследованиях, показывающая максимальные преимущества для продления жизни — это 150-180 минут в неделю, а ниже 90 минут в неделю уже мало полезно [pubmed.ncbi.nlm.nih.gov/18695077].
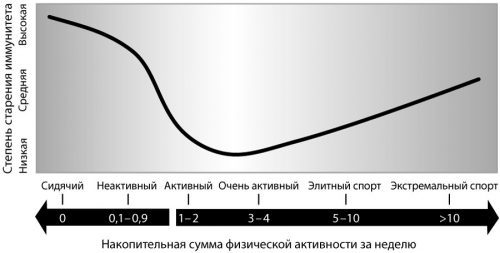 Рисунок 10. При умеренной аэробной нагрузке 150-300 минут в неделю наблюдается наименьшая скорость старения иммунной системы [ncbi.nlm.nih.gov/pubmed/27023222]. А чрезмерные тренировки свыше 360 минут в неделю уже наоборот ухудшают иммунную функцию [ncbi.nlm.nih.gov/pubmed/25660917].
Рисунок 10. При умеренной аэробной нагрузке 150-300 минут в неделю наблюдается наименьшая скорость старения иммунной системы [ncbi.nlm.nih.gov/pubmed/27023222]. А чрезмерные тренировки свыше 360 минут в неделю уже наоборот ухудшают иммунную функцию [ncbi.nlm.nih.gov/pubmed/25660917].
Некоторые функции иммунной системы можно восстановить при помощи здорового питания. Для этого нужно избегать, как недоедания, так и переедания, а также употреблять 600-800 грамм овощей в сутки
Индекс массы тела (ИМТ) — показатель, представляющий собой отношение массы тела к росту человека. Он позволяет косвенно определить, является ли масса тела нормальной, избыточной или недостаточной. Его рассчитывают по формуле: ИМТ = m/h2, где m — масса тела в килограммах, а h — рост человека в метрах. Риск смерти от инфекционных заболеваний у людей старше 70 лет значительно возрастает, если индекс массы их тела менее 20 кг/м2 [pubmed.ncbi.nlm.nih.gov/20370857]. Недостаточный вес также может способствовать увеличению смертности от инфекционных заболеваний из-за неспособности удовлетворить энергетические потребности, связанные с иммунным ответом на микробные инфекции [pubmed.ncbi.nlm.nih.gov/16614394]. С другой стороны, даже дополнительные 5 кг свыше ИМТ 25 кг/м2 связаны с риском умереть от острых респираторных вирусных инфекций (ОРВИ). При чем, если ИМТ ниже 25 кг/м2 связан с сокращением риска умереть от ОРВИ на 69% [ncbi.nlm.nih.gov/pubmed/19299006]. Оптимальный ИМТ для иммунитета у взрослых людей до 65 лет = 20-25 кг/м2.
Измерять окружность талии нужно в положении стоя, в конце фазы выдоха, расслабив мышцы живота, на 2 см. выше пупка — в средней точке между последним ребром и гребнем подвздошной кости [ncbi.nlm.nih.gov/pubmed/29300433]. Внутрибрюшное ожирение, измеряемое по окружности талии связано с более высоким риском умереть от ОРВИ у мужчин [ncbi.nlm.nih.gov/pubmed/24582192]. Ожирение также является одним из основных факторов риска умереть от COVID-19 [pubmed.ncbi.nlm.nih.gov/32173574]. Признаком внутрибрюшного ожирения считают окружность талии у мужчин ≥ 90 см, а у женщин > 80–85 см (по разным оценкам) [ncbi.nlm.nih.gov/pubmed/30272100] [ncbi.nlm.nih.gov/pubmed/30609857] [ncbi.nlm.nih.gov/pubmed/30092838] [ncbi.nlm.nih.gov/pubmed/31909366]. Оптимальная окружность талии у мужчин ≥ 90 см, а у женщин > 80–85 см (по разным оценкам).
Некоторые функции иммунной системы можно восстановить при помощи здорового питания. Кишечная микрофлора вырабатывает особые молекулы, помогающие делению и дифференциации регуляторных T-клеток, а регуляторные Т-клетки играют важную роль в контроле воспаления, аутоиммунных реакций, онкологических заболеваний [nature.com/articles/nature12331]. Анализ популяций выявил сильную взаимосвязь между диетой и составом микрофлоры, а также между составом микрофлоры, заболеваемостью и уровнем воспаления у пожилых людей [nature.com/articles/nature11319]. Манипуляции с составом кишечной микрофлоры представляются еще одним эффективным способом увеличения продолжительности жизни и улучшения самочувствия в старости [nature.com/articles/nature11319] [link.springer.com/article/10.1007/s10522-011-9352-5]. Поэтому важно употреблять в пищу большое количество сырых овощей с целью получения достаточного количества грубой клетчатки, позитивно воздействующей на состав кишечной микрофлоры. Так Международный Всемирный фонд исследований рака рекомендует на основании исследований сделать цельные зерна, некрахмалистые овощи, фрукты и бобовые, в том числе чечевицу, основной частью обычного ежедневного рациона (не менее 30 г клетчатки и не менее 400 г, а лучше 800 г фруктов и овощей каждый день) [wcrf.org/dietandcancer/recommendations/wholegrains-veg-fruit-beans]. Пожилым людям нельзя переедать, но также нельзя и недоедать. Недостаточный вес может способствовать увеличению смертности от инфекционных заболеваний из-за неспособности удовлетворить энергетические потребности, связанные с иммунным ответом на микробные инфекции [pubmed.ncbi.nlm.nih.gov/16614394]. С другой стороны, временные пищевые паузы полезны. Умеренное временное сокращение потребления пищи может повысить защитный иммунитет [pubmed.ncbi.nlm.nih.gov/35139351]. Имеются данные, свидетельствующие о том, что ожирение ограничивает разнообразие Т-клеточных рецепторов у людей с ожирением и диабетом, снижает выработку тимусом наивных Т-клеток [pubmed.ncbi.nlm.nih.gov/32937152]. Даже дополнительные 5 кг излишней массы тела связаны с риском умереть от острых респираторных вирусных инфекций [ncbi.nlm.nih.gov/pubmed/19299006]. Ожирение также является одним из основных факторов риска умереть от COVID-19 [pubmed.ncbi.nlm.nih.gov/32173574].
Исключение дефицита сна восстанавливает функцию иммунитета и снижает риск заболеть простудными заболеваниями в несколько раз
Предварительные данные на людях показали, что сокращение сна существенно нарушает функцию T-клеток иммунитета [ncbi.nlm.nih.gov/pubmed/19040608]. Сокращение сна снижает способность клеток иммунитета уничтожать вирусы [ncbi.nlm.nih.gov/pubmed/8621064]. Натуральные киллеры представляют собой тип токсических лимфоцитов, которые являются критически важными для иммунитета [ncbi.nlm.nih.gov/pubmed/18388298]. Они влияют на несколько видов злокачественных клеток и инфекций, ограничивая их распространение. Эти клетки становятся активными спустя примерно 3 дня после поступления инфекции в организм и сразу реагируют на раковые клетки в организме. Можно сказать, что натуральные киллеры постоянно ищут опухолевые клетки и непосредственно воздействуют на них, вызывая их гибель. Натуральные клетки уникальны, поскольку они обладают способностью распознавать инфицированные клетки в отсутствие антител и специфических маркеров, что позволяет значительно ускорить иммунную реакцию и выздоровление человека. Эти клетки были названы естественными киллерами, поскольку, по ранним представлениям, они не требовали активации для уничтожения клеток, не несущих маркеров главного комплекса гистосовместимости I типа (MHC1). Эта роль особенно важна, потому что вредные клетки, на которых отсутствуют маркеры MHC1, не могут быть обнаружены и уничтожены другими иммунными клетками, такими как клетки Т-лимфоцитов [ncbi.nlm.nih.gov/pubmed/18388298]. Известно, что, если организм не сможет вырабатывать натуральные клетки, то под воздействием бактерий и вирусов может достаточно быстро умереть. Был выявлен дефицит натуральных киллеров у людей в начальной стадии герпес-вирусной инфекции [ncbi.nlm.nih.gov/pubmed/18388298]. Эпидемиологические данные еще в конце 20 века показали, что работники ночных смен, которые обычно испытывают нарушение сна, демонстрируют подавленную клеточную иммунную функцию и повышенную частоту инфекций дыхательных путей [ncbi.nlm.nih.gov/pubmed/6985367] [ncbi.nlm.nih.gov/pubmed/6984725]. Также исследование 2018 года показало, что среди 651 новобранцев британской армии более трети спали менее 6 часов в сутки во время их обучения. И эта треть новобранцев в 4 раза чаще имела инфекции верхних дыхательных путей, теряла больше учебных дней из-за болезни [ncbi.nlm.nih.gov/pubmed/29746692]. У грызунов, иммунизированных вирусом гриппа, лишение сна в течение всего 7 часов сопровождается отсутствием достижения устойчивого вирусологического ответа в легких и отсутствием специфической продукции антител к гриппу в сравнении с контрольной группой грызунов, тоже иммунизированных вирусом гриппа. И ничего этого не наблюдалось у не иммунизированных вирусом грызунов, даже если их лишали сна на 7 часов. Это исследование указывает на то, что у грызунов сон — это поведенческое состояние, которое необходимо для оптимальной иммунной функции в присутствии возбудителя респираторного тракта, а сокращение сна блокирует формирование специфического иммунитета к болезни [ncbi.nlm.nih.gov/pubmed/2562046] [ncbi.nlm.nih.gov/pubmed/2575411]. Длительная потеря сна у животных приводит к летальному исходу вследствие системной инфекции и сепсиса условно-патогенными бактериальными микроорганизмами [ncbi.nlm.nih.gov/pubmed/8238617].
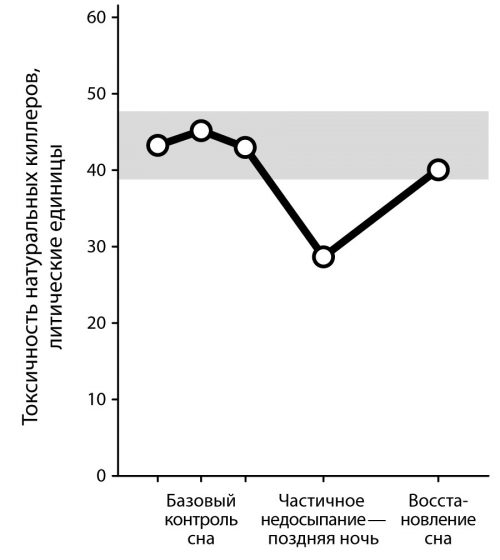 Рисунок 11. Влияние частичного лишения сна поздней ночью на активность иммунных натуральных клеток киллеров (среднее значение ± стандартная ошибка средних литических единиц) у 23 здоровых мужчин. Серая область отображает среднее значение ± стандартная ошибка среднего из трех контрольных базовых значений. Значения литических единиц отражают относительную цитотоксичность (ядовитость для чужеродных клеток) клеток иммунитета лимфоцитов [ncbi.nlm.nih.gov/pubmed/7871104].
Рисунок 11. Влияние частичного лишения сна поздней ночью на активность иммунных натуральных клеток киллеров (среднее значение ± стандартная ошибка средних литических единиц) у 23 здоровых мужчин. Серая область отображает среднее значение ± стандартная ошибка среднего из трех контрольных базовых значений. Значения литических единиц отражают относительную цитотоксичность (ядовитость для чужеродных клеток) клеток иммунитета лимфоцитов [ncbi.nlm.nih.gov/pubmed/7871104].
В пилотном исследовании лишение сна в конце ночи (время бодрствования с 3 до 7 часов утра) у 18 из 23-х здоровых мужчин снижало активность натуральных киллеров иммунитета — на 28% в среднем (рис.) для 23-х человек [ncbi.nlm.nih.gov/pubmed/7871104]. В другом исследовании изучались 46 здоровых мужчин без недавней истории инфекций. Участвовали в исследовании только мужчины, так как активность натуральных киллеров иммунитета, как было показано, колеблется в течение менструального цикла. 42 человека завершили исследование. Средний возраст мужчин был 35 лет (от 25 до 65). Дневники активности сна и бодрствования, полученные в течение 2 недель до начала исследования, подтвердили, что все добровольцы регулярно спали в среднем 7,2 часа в сутки — ночью между 10 часами вечера и 7 часами утра. Потеря сна в начале ночи приводила к подавлению активности натуральных киллеров с уменьшением как числа циркулирующих натуральных киллеров, так и их функциональной активности. Такие изменения сохранялись, по крайней мере, в течение одной ночи восстановительного сна [ncbi.nlm.nih.gov/pubmed/8621064]. Ранее считалось, что плохой сон повышает нашу восприимчивость к обычной простуде. Однако прямых доказательств этому утверждению практически не было кроме проспективных когортных исследований, экспериментов влияния лишения сна на клетки иммунитета и исследований на животных. И вот ученые из Университета Карнеги-Меллон, Питтсбург, Пенсильвания, США в 2009 году опубликовали исследование, в котором решили проверить, связаны ли продолжительность и качество сна в течение нескольких недель, предшествующих вирусному воздействию, с восприимчивостью к простудным заболеваниям. Дизайн исследования был примерно такой. Две недели наблюдали за сном, далее сажали людей на карантин. В течение первых 24 часов карантина (до вирусного воздействия) участники проходили осмотр носа и промывание носа. Затем участников инфицировали вирусом через назальные капли и смотрели вероятность заболеть и иные показатели развития инфекции в течение следующей недели карантина.
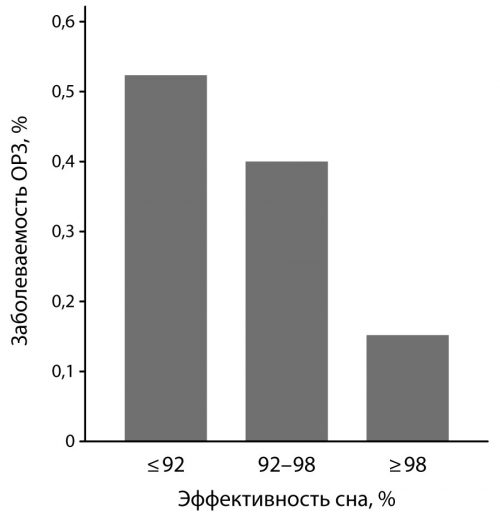 Рисунок 12. Эффективность сна (процент времени, проведенного в постели во сне по отношению к общему времени, проведенному в постели), усредненная за 14 дней наблюдения до заражения вирусом, связана с процентом лиц, у которых впоследствии развилась простуда. Процент простудных заболеваний основан на прогнозируемых значениях (с поправкой на предрасположенность к заболеванию и возраст) [ncbi.nlm.nih.gov/pubmed/19139325].
Рисунок 12. Эффективность сна (процент времени, проведенного в постели во сне по отношению к общему времени, проведенному в постели), усредненная за 14 дней наблюдения до заражения вирусом, связана с процентом лиц, у которых впоследствии развилась простуда. Процент простудных заболеваний основан на прогнозируемых значениях (с поправкой на предрасположенность к заболеванию и возраст) [ncbi.nlm.nih.gov/pubmed/19139325].
В эксперименте приняли участие 153 здоровых мужчин и женщин в возрасте от 21 до 55 лет. Участники с менее чем 7 часами сна почти в 3 раза больше были склонны к простудам, чем те, кто спал от 8 и более часов в сутки (рис.12). Эффективность сна определялась, как продолжительность сна, разделенная на время в постели (время от лежания до выхода из постели), усредненное за 14 дней наблюдения до заражения вирусом. Исследователи заключают, что эти взаимосвязи не могут быть объяснены различиями в титрах антител к вирусу, демографическими показателями, сезоном года, массой тела, объективным социально-экономическим статусом, психологическими переменными или практикой здравоохранения. Процент дней, когда человек чувствовал себя отдохнувшим, также не был связан с простудными заболеваниями [ncbi.nlm.nih.gov/pubmed/19139325] Хотя предыдущее исследование не позволяет сделать причинно-следственные выводы, так как возможно люди хуже спали по иным причинам, и эта иная причина формировала восприимчивость к инфекциям. Например, люди с депрессией хуже спят. Однако данное исследование устраняет обратную причинность в качестве объяснения. То есть, если раньше можно было предположить, что люди хуже спят, потому что чаще болеют, то данное исследование доказало, что это не болезнь влияет на сон, а люди болеют потому, что или хуже спять, или потому, что что-то влияет на качество их сна и это что-то является причиной склонности к простудам.
Статины могут стимулировать иммунитет к более эффективной работе по обнаружению опухолевых клеток и претендуют на лекарства для улучшения иммунной функции
Статины – это ингибиторы 3-гидрокси-3-метилглутарил-СоА-редуктазы (ГМКР). ГМКР – фермент, влияющий на скорость синтеза холестерина. Исследование о влиянии статинов на смертность и прогрессирование рака среди 1 111 407 пациентов показало, что назначение статинов, как до онкологического заболевания, так и вовремя, связано со снижением общей смертности от колоректального рака, от рака молочной железы и предстательной железы [ncbi.nlm.nih.gov/pubmed/27859151]. Мета-анализ 13 исследований с участием 99 297 человек показал, что лечение статинами связано со значительно улучшенной выживаемостью у больных раком легких даже на IV стадии. Потенциальные противоопухолевые механизмы статинов могут заключаться в препятствовании разрастания опухолевых клеток, в подавлении миграции раковых клеток в другие органы, а также в том, что статины нарушают питание опухолей, препятствуя образованию новых кровеносных сосудов. Статины могут индуцировать самоуничтожение раковых клеток и стимулировать иммунитет к более эффективной работе по обнаружению опухолевых клеток. Снижая уровень воспаления, статины могут снижать риски образования раковых клеток в будущем [ncbi.nlm.nih.gov/pubmed/30641276]. Однако эти результаты являются предварительными и нуждаются в подтверждении в рандомизированных двойных слепых плацебо-контролируемых исследованиях.
Хроническое употребление алкоголя, а также, вероятно, и курение могут ослабить защитные силы иммунитета
Хроническое употребление алкоголя связано с повышением частоты развития тяжелых заболеваний из-за легочных инфекций, а также с риском повторного заражения. Хроническое употребление алкоголя снижает ответ иммунитета на вирус [ncbi.nlm.nih.gov/pubmed/31712384] [ncbi.nlm.nih.gov/pubmed/16930226]. Чрезмерное опьянение (1 часть водки, 2 части безалкогольного) повысило уровень кортизола у испытуемых на 233.13% [ncbi.nlm.nih.gov/pubmed/23252809], а кортизол маркер стресса, который при хроническом длительном воздействии может снижать иммунную функцию через резистентность β2 адренергических рецепторов [ncbi.nlm.nih.gov/pubmed/8561294]. Вероятно, курение, также вредно для иммунитета. Компьютерная томография ткани тимуса показала, что замена функциональной ткани тимуса на жировую положительно коррелирует с курением [pubmed.ncbi.nlm.nih.gov/25925358].
Выводы:
- С возрастом снижается количество иммунных наивных Т-клеток и разнообразие их рецепторов, необходимых для эффективной реакции на незнакомые вирусы; снижается эффективность отбраковывания аутореактивных Т-лимфоцитов иммунной системы, способных вызывать хроническое воспаление и аутоиммунные заболевания
- Все иммунные клетки организма формируются в костном мозге от гемопоэтических стволовых клеток, которые могут оставаться молодыми, но стареют под воздействием стареющей стволовой ниши, что также сопровождается старением клеток врожденного и адаптивного иммунитета
- Тимус - это орган иммунной системы, придающий Т-лимфоцитам иммунные свойства. Он важен для юного организма, иммунитет которого только учится распознавать вредоносные агенты. Однако для взрослого организма тимус уже не так важен. Удаление тимуса в раннем возрасте, когда иммунитет еще не сформировался, сокращает продолжительность жизни. Удаление же тимуса в возрасте 40-60 лет практически не влияет на ожидаемую продолжительность жизни
- Хроническая вирусная инфекция может привести к необратимому повреждению иммунной системы, что выражается в снижении иммунной защиты от вредоносных агентов и раковых опухолей
- «Воспалительное старение» может быть состоянием адаптационной повышенной готовности иммунитета для быстрого ответа на угрозу от вредоносных агентов в условиях, когда адаптивная иммунная система терпит неудачу из-за старения, а следовательно, медикаментозное подавление «воспалительного старения» без восстановления функции адаптивного иммунитета может создавать угрозу выживания
- Чтобы на основании анализов иммунных клеток в крови предсказывать, как то или иное воздействие (диеты, лекарства и др.) повлияло на риски смертности, нужно на основании машинного обучения создавать модели, учитывающие возраст, год рождения, пол, генетику, окружающую среду, питание, микробиоту, пожизненное воздействие вредоносных агентов (вирусов, бактерий и др.), доступ к медицине, эпидемии и войны
- Введение интерлейкина 7-го типа и фактора роста кератиноцитов, трансплантация эпителиальных клеток тимуса, использование внеклеточной матрицы в качестве каркаса для клеток с целью регенерации тимуса, а также пересадка костного мозга - перспективные методы омоложения иммунной системы
- 4-5 ежемесячных циклов голоданий по 4 дня подряд могут увеличивать долю наивных Т-клеток иммунитета у людей, что связано с ростом вероятности, что при проникновении в организм какого-либо нового вируса найдётся Т-клетка, рецепторы которой окажутся подходящими для того, чтобы его обезвредить
- Влияние экстремального закаливания организма холодом на иммунитет не изучено и потенциально может повысить риск умереть
- Не существует доказательств эффективности добавок цинка и витамина D для снижения риска простудиться, заболеть, для сокращения продолжительности заболевания, а также для снижения симптомов аутоиммунных заболеваний
- Иммуномодуляторы не входят ни в один международный стандарт лечения или профилактики простудных заболеваний из-за отсутствия доказательств эффективности
- Повышение уровня гормонов стресса в результате воздействия хронического стресса увеличивает риск заболеть инфекционными заболеваниями
- Люди среднего и пожилого возраста, которые регулярно занимаются аэробными физическими упражнениями средней интенсивности, менее подвержены инфекциям, имеют лучшую реакцию на вакцинацию, повышенную способность наивных Т-клеток к делению и мобилизации, обладают повышенной способностью нейтрофилов к поглощению вредоносных агентов, большей цитотоксической активностью натуральных киллеров иммунитета, лучшей иммунной защитой от раковых опухолей
- Некоторые функции иммунной системы можно восстановить при помощи здорового питания. Для этого нужно избегать, как недоедания, так и переедания, а также употреблять 600-800 грамм овощей в сутки
- Исключение дефицита сна восстанавливает функцию иммунитета и снижает риск заболеть простудными заболеваниями в несколько раз
- Статины могут стимулировать иммунитет к более эффективной работе по обнаружению опухолевых клеток и претендуют на лекарства для улучшения иммунной функции
- Хроническое употребление алкоголя, а также, вероятно, и курение могут ослабить защитные силы иммунитета
-
Знаете ли вы, что сайт nestarenie.ru — объективно один из самых популярных в России ресурсов про старение и долголетие - в Яндексе, в Гугле, по количеству, качеству и лояльности аудитории. nestarenie.ru имеет потенциал, чтобы стать одним из самых популярных сайтов о борьбе со старением не только в России, но и в мире. Для этого нужны деньги. Я призываю всех сделать пожертвования, а также убедить своих друзей поступить аналогично. Карта МИР в Сбере (рубли): 2202 2032 1501 6686 (МАЙЯВИ Ч.)
Обязательно оставляйте свои комментарии под статьей, которую Вы читаете. Это очень важно для нас.
Предлагаем Вам оформить почтовую подписку на самые новые и актуальные новости, которые появляются в науке, а также новости нашей научно-просветительской группы, чтобы ничего не упустить. Обязательно оставляйте свои комментарии под статьей, которую вычитаете. Это очень важно для нас.

Автор статьи
Веремеенко Дмитрий Евгеньевич
Телефон:
Почта:
Сфера деятельности - data science в медицине
Основатель проекта, изучающего терапии, направленные на увеличение продолжительности жизни человека (nestarenie.ru/slb-expert_.html)
Со-основатель IT сервиса продления жизни
Основатель форума о продлении жизни Nestarenie Camp (nestarenie.ru/camp.html)
Со-автор книги "Бонусные годы" (nestarenie.ru/kniga-3.html)
Создатель справочного блога о старении человека (nestarenie.ru)
Социальные сети:
- Карта Viza (доллары): 4215 8901 1587 0138 для переводов за пределами РФ
- Карта МИР в Сбере (рубли): 2202 2032 1501 6686 (МАЙЯВИ Ч.) - на территории РФ
71 комментарий
-
Лилия31 марта 2024, 21:47
А как выглядит голодание с употреблением 500-700 калорий? Что можно есть?
-
Максим (58-й-183см-70кг-талия 78см)28 марта 2023, 06:06
Основатель «Сбермаркета» Дмитрий Жулин попал в реанимацию
А его девушка, студентка медицинского института, погибла.
Оба ранее делали капельницы с препаратом «Лаеннек».
bfm.ru/news/521982Дополнительно пишут, что купили по дешевке, собирались повысить иммунитет, а он у молодых и так высокий, начался цитокоиновый шторм, спасти не смогли.
Ранее писал, что в октябре-ноябре делал полный курс (50 ампул внутривенно и внутримышечно) Лаеннека, препарат покупал на 25% дороже, по рекомендации и с гарантией свежести, оригинала и соблюдения правил хранения. И как мне ТАМ сказали – «тебе лучше не знать, что покупают те, кто хочет подешевле, иначе спать не сможешь»! Еще тогда я этим людям поверил и поверил сразу!
Фото фиксация:
ic.wampi.ru/2023/02/07/IMG_3178.jpg
ic.wampi.ru/2023/02/07/IMG_3135.jpg
_______________________________
Мой альбом wampi.ru/image/RPkjzxI -
Svetlana21 марта 2023, 20:20
А как бороться с герпесом? Стоит ли при появлении на губах/носу принимать таблетки ацикловир? Или достаточно мазать наружно?
-
Денис07 июля 2023, 10:01
Пить курсами валацикловир (Валвир) или более современные и мощные препараты (Фамвир) с тем же принципом действия. Переболев раз не простым (который был всегда), а опоясывающим герпесом, вынужденно погрузился в тему.
Все препараты, включая древний ацикловир, эффективны, но новые лучше. Скажем, орально Валацикловир даст тот же эффект, что ацикловир внутривенно.
“Мазать” – это после драки махать кулаками, а вот превентивно пропить курс весной или летом – это точно сработает. Длительность курса определяется собственным иммунитетом. Мне хватает недельного. Товарищу прописывали полгода.
Но после курса, герпес как проблема исчезает полностью. При попытках появиться, применяю схему 2 гр/сутки (есть в инструкции). Для меня сегодня видеть герпес на губе человека сродни гнилым зубам – странно, чего это он не вылечит?..
-
-
Гека23 февраля 2023, 11:13
Еще подсказка. Почему у большинства псориазных больных пяточки как у младенца и никогда не трескаются. Фактора всего два избыток одного витамина и дефицит одного фактора. А закрепляет все это микробиота.
-
Гека22 февраля 2023, 15:50
Мнение же о псориазе и витамине д основано не на циклах обострения и ремиссии, а на наблюдениях и простой логической ошибке. Люди заметили что на солнышке состояние псориаза улучшается, и стали думать а что же на солнышке в коже вырабатывается, а так это же витамин д. А надо было думать что же на солнышке разрушается, и избыток чего приводит к излишней кератинизации ))
-
Гека22 февраля 2023, 15:29
Углубляясь в частности ученые не видят общей картины. Или находятся в ситуации систематической ошибки выжившего. Псориаз легко и успешно лечится, двумя препаратами. Источником воспаления всего в организме является серотонин, витамин д подавляет пиридоксиновый обмен может помогать при ревматойдном артрите и паре аутоимунок, но не является лечением и совмещен с кучей побочки. Так же и статины, исследования с положительной динамикой есть, а можно было бы добавить в исследования сколько человек из тех групп исследуемых впоследствии совершили суицид или попытку, а там нормально так
-
Максим (57лет-183см-70кг-талия 78см)15 ноября 2022, 07:02
Отвечаю Алексей Москальков
“Кундалини” придется подождать 2 года. Ранее писал, жду свои 60 лет плюс 1 день, иначе даже в ЦАО г.Москвы не чувствую себя в безопасности. -
Максим+(57лет-183см-71кг-талия+78см)14 ноября 2022, 10:59
Продолжение!
Завершена 1 серия.
Было сделано 10 капельниц Лаеннек по 3 ампулы.
Вначале соблюдал назначение врача.
До 18-й ампулы внутривенно – эффект ноль.
Стало жаль потерянного времени и денег.
Поэтому, действуя осознанно, игнорируя порядок назначенной врачом процедуры, я разрешил медсестре увеличить скорость капельницы в два раза. И только после 24-й ампулы, как говорят, «поймал приход». Во время ходьбы на улице внезапно внутри тела в районе солнечного сплетения возникла какая-то «молодая» энергия, которая стала подниматься вверх по туловищу к шее и голове, дошла до мозгов и рассыпалась серебряным конфетти сверху вниз по всему телу, от макушки до пяток. Это длилось несколько секунд, я ощутил забытую молодость и почувствовал, что некие силы, ранее дремавшие внутри меня, стали просыпаться… Последние 6 ампул вливал коротким интервалом с меньшей дозой физраствора. Вот теперь я узнал, что такое Лаеннек! Было несколько необычно ярких цветных солнечных снов о том, как я летаю во сне. Это хрестоматийный сон молодого растущего организма (детям часто такое снится).
После 10 капельниц сдал кровь на иммунологическое исследование (расширенное) в Хеликс.
Это целый комплекс анализов, если Дмитрию интересно, могу выслать ему на почту.
В целом, я доволен. Читал в Интернете, что на расширенное исследование дают допуск от 20 до 40%, огромное число факторов влияет на результат. У меня лучше!
Зафиксирована интересная особенность. Например – лейкоцитарная формула вся в норме, но все ее элементы находятся на нижнем уровне «нормы», итого в сумме получается общее снижение лейкоцитов. Но дело в том, что уровень лейкоцитов поднимает воспаление, а его у меня нет! Тоже самое и с субполяциями лимфоцитов, некоторые элементы при отсутствии даже вялотекущего воспаления не нужны и находятся в самом низу рефренса (спят, как в анабиозе). Анализаторы даже после физической нагрузки не могут зафиксировать хоть какие-то интерлейкины (выше об этом писал). При этом все виды иммуноглобулинов и С3-4 комплементы, ЦИКи в норме.
Начата 2 серия. 10 уколов Лаеннек внутримышечно сразу по 2 ампулы.-
Алексей Москальков14 ноября 2022, 13:24
Максим+(57лет-183см-71кг-талия+78см), “Во время ходьбы на улице внезапно внутри тела в районе солнечного сплетения возникла какая-то «молодая» энергия, которая стала подниматься вверх по туловищу к шее и голове, дошла до мозгов и рассыпалась серебряным конфетти сверху вниз по всему телу, от макушки до пяток. Это длилось несколько секунд, я ощутил забытую молодость и почувствовал, что некие силы, ранее дремавшие внутри меня, стали просыпаться… ” – да у вас кундалини пробудилась!
-
-
Валентина10 ноября 2022, 20:57
Спасибо большое за ответ и за Ваш труд
-
Валентина10 ноября 2022, 18:23
Дмитрий, у меня такая же аллергия на холод, как у Вашей жены. Зимой невозможно выйти на улицу-одышка сразу. Подскажите, пожалуйста, как вы избавились от этого.
-
Сергей Александрович.28 октября 2022, 11:29
СПАСИБО!
-
Ирина28 октября 2022, 07:51
Дмитрий, если есть аллергия на некоторые химическме вещества, например бытовую химию или реагенты на дороге, что делать? Как от этого избавиться? Голодания в таком случае помогут, чтобы тучные клетки не атаковали организм?
Большое спасибо за интересную статью. Очень сложно в этом разбираться самой, но Вы все разложили по полочкам. К врачам обращаться бесполезно, надо самим пытаться разобраться. Огромный объем работы провели.
-
Артем22 апреля 2023, 14:50
Большинство аллергий устраняется психотерапией.
-
-
Татьяна Г.27 октября 2022, 13:40
Мне очень интересно читать Ваши статьи. Интересная для меня была информация о витамине Д и статинах. О статинах хотелось бы побольше информации, об их плюсах и минусах. Эти препараты я пью давно, т.к. нет щитовидной железы, отсюда остеопороз, и кальций откладывается не в костях, а в сосудах .
Очень заинтересована в Вашей новой проработке проблемы плохого сна у пожилых ( преждевременное пробуждение и невозможность заснуть, а потом днем как вареная), а к снотворным – быстрое привыкание. Я думаю, что у каждого второго 70+ эти проблемы имеют место.
Благодарю Вас за Вашу работу. -
Татьяна Г.27 октября 2022, 13:37
Мне очень интересно читать Ваши статьи. Интересная для меня была информация о витамине Д и статинах. О статинах хотелось бы побольше информации, об их плюсах и минусах. Эти препараты я пью давно, т.к. нет щитовидной железы, отсюда остеопороз, и кальций откладывается не в костях, а в сосудах .
Очень заинтересована в Вашей новой проработке проблемы плохого сна у пожилых ( преждевременное пробуждение и невозможность заснуть, а потом днем как вареная), а к снотворным – быстрое привыкание. Я думаю, что у каждого второго 70+ эти проблемы имеют место.
Благодарю Вас за Вашу работу. -
Юлия25 октября 2022, 18:22
Добрый вечер! Дмитрий , вы пишите “результате рандомизированного контролируемого исследование был сделан вывод о том, что рассасывание леденцов с ацетатом цинка не сокращает срок выздоровления при простудах [bmjopen.bmj.com/content/10/1/e031662].”
Правильно ли я понимаю, что то исследование, о котором вы писали ранее про прием цинка ацетата в начале вирусного заболевания и сокращение времени болезни на 50% , ..уже неактуально?…
-
Максим (58-й -183см-70кг-талия 78см)03 октября 2022, 12:51
Продолжение …
Закончил курс уколов (10 через день) Тималин.
Через 14 дней повторно сдал панель №1 субполяций лимфоцитов, панель интерлейкинов, циркулирующих иммунных комплексов и опухолевых маркеров. Сдавал строго после состояния покоя 48 часов, так как был нужен уровень именно плохого интерлейкина. Анализы зафиксировали стабилизацию иммунограммы, отсутствие воспалительных процессов.
Поэтому я решил проверить влияние физической нагрузки на интерлейкины и сдал анализ повторно, через час после бега на 8 км. В моем случае разница отсутствовала.
Вот мои результаты после физической нагрузки (через 1 час после бег 8 км).
Интерлейкин 6 – мой результат <1.5 пг/мл (рефренс < 7.0)
Интерлейкин 8 – мой результат 14.3 пг/мл (рефренс < 62)
Интерлейкин 10 – мой результат < 1.0 пг/мл (рефренс < 31)
ФНО/TNFα (Фактор некроза опухоли) – мой результат <1.0 пг/мл (рефренс < 6).
Это не все анализы, их очень много и просто не хочу все вручную печатать. Главное – они хорошие и отличные!
Посетил иммунолога.
Результаты анализов позволили правильно назначить индивидуальную схему для введения препарата Лаеннек.
Назначена схема введения препарата.
1 серия: 3 (три) ампулы внутривенно капельно на 250 мл физраствора, скорость 30-40 капель в минуту, интервал 72 часа (всего 10 введений), затем вновь сдается контрольная панель субполяций лимфоцитов.Приступил к выполнению 1 серии.
Дополнительно в плане подготовки перед началом введения Лаеннек было сделано следующее. В течении 20 дней до 1 укола был подавлен фермент матриксной протеиназы. За 2 недели до введения Лаеннек был внутриклеточно повышен и остается повышенным уровень конфермента (β) NAD+ (самая активная форма бета).
-
Ирина24 октября 2022, 22:50
Максим, здравия! Интересно было бы пообщаться с вами, но не на этой платформе, по теме слегка над имеющейся информацией. Вас можно найти ВК? Благодарю)
-
Максим (58-й-183см-70кг-талия 78см)26 октября 2022, 07:28
Отвечаю Ирине: Случайно заметил Ваш вопрос, социальными сетями не пользуюсь, можно в телеграмм в чат написать, так другие делают.
Пока новостей за иммунитет особых нет, продолжается 1 серия, сегодня будет 7 седьмое (всего 10 вливаний по 3 ампулы) вливание Лаеннек. Неделя перерыв и пойдет 2 серия – сразу уколы по 3 ампулы внутримышечно (всего 20).
Дополнительно буду употреблять : “золотое кольцо токоферолов” – 4 формы токоферола и 4 токотриенола (спецконтейнер – хранить в темноте, в холодильнике, открывать только перед употреблением).
-
-
-
Елена10 сентября 2022, 16:41
Что может значить значительное повышение CD4+ CD8+, повышение более чем в 20 раз. ?
-
Максим (57лет-183см-70кг-талия 78см)07 сентября 2022, 06:48
Новости иммунологии!
Заканчиваю курс уколов Тималин. Врач сказала, что моя реакция 4 из 5 на этот препарат это не пожизненно, а максимум на 6 месяцев. Затем моя индивидуальная чувствительность к панели иммуномодуляторов изменится. В конце сентября снова сдам панель субполяций лимфоцитов и панель интерлейкинов. Последние буду сдавать только после состояния покоя 48 часов, так как нужен уровень именно плохого интерлейкина. Это позволит правильно назначить схему для введения препарата Лаеннек. У меня будет полный курс, 50 уколов внутривенно, капельно. Это дорогой препарат, много подделок, особенно в московских салонах красоты, поэтому есть процедура проверки, на Айфон ставится приложение производителя и по голограмме, кур-коду и чипу считывается сигнал оригинальности. Появляется специальный экран. После подтверждения которого можно перейти на сайт производителя и еще раз убедиться, что это оригинал. Также буду сдавать опухолевые маркеры с целью рассмотреть целесообразность применения препарата подавителя CD4 и CD8 Т-лимфоцитов, экспрессирующих рецептор запрограммированной смерти-1 (PD-1). Дмитрий писал об этом препарате в статье о почках.
Спросил врача – могу ли я увидеть свой иммунитет и оценить его качество и возраст. Она сказала, что в клинической практики такого нет, только на академическом уровне, экспериментальные разработки. Но и там много проблем, например, что считать рефренсами? На экране масс-спектрометра здоровые и молодые клетки иммунитета выглядят как рой весело порхающих пчелок, а внизу экрана серая слабо шевелящаяся масса отходов, биомусор, старый, умирающий иммунитет. Я сказал, что хочу увидеть свой иммунитет. Но как я понял из ее ответа, что у меня сейчас не иммунитет, а биомусор и никто на это время свое не потратит. -
Максим (57лет-183см-70кг-талия 78см)31 августа 2022, 03:47
Отвечаю батя Батина
Так и есть (!миры космических цивилизаций протянули руку помощи!), к тому же если читали и видели мои посты ранее в Телеграмм чате, у меня всегда есть доказательства и я их предъявляю. Вероятно, это для кого-то стало неудобным и меня там заблокировали. Здесь у меня также нет возможности предъявлять вещественные (письменные) доказательства, Остается писать только словами.
На сейчас у меня подборка доказательств с октября прошлого года и она пополняется. В настоящее время для постановки заплатки применяется Тактивин. Осталось 5 уколов, потом, через 2 недели новый контроль субполяции лимфоцитов.-
Виктор К.31 августа 2022, 15:40
В сообщении от 29. 08 в 15:52 вы пишете у меня 1 этап, серия уколов Тиамин , а сейчас пишите тактивин. Так что вам колят витамины или пептиды?
-
Максим (58-й -183см-70кг-талия 78см)31 августа 2022, 19:21
Отвечаю для Виктор К.
Действительно, моя опечатка!
А все из-за того, что фото и результаты анализов нельзя вставлять.
Тактивин и Тималин – это разные названия одного и того же препарата.Мне колят Тималин, укол через день, всего будет 10 уколов.
Затем через 2 недели контроль панели №1 субполяции лимфоцитов.
Ранее был сделан индивидуальный тест на этот препарат, моя чувствительность 4 из 5 возможных.Прийдется таким образом давать ссылку на фото.
Тималин 10 мг 10 шт. флакон лиофилизат для приготовления раствора для внутримышечного введения
//apteka.ru/product/timalin-10-mg-10-sht-flakon-liofilizat-dlya-prigotovleniya-rastvora-dlya-vnutrimyshechnogo-vvedeniya-5e326a6465b5ab000165228a/
-
-
-
Максим (58-й -183см-70кг-талия 78см)29 августа 2022, 18:36
Этого недостаточно для официальной медицины?
Госреестр лекарственных средств
Торговое наименование лекарственного препарата Лаеннек
Регистрационный номер П N013851/01
Код АТХ L03, A05BA ИММУНОСТИМУЛЯТОРЫ/grls.rosminzdrav.ru/GRLS.aspx?RegNumber=&MnnR=&lf=&TradeNmR=%D0%9B%D0%B0%D0%B5%D0%BD%D0%BD%D0%B5%D0%BA&OwnerName=&MnfOrg=&MnfOrgCountry=&isfs=0&isND=-1®type=&pageSize=10&order=RegDate&orderType=desc&pageNum=1
-
батя Батина30 августа 2022, 13:34
Максим (58-й -183см-70кг-талия 78см) : “цель 1 этапа — немедленная заплатка на поврежденный иммунитет” – ну ты крутой. инопланетные методы из будущего.
-
-
Максим (58-й -183см-70кг-талия 78см)28 августа 2022, 17:31
Дмитрий, есть какие-то исследования по препарату Лаеннек (Япония) (внутривенно) — гидролизат плаценты человека?!
“Лаеннек” 一 натуральный биостимулятор, созданный на основе гидролизата человеческой плаценты. Он был разработан и впервые применен в 1956 году в Японии доктором медицинских наук Хиэда Кэнтаро. Однако несмотря на японское происхождение, препарат имеет русские корни: академик В.П.Филатов был родоначальником теории тканевой терапии и первым предложил использовать в медицине препараты из плаценты.
Изначально “Лаеннек” был создан как иммуномодулирующее и гепатопротекторное средство. Однако со временем были глубоко изучены его мощные омолаживающие свойства и препарат стал широко применяться в эстетической медицине и антивозрастной косметологии.
-
Леонид26 августа 2022, 15:10
Спасибо.
-
Арташес16 августа 2022, 12:04
Интересно,но опять много темных мест,лет60назад Пархон и Анна Асланян начали лечение старости 2%новокаином,и сейчас эта тради2ия в Бухаресте продолжают,интересно ваше мнение об этом,Поллинг а сша поднял С витаминны1 бум,правда он скончался в 93 года!Дмитрий а вы какого мнения о них!Большое спасибо՝Арташес Торосян,не врач!Спасибо,Армения,Еревае
-
Игорь13 августа 2022, 16:14
Дмитрий, если составить своеобразный рейтинг способов поднятия иммунитета, то лучшим будет FMD? И второй вопрос, могу ли я в дни кардио принимать метапролол за несколько часов до тренировки? Я- здоров и Лолы переношу хорошо, хочу поэкспериментировать на свой страх и риск или это только для ослабленных людей?
-
Алексей11 августа 2022, 18:34
Странно, что у одной из лучших статей блога совсем нет комментариев. Спасибо за качественное погружение в тему!
Дмитрий, не встречалось ли Вам по ходу дела что-то про влияние аллергий на иммунитет или может даже про влияние АСИТ (лечение аллергии пошаговым введением сверхдоз аллергена) на иммунитет? Если аллергия, по сути, источник хронического воспаления, то эмпирически в моём дилетантском представлении можно ожидать 1) повышенного износа иммунитета от аллергии; 2) снижения/нарушения специфичности иммунитета при использовании лечения сверхдозами аллергена. Поиск по научным статьям, к сожалению, ничего не дал. Да и сложилось впечатление, что человечество понимает механизма аллергии пока только на уровне трёхлетнего ребёнка =)-
Максим (58-й -183см-70кг-талия 78см)12 августа 2022, 04:41
Алексей, ошибаетесь! Я не только прочитал этот цикл статей, но и начал немедленно действовать!
В другой ветке писал …. мой визит к иммунологу оказался успешным.
Было обнаружено снижение иммунитета в начале этого года, сейчас организм пытается залатать эту дыру в иммунитете. И снова анализы придут мне на помощь.
Под контролем иммунолога я пройду несколько этапов.
1. Немедленные действия по устранению дыры в иммунитете
2. Восстановление и стабилизация иммунитета
3. Укрепление и омоложение иммунитета, создание «подушки безопасности».По 1 этапу. Уже через 16 дней я получу стартовые препараты, к этому времени будут готовы анализы, которые покажут через что можно воздействовать именно на мой иммунитет. В частности, это расширенная панель интерферонов и иммуномодуляторов, типа: гаммаферон, ингарон, реферон, виферон, амиксин, ниовир, циклоферон, галавит, иммун. Далее, это все анализы, связанные с фагоцитарной активностью и панель 1 уровня от СD3 до CD19 и их различные сочетания.
Иммунолог мне сказала, что сейчас имеются и доступны средства разного ценового диапазона (от таблеток до уколов и вливаний) для решения моей проблемы. Соответственно, чем дороже, тем эффективнее и надежнее.-
Ирина15 августа 2022, 05:43
Максим , буду благодарна если поделитесь контактом вашего иммунолога. Спасибо
-
Максим (58-й -183см-70кг-талия 78см)15 августа 2022, 15:53
Это не секрет!
Лебедева Инна Сергеевна
Врач аллерголог-иммунолог
«СМ-Клиника» на ул. Ярославская (м. «ВДНХ»)
-
-
Максим (58-й -183см-70кг-талия 78см)22 августа 2022, 17:02
Продолжу историю своего иммунитета.
Пришли результаты анализов:
Фагоцитоз (комплекс) – низкие показатели, но норма.
Интерфероновый статус – норма, но отдельные показатели низкие.
Панель чувствительности к иммуномодуляторам – коротко – Тактивин 4 из 5 возможных, остальное 1-2.
Панель 1 уровня субполяций лимфоцитов – натуральные киллеры (NK) почти 0, Т-цитотоксические – почти 0, все остальное на границе нижней нормы.
Формальный мой диагноз – D83.8 другие общие вариабельные иммунодефициты (по импортной классификации – CVID).
Делаем ставку на Тактивин (Тималин) (это уколы тимуса экстракт), после 1 серии уколов новый контроль уровня субполяций лимфоцитов.
Контрольные (желаемые) цифры от иммунолога я получил. Приступил к выполнению …-
Максим (58-й -183см-70кг-талия 78см)23 августа 2022, 06:59
Дополнение.
Что интересно, мои два последних ОАК (расширенные) были без отклонений, все уже было в пределах рефренса!!! Даже лимфоциты абсолютные (авс) были в норме! И если бы я не стал копать глубже – сделал иммунограмму расширенную, другие анализы, которые назвал ранее, я даже бы не подозревал о дыре в своем иммунитете и чем мне это грозит в самом ближайшем будущем.Что касается Тактивин (Тималин) (это уколы тимуса экстракт) – это старый советский препарат, чернобыльцев им кололи. Только результат зависит не от самого укола, а от индивидуальной реакции организма на него. А на это только анализ может дать ответ. Мне повезло, чувствительность индивидуальная 4 из 5 возможных. Иммунолог сказала, что чувствительность 5 (пять) единиц на иммуномодулятор она видела в анализах только 2 раза за всю жизнь.
На 3 этапе, вероятно займемся активностью всех цитокоинов (интерлейкины), если они даже в рефренсе, но около верхней границы, будем давить их вниз – это невидимый атеросклерозный диверсант!
-
-
-
Свежие комментарии
Подпишитесь на свежие статьи
Предлагаем Вам оформить почтовую подписку на самые новые и актуальные новости, которые появляются в науке, а также новости нашей научно-просветительской группы, чтобы ничего не упустить.