Дата создания: 7 февраля 2018
Обновлено: 09 июля 2021
Маркер повреждения ДНК и окислительного стресса 8-oxo-dGsn
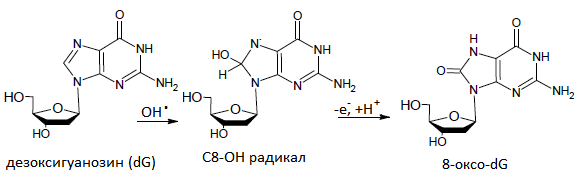
8-оксо-2'-дезоксигуанозин (8-оксо-dG) — окисленное производное дезоксигуанозина. 8-оксо-dG - это преобладающая форма повреждения ДНК от окислительного стресса. Молекула ДНК состоит из азотистых оснований: гуанина, тимина, аденина и цитозина. ДНК в живых системах постоянно подвергается действию окислительного стресса. Гуанин обладает самым низким потенциалом ионизации среди природных азотистых оснований, поэтому наиболее подвержен окислительному повреждению. Образование 8-оксо-2’-дезоксигуанозина в результате реакции 2’-оксигуанозина с гидроксилрадикалами изображено на рисунке.
 С возрастом из-за окислительного стресса в ДНК (молекула, где закодирован генетический код организма) возникают ошибки и мутации. Чем быстрее скорость накопления повреждений ДНК и мутаций, тем быстрее стареет организм. 2011 год, Университет Ливерпуля, Великобритания. Накопление повреждений ДНК с возрастом является одной из основных причин старения. А генетические манипуляции с путями ремонта ДНК у мышей, еще более укрепляют эту гипотезу. У человека и других млекопитающих, повреждение ДНК происходит от 25 до 115 раз в минуту в каждой клетке. Ускоренное старение было связано с дефектами в ремонте ДНК, что указывает на то, что повышенный уровень повреждений ДНК может ускорять физиологический спад и развитие возрастных заболеваний, а не только риска раковых опухолей. В данных исследованиях повышение повреждений ДНК определялось с помощью маркера разрушения ДНК 8- oxo-dG.
С возрастом из-за окислительного стресса в ДНК (молекула, где закодирован генетический код организма) возникают ошибки и мутации. Чем быстрее скорость накопления повреждений ДНК и мутаций, тем быстрее стареет организм. 2011 год, Университет Ливерпуля, Великобритания. Накопление повреждений ДНК с возрастом является одной из основных причин старения. А генетические манипуляции с путями ремонта ДНК у мышей, еще более укрепляют эту гипотезу. У человека и других млекопитающих, повреждение ДНК происходит от 25 до 115 раз в минуту в каждой клетке. Ускоренное старение было связано с дефектами в ремонте ДНК, что указывает на то, что повышенный уровень повреждений ДНК может ускорять физиологический спад и развитие возрастных заболеваний, а не только риска раковых опухолей. В данных исследованиях повышение повреждений ДНК определялось с помощью маркера разрушения ДНК 8- oxo-dG.
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/21600302
- www.ncbi.nlm.nih.gov/pubmed/10792040
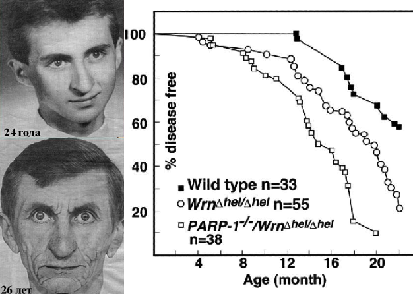 Так, например, канадскими учеными в 2003 году было показано, что люди с синдромом Вернера (прогерея взрослых) быстро стареют и имеют дефицит PARP1 (ядерный фермент, отвечающий за ремонт ДНК) и имеют более высокое значение маркера разрушения ДНК 8- oxo-dG. Такие люди могут состариться буквально за 2 года, как показано на реальных фотографиях одного и того же человека в возрасте с 24 лет до 26 лет. Так активность ядерного фермента PARP1 возрастает в 500 раз и более при связывании с участками разрыва ДНК (ремонтирует ДНК). И как показано на графиках (см. рисунок) мыши с дефицитом PARP1 живут гораздо меньше. У них быстрее разрушается ДНК. Также французские ученые в 1998 году показали, что в лимфобластах долгожителей (100 лет и старше) наоборот значительно выше активности PARP1, чем в клеточных линиях молодых людей (от 20 до 70 лет). То есть, как мы видим, чем выше фермент, восстанавливающий ДНК, тем дольше живут люди.
Так, например, канадскими учеными в 2003 году было показано, что люди с синдромом Вернера (прогерея взрослых) быстро стареют и имеют дефицит PARP1 (ядерный фермент, отвечающий за ремонт ДНК) и имеют более высокое значение маркера разрушения ДНК 8- oxo-dG. Такие люди могут состариться буквально за 2 года, как показано на реальных фотографиях одного и того же человека в возрасте с 24 лет до 26 лет. Так активность ядерного фермента PARP1 возрастает в 500 раз и более при связывании с участками разрыва ДНК (ремонтирует ДНК). И как показано на графиках (см. рисунок) мыши с дефицитом PARP1 живут гораздо меньше. У них быстрее разрушается ДНК. Также французские ученые в 1998 году показали, что в лимфобластах долгожителей (100 лет и старше) наоборот значительно выше активности PARP1, чем в клеточных линиях молодых людей (от 20 до 70 лет). То есть, как мы видим, чем выше фермент, восстанавливающий ДНК, тем дольше живут люди.
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/1465394
- www.ncbi.nlm.nih.gov/pubmed/12707040
- www.ncbi.nlm.nih.gov/pubmed/9587069
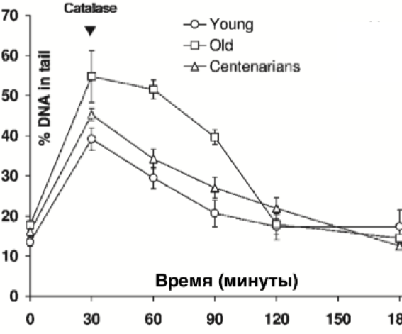 В клетках пожилых людей (69 до 75 лет) PARP1 и PARP2 уменьшается в 2 раза в сравнении с молодыми (от 19 до 26 лет). Но у долгожителей (от 100 до 107 лет) экспрессия PARP1 на уровне молодых людей, как можно увидеть на рисунке слева. Получается, что у долгожителей меньше повреждается ДНК. А фермент, отвечающий за ремонт ДНК, значительно более активен.
В клетках пожилых людей (69 до 75 лет) PARP1 и PARP2 уменьшается в 2 раза в сравнении с молодыми (от 19 до 26 лет). Но у долгожителей (от 100 до 107 лет) экспрессия PARP1 на уровне молодых людей, как можно увидеть на рисунке слева. Получается, что у долгожителей меньше повреждается ДНК. А фермент, отвечающий за ремонт ДНК, значительно более активен.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/17518695
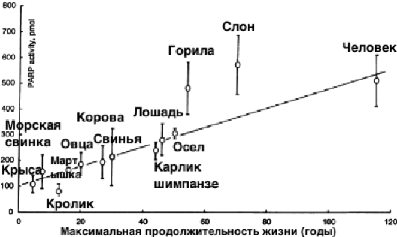 Связь более высокого PARP1 в лейкоцитах клеток с более высокой максимальной продолжительностью жизни распространяется не только в рамках одного вида, но и на видовые отличия. Так в среднем, чем выше PARP1 у вида млекопитающих, тем дольше живет данный вид. Посмотрите на картинке. Сравнивается связь PARP1 в лейкоцитах клеток с максимальной продолжительностью жизни крыс, кролика, морской свинки, мартышки, овцы, коровы, свиньи, лошади, карликовых шимпанзе, осла, гориллы, слона и человека. И чем выше PARP1 у вида млекопитающих, тем стабильнее ДНК (меньше повреждений ДНК), тем дольше живет данный вид животных.
Связь более высокого PARP1 в лейкоцитах клеток с более высокой максимальной продолжительностью жизни распространяется не только в рамках одного вида, но и на видовые отличия. Так в среднем, чем выше PARP1 у вида млекопитающих, тем дольше живет данный вид. Посмотрите на картинке. Сравнивается связь PARP1 в лейкоцитах клеток с максимальной продолжительностью жизни крыс, кролика, морской свинки, мартышки, овцы, коровы, свиньи, лошади, карликовых шимпанзе, осла, гориллы, слона и человека. И чем выше PARP1 у вида млекопитающих, тем стабильнее ДНК (меньше повреждений ДНК), тем дольше живет данный вид животных.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/1465394
 2016 Токийский медицинский и стоматологический Университет показал, что старение волосяного фолликула и потеря волос также связаны с повреждением ДНК в стволовых клетках. А NAD+ Никотинамидадениндинуклеотид (NAD) кофермент, присутствующий во всех живых клетках, отодвигают облысение и поседение на попозже. На данном примере также видно, что повреждение ДНК влияет на внешнее старение человека, а не только на риск онкологических заболеваний. Защита ДНК стволовых клеток, ответственных за рост и цвет волос, является действенной стратегией предупреждения поседения и потери волос с возрастом. А оценивать окислительный стресс можно по маркеру разрушения ДНК и окислительного стресса 8- oxo-dG.
2016 Токийский медицинский и стоматологический Университет показал, что старение волосяного фолликула и потеря волос также связаны с повреждением ДНК в стволовых клетках. А NAD+ Никотинамидадениндинуклеотид (NAD) кофермент, присутствующий во всех живых клетках, отодвигают облысение и поседение на попозже. На данном примере также видно, что повреждение ДНК влияет на внешнее старение человека, а не только на риск онкологических заболеваний. Защита ДНК стволовых клеток, ответственных за рост и цвет волос, является действенной стратегией предупреждения поседения и потери волос с возрастом. А оценивать окислительный стресс можно по маркеру разрушения ДНК и окислительного стресса 8- oxo-dG.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/26912707
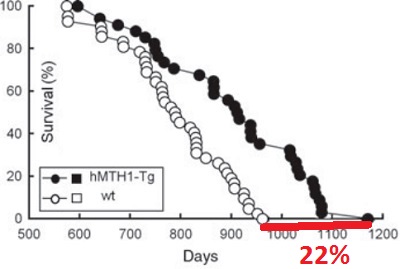 В 2013 год (Италия). Белок MTH1 участвует в ремонте повреждений ДНК и РНК. А генетическая сверх экспрессия MTH1 увеличивает продолжительность жизни у трансгенных мышей на 22% в сравнении с мышами дикого типа. У таких мышей геномные повреждения с возрастом накапливались гораздо меньше, что также можно увидеть по маркеру повреждения ДНК 8-oxodG, который имеет более низкие значения у пожилых трансгенных животных со сверх экспрессией MTH1. На графике видно, как растет их продолжительность жизни.
В 2013 год (Италия). Белок MTH1 участвует в ремонте повреждений ДНК и РНК. А генетическая сверх экспрессия MTH1 увеличивает продолжительность жизни у трансгенных мышей на 22% в сравнении с мышами дикого типа. У таких мышей геномные повреждения с возрастом накапливались гораздо меньше, что также можно увидеть по маркеру повреждения ДНК 8-oxodG, который имеет более низкие значения у пожилых трансгенных животных со сверх экспрессией MTH1. На графике видно, как растет их продолжительность жизни.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/23648059
Существует очень много механизмов ремонта ДНК. И все они очень сильно влияют на продолжительность жизни и скорость старения. Приведем еще несколько примеров.
Ген Ercc1 участвуют в восстановлений повреждений ДНК. Мышей с дефицитом гена Ercc1 (Ercc1∆/-) показывают многочисленные функции ускоренного старения. Сокращение калорий на 30% у таких мышей продлевает жизнь в 3 раза.
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/27556946
Люди долгожители от 100 до 107 лет имеют более высокие ферменты ремонта ДНК (PARP1 и Ku70) чем у (69 до 75 лет). А мыши с дефицитом Ku70 (Ku70 -/-) быстро стареют и живут примерно в 2 раза меньше. При дефиците и PARP1 и Ku70 также наблюдается более высокое повреждение ДНК. Которое определяется повышением маркера разрушения ДНК 8-oxo-dG.
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/21600302
- www.ncbi.nlm.nih.gov/pubmed/17518695
- www.ncbi.nlm.nih.gov/pmc/articles/PMC2169178
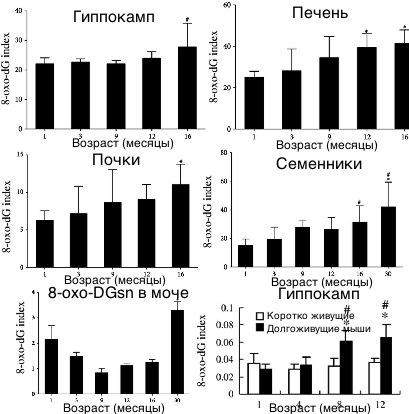 На графике слева показан эксперимент в котором замеряли маркер повреждения ДНК и окислительного стресса 8-oxo-dGsn в различных органах и системах крыс. Мы можем видеть, что в гиппокампе крыс в возрасте 16 месяцев (эквивалент 40 годам человека) повышается скорость накопления повреждений ДНК - повышался окислительный стресс. Мы также видим, что в печени, в почках, в семенниках скорость повреждения ДНК и окислительного стресса растет с возрастом. На диаграмме слева внизу видно, что маркер повреждения ДНК и окислительного стресса 8-oxo-dGsn в моче у крыс высокий в детстве и в возрасте 16 месяцев. В детстве - потому что организм растет. Во время роста клетки быстро делятся, а ДНК быстрее создают копии новых ДНК, что ведет к повышению количества ошибок и возникновения мутаций. Повышение в моче крыс маркера повреждения ДНК 8-oxo-dGsn в 16 месяцев связано с повышением окислительного стресса в процессе старения животных. Также на нижнем графике справа видно что в гиппокампе короткоживущих мышей уже в 8 месяцев повышается маркер повреждения ДНК 8-oxo-dGsn в отличии от нормально живущих мышей. Мыши с ускоренным старением (SAMP8) имеют раннее снижение способности к обучению и ухудшение памяти. У более долгоживущих мышей (SAMR1) накопление 8-oxo-dGsn не наблюдалось в таком раннем возрасте
На графике слева показан эксперимент в котором замеряли маркер повреждения ДНК и окислительного стресса 8-oxo-dGsn в различных органах и системах крыс. Мы можем видеть, что в гиппокампе крыс в возрасте 16 месяцев (эквивалент 40 годам человека) повышается скорость накопления повреждений ДНК - повышался окислительный стресс. Мы также видим, что в печени, в почках, в семенниках скорость повреждения ДНК и окислительного стресса растет с возрастом. На диаграмме слева внизу видно, что маркер повреждения ДНК и окислительного стресса 8-oxo-dGsn в моче у крыс высокий в детстве и в возрасте 16 месяцев. В детстве - потому что организм растет. Во время роста клетки быстро делятся, а ДНК быстрее создают копии новых ДНК, что ведет к повышению количества ошибок и возникновения мутаций. Повышение в моче крыс маркера повреждения ДНК 8-oxo-dGsn в 16 месяцев связано с повышением окислительного стресса в процессе старения животных. Также на нижнем графике справа видно что в гиппокампе короткоживущих мышей уже в 8 месяцев повышается маркер повреждения ДНК 8-oxo-dGsn в отличии от нормально живущих мышей. Мыши с ускоренным старением (SAMP8) имеют раннее снижение способности к обучению и ухудшение памяти. У более долгоживущих мышей (SAMR1) накопление 8-oxo-dGsn не наблюдалось в таком раннем возрасте
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pmc/articles/PMC3657452
- www.ncbi.nlm.nih.gov/pubmed/1973592
Есть и другие маркеры окислительного стресса. Так соотношение уровня глутатиона (GSH) и окисленного глутатиона (GSSG) также является показателем окислительного стресса. Но часто бывает, что GSH в норме, а маркер повреждения ДНК и окислительного стресса 8-oxo-dGsn повышен. Что указывает на то, что 8-oxo-dGsn является более точным, так как показывает именно само разрушение ДНК. Например, у пожилых самцов мышей такой же уровень GSH, как и у пожилых самок, а вот 8-oxo-dGsn у пожилых самцов выше, чем у пожилых самок.
Ссылки на исследования:
- www.ncbi.nlm.nih.gov/pubmed/19883294
Тем не менее все, что снижает глутатион, повышает окислительный стресс и повышает 8-oxo-dGsn. А уровень глутатиона снижается с возрастом.
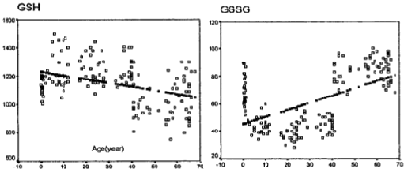 В 2002 году Университет Османгази в Турции опубликовал исследование в котором показал, что содержание глутатиона в клетках снижается в процессе старения даже при отсутствии заболеваний. Смотрите график этого исследования — слева. Уже после 40 лет уровень глутатиона (GSH) в плазме крови у 176 здоровых людей начинает резко снижаться, а уровень окисленного глутатиона (GSSG) резко повышаться. Это происходит из-за снижения скорости синтеза глутатиона. То есть после 40 лет резко повышается окислительный стресс для ДНК, ускоряется старение, повышается уровень ошибок ДНК и мутаций ДНК. Мы это видим, как резкое ускорение внешнего старения. После 40 лет в геометрической прогрессии растет вероятность заболевать раком, начинают снижаться умственные способности, резко снижаются спортивные результаты
В 2002 году Университет Османгази в Турции опубликовал исследование в котором показал, что содержание глутатиона в клетках снижается в процессе старения даже при отсутствии заболеваний. Смотрите график этого исследования — слева. Уже после 40 лет уровень глутатиона (GSH) в плазме крови у 176 здоровых людей начинает резко снижаться, а уровень окисленного глутатиона (GSSG) резко повышаться. Это происходит из-за снижения скорости синтеза глутатиона. То есть после 40 лет резко повышается окислительный стресс для ДНК, ускоряется старение, повышается уровень ошибок ДНК и мутаций ДНК. Мы это видим, как резкое ускорение внешнего старения. После 40 лет в геометрической прогрессии растет вероятность заболевать раком, начинают снижаться умственные способности, резко снижаются спортивные результаты
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/11835271
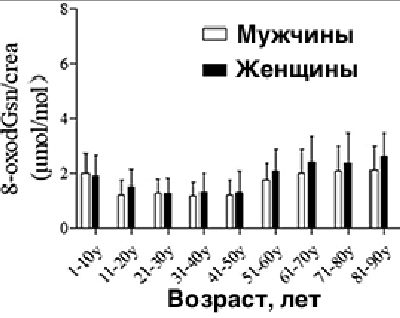 2018 год, Сычуаньский Университет и Национальный Центр Геронтологии, Китай. Исследовались 1 228 здоровых жителей Китая (613 мужчин и 615 женщин) в возрасте 2-90 лет. Оценивалась связь между 8-oxo-dGsn и возрастом/полом. Наблюдалось возрастное увеличение значения 8-oxo-dGsn с возрастом, начиная с 40-50 летнего возраста (см. график слева).
2018 год, Сычуаньский Университет и Национальный Центр Геронтологии, Китай. Исследовались 1 228 здоровых жителей Китая (613 мужчин и 615 женщин) в возрасте 2-90 лет. Оценивалась связь между 8-oxo-dGsn и возрастом/полом. Наблюдалось возрастное увеличение значения 8-oxo-dGsn с возрастом, начиная с 40-50 летнего возраста (см. график слева).
Ссылка на исследование:
- www.ncbi.nlm.nih.gov/pubmed/29535624
Как же использовать 8-oxo-dGsn для диагностики старения? Все просто. Если мы сдаем анализ на 8-oxo-dGsn, затем что-то в жизни (лечение, образ жизни, болезни) повышает уровень 8-oxo-dGsn в следующем анализе, то значит такое лечение, образ жизни или болезни были ускоряющими наше старение. И наоборот. Хотя наоборот имеет нюансы - нельзя снижать 8-oxo-dGsn в клетках рака. Иначе они лучше выживают.
норма - 0.1-0.3 ng/mL
Предлагаем Вам оформить почтовую подписку на самые новые и актуальные новости, которые появляются в науке, а также новости нашей научно-просветительской группы, чтобы ничего не упустить.
 Автор статьи — Веремеенко Дмитрий Евгеньевич, основатель исследовательского проекта, изучающего терапии, направленные на увеличение продолжительности жизни человека "Лаборатория Экспертных Исследований Тераностика_про" (nestarenie.ru/slb-expert_.html), создатель экспертной системы Тераностика_про, основатель Nestarenie Camp (https://nestareniecamp.ru), со-основатель on-line курса Nestarenie, автор книги "Диагностика старения" (https://nestarenie.ru/Diagnostika.pdf), и со-автор книги "Как дожить до 22 века" (http://book.hostenko.com), создатель блога https://nestarenie.ru, Тел. +7 925 9244328 Dmitriy-tae@yandex.ru
Автор статьи — Веремеенко Дмитрий Евгеньевич, основатель исследовательского проекта, изучающего терапии, направленные на увеличение продолжительности жизни человека "Лаборатория Экспертных Исследований Тераностика_про" (nestarenie.ru/slb-expert_.html), создатель экспертной системы Тераностика_про, основатель Nestarenie Camp (https://nestareniecamp.ru), со-основатель on-line курса Nestarenie, автор книги "Диагностика старения" (https://nestarenie.ru/Diagnostika.pdf), и со-автор книги "Как дожить до 22 века" (http://book.hostenko.com), создатель блога https://nestarenie.ru, Тел. +7 925 9244328 Dmitriy-tae@yandex.ru
Группа nestarenieRU в Facebook www.facebook.com/groups/nestarenie
Мой аккаунт в Facebook: https://www.facebook.com/nestarenieRU
YouTube-канал https://www.youtube.com/c/nestarenieRU
Знаете ли вы, что сайт nestarenie.ru — объективно один из самых популярных в России ресурсов про старение и долголетие - в Яндексе, в Гугле, по количеству, качеству и лояльности аудитории. nestarenie.ru имеет потенциал, чтобы стать одним из самых популярных сайтов о борьбе со старением не только в России, но и в мире. Для этого нужны деньги. Я призываю всех сделать пожертвования, а также убедить своих друзей поступить аналогично.
-
-
- Карта Viza (доллары): 4215 8901 1587 0138 для переводов за пределами РФ
- Карта МИР в Сбере (рубли): 2202 2032 1501 6686 (МАЙЯВИ Ч.) - на территории РФ
-
Узнайте подробнее помочь развитию блога.
Рекомендуем ещё почитать следующие статьи:
- Метформин - самое изученное и надёжное лекарство от старости.
- Подробная программа продления жизни научно доказанными способами.
- Витамин K2 (МК-7) сокращает смертность
- Витамин B6+магний снижают смертность на 34%
- Глюкозамин Сульфат эффективно продлевает жизнь и защищает от многих видов рака
- Фолаты для предупреждения раннего старения
- Как победить метилглиоксаль — вещество, которое нас старит.
Обязательно оставляйте свои комментарии под статьей, которую Вы читаете. Это очень важно для нас.
Предлагаем Вам оформить почтовую подписку на самые новые и актуальные новости, которые появляются в науке, а также новости нашей научно-просветительской группы, чтобы ничего не упустить. Обязательно оставляйте свои комментарии под статьей, которую вычитаете. Это очень важно для нас.

Автор статьи
Веремеенко Дмитрий Евгеньевич
Телефон:
Почта:
Сфера деятельности - data science в медицине
Основатель проекта, изучающего терапии, направленные на увеличение продолжительности жизни человека (nestarenie.ru/slb-expert_.html)
Со-основатель IT сервиса продления жизни
Основатель форума о продлении жизни Nestarenie Camp (nestarenie.ru/camp.html)
Со-автор книги "Бонусные годы" (nestarenie.ru/kniga-3.html)
Создатель справочного блога о старении человека (nestarenie.ru)
Социальные сети:
- Карта Viza (доллары): 4215 8901 1587 0138 для переводов за пределами РФ
- Карта МИР в Сбере (рубли): 2202 2032 1501 6686 (МАЙЯВИ Ч.) - на территории РФ
53 комментария
-
Антон16 февраля 2022, 10:59
Добрый день.
Интересует вопрос о поседение волос – на данный момент есть ли какие то доказанные средства для защиты от седины? -
Валерий14 сентября 2018, 04:03
Дмитрий, добрый день! Спасибо Вам за полезные статьи!
Подскажите пожалуйста, что необходимо принимать мужщинам , чтобы предупредить потерю и поседение волос? Спасибо!
-
а03 августа 2018, 03:51
капсаицин митогерментин?
-
Алекс Локк21 июня 2018, 13:24
Дмитрий, а есть ли понимание, насколько быстро накапливается и выводится 8-oxo-dGsn, за какой диапазон времени он показывает результаты?
Например: я скорректировал образ жизни, через сколько недель имеет смысл сдавать маркер?
Другой пример: я принимаю митогорметины + раз в 2 недели 450мг рутина. Покажет ли маркер усреднённый результат за несколько недель, или сразу снизится после приёма рутина? -
Kонстантин02 июня 2018, 19:39
Дмитрий, а 8-hydroxy-2-deoxyguanosine – это другой показатель? Он не настолько точен как -ОН-дезоксигуанозин? Спасибо!
-
Kонстантин11 мая 2018, 03:39
Дмитрий, а что вы думаете про использование отношения между этими двумя биомаркерами для оценки оксидативного стресса и/или антиоксидантной защиты?
– Glutathione (reduced)
– Glutathione (oxidized)А также соотношение этих двух:
S-adenosylmethionine (RBC)
S-adenosylhomocysteine (RBC)Некотороые практики считают, что если соотношение сильно перекошено в определенную сторону, то может иметь смысл на него влиять. Вы не согласитесь?
-
Юрий10 мая 2018, 17:36
Дмитрий, можете что-то написать об информативности эитого анализа – например на примере своих коллег? Я как и Павел – не очень пока понимаю его смысл. Спасибо.
-
Pavel26 апреля 2018, 14:43
Дмитрий, а как обстоят дела с чувствительностью теста на 8-oxo-dGsn в рамках интервенций против старения? Как видно из схемы, уровни его практически одинаковы, что для 20-летнего, что для 45-летнего человека, хотя у последнего поломок в ДНК и мутаций гораздо больше. Может ли тогда этот анализ детектировать небольшие изменения в диете, уровне физ. активности, приёме БАДов и прочем? Если отбросить ситуации полётов в космос или употребления по литру водки в сутки (тут уровень скорее всего повысится). Вы или Ваши коллеги уже сдавали этот анализ, насколько он всё-таки оказался информативен?
-
Матвей29 марта 2018, 13:00
Спасибо за ценную инфо.
Просьба уточнить количественные значения маркера 8-oxo-dGsn (диапазон реф. значений)
На сайте лаборатории (dnkom.ru) не нашел пример такого анализа (там только и деньги и описание процедуры).
Спасибо. -
Наталья10 февраля 2018, 11:28
Дмитрий, как по-Вашему, если ставить рейтинг важности измерений параметров, чтобы контролировать организм, то маркер 8-oxo-dGsn будет каким по списку, то есть насколько он диагностически важен? Просто пытаюсь понять, если не все можно по разным причинам измерить, то , что важнее??: ОАК, БАК, СРБ, онкомаркеры, глюк. гемоглобин, ИФР, интерлейкин, витамин Д?
-
Виктория09 февраля 2018, 18:12
Анализ на Маркер повреждения ДНК 8-oxo-dGsn получается можно сделать только в Москве? ((( В Украине я не нашла такого анализа где можно сдать(
-
Na09 февраля 2018, 10:16
В чем заключается гипокислородная терапия?
-
Татьяна08 февраля 2018, 16:50
Дима! Здравствуйте , а где можно найти лекцию по метрологии нам? С уважением Татьяна
-
Александр08 февраля 2018, 16:07
Дмитрий, теперь в программе “НЕСТАРЕНИЕ” будет 200гр. брокколи?
-
Pavel08 февраля 2018, 13:38
Получается, маркер необходим только при тестировании митогорметинов, чтоб не спровоцировать избыточный оксидативный стресс. Ведь если потреблять антиоксиданты, ДНК во всех клетках (в том числе, раковых) будет защищена, а маркер будет низким и создавать иллюзию благополучия. Или это неправильный ход мыслей?
-
Л.Б.08 февраля 2018, 09:02
Не совсем понятно каким должно быть значение этого маркера. Его высокий уровень будет говорить о накоплении мутаций за весь предыдущий период жизни? Или это повреждение ДНК в данный момент? Если не увлекаться митогорметинами и антиоксидантами (т.е. руководствоваться алгоритмом), то нет смысла делать этот анализ?
-
Татьяна08 февраля 2018, 06:07
Спасибо Дмитрий за прекрасную лекцию по митогорметинам, прослушанную вчера.
Очень, содержательно, широкий объем научный выдержек, доступным языком и интересно! Видно, что проделан огромный труд и затрачено колоссальное количество времени. С уважением, Татьяна -
Константин08 февраля 2018, 00:54
Вопрос по поводу вашего комментария о сочетании 2+ митогерментинов одновременно. Можно/нужно ли сочетать брокколи с тренировками: например, в виде ростков сразу перед или сразу после тренировки? Или же лучше отделять хотя бы одним днем?
Такой же вопрос про глюкозамин.
-
Виктория08 февраля 2018, 19:59
Дмитрий, как всегда спасибо за ваш труд. Хочу немного уточнить, не совсем поняла. Вы пишите: “Повышение дозы митогорметина, либо одновременное применение двух митогорметинов может повысить АФК выше возможностей стрессоустойчивости организма и повысить окислительный стресс. ” и далее приводится перечень митогорметинов. Вопрос: применение не более двух это в течении дня? За один прием? Или можно в течении дня но разделять приемы с промежутком в час?
-
Свежие комментарии
Подпишитесь на свежие статьи
Предлагаем Вам оформить почтовую подписку на самые новые и актуальные новости, которые появляются в науке, а также новости нашей научно-просветительской группы, чтобы ничего не упустить.
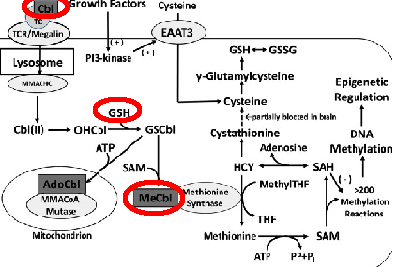
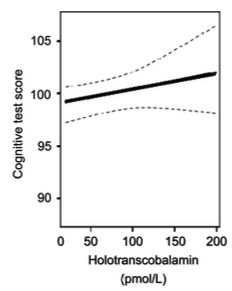 Хорошо отражает внутриклеточный уровень витамина б12 его активная форма – голотранскобаламин (который будет измерять с 1 августа в панели OL 1.3 вместо общего б12 – кстати). Его уровень хорошо коррелирует с когнитивными функциями (см. рисунок сверху). В то время как гомоцистеин был малоинформативен.
Хорошо отражает внутриклеточный уровень витамина б12 его активная форма – голотранскобаламин (который будет измерять с 1 августа в панели OL 1.3 вместо общего б12 – кстати). Его уровень хорошо коррелирует с когнитивными функциями (см. рисунок сверху). В то время как гомоцистеин был малоинформативен.